Hỗn hợp X gồm Cu,Fe,Al. Cho 0,5 mol X tác dụng với HCl được 0,4 mol H2.Biết 47,6 gam X tác dụng hoàn toàn với 29,12 lít Cl2. Tính phần trăm khối lượng Fe trong X

Những câu hỏi liên quan
Cho 20,4 gam hỗn hợp X gồm Fe, Zn, Al tác dụng với dung dịch H2SO4 dư thu được 10,08 lít H2 (đktc). Mặt khác cho 0,2 mol X tác dụng vừa đủ với 6,16 lít Cl2 (đktc). Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp X biết Fe + Cl2 ® FeCl3 Zn + Cl2 ® ZnCl2 Al + Cl2 ® AlCl3
Đọc tiếp
Cho 20,4 gam hỗn hợp X gồm Fe, Zn, Al tác dụng với dung dịch H2SO4 dư thu được 10,08 lít H2 (đktc). Mặt khác cho 0,2 mol X tác dụng vừa đủ với 6,16 lít Cl2 (đktc). Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp X biết
Fe + Cl2 ® FeCl3
Zn + Cl2 ® ZnCl2
Al + Cl2 ® AlCl3
Gọi $n_{Fe} = a(mol), n_{Zn} = b(mol) , n_{Al} = c(mol) \Rightarrow 56a + 65b + 27c = 20,4(1)$
$Fe + H_2SO_4 \to FeSO_4 + H_2$
$Zn + H_2SO_4 \to ZnSO_4 + H_2$
$2Al +3 H_2SO_4 \to Al_2(SO_4)_3 +3 H_2$
Theo PTHH : $n_{H_2} = a + b + 1,5c = \dfrac{10,08}{22,4} = 0,45(mol)(2)$
Mặt khác :
$2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
$Zn + Cl_2 \xrightarrow{t^o} ZnCl_2$
$2Al + 3Cl_2 \xrightarrow{t^o} 2AlCl_3$
Theo PTHH : $n_{Cl_2} = 1,5n_{Fe} + n_{Zn} + 1,5n_{Al}$
Suy ra : \dfrac{1,5a + b + 1,5c}{a + b + c} = \dfrac{0,275}{0,2}(3)$
Từ (1)(2)(3) suy ra : a = 0,2 ; b = 0,1 ; c = 0,1
$\%m_{Fe} = \dfrac{0,2.56}{20,4}.100\% = 54,9\%$
$\%m_{Zn} = \dfrac{0,1.65}{20,4}.100\% = 31,9\%$
$\%m_{Al} = 100\% - 54,9\% - 31,9\% = 13,2\%$
Đúng 2
Bình luận (0)
Cho 53,75 gam hỗn hợp X gồm kim loại Sn, Fe, Al tác dụng vừa đủ với 25,20 lít khí Cl2 (đktc). Mặt khác khi cho 0,40 mol hỗn hợp X tác dụng với dung dịch HCl nóng, dư thư được 9,92 lít khí H2 (đktc). Biết các phản ứng xảy ra hoàn toàn. Khối lượng của kim loại Al trong 0,40 mol hỗn hợp X có giá trị gần với A. 1,5 B. 4,0 C. 2,3 D. 3,1
Đọc tiếp
Cho 53,75 gam hỗn hợp X gồm kim loại Sn, Fe, Al tác dụng vừa đủ với 25,20 lít khí Cl2 (đktc). Mặt khác khi cho 0,40 mol hỗn hợp X tác dụng với dung dịch HCl nóng, dư thư được 9,92 lít khí H2 (đktc). Biết các phản ứng xảy ra hoàn toàn. Khối lượng của kim loại Al trong 0,40 mol hỗn hợp X có giá trị gần với
A. 1,5
B. 4,0
C. 2,3
D. 3,1
Đáp án : A
Trong 53,75g X có x mol Sn ; y mol Fe ; z mol Al
=> t(119x + 56y + 27z) = 53,75g
X + Cl2 -> SnCl4 ; FeCl3 ; AlCl3
⇒ t 4 x + 3 y + 3 z = 2 n C l 2 = 2 , 25 m o l
(Trong 0,4 mol lượng chất gấp t lần)
=> 9(119x + 56y + 27z) = 215(4x + 3y + 3z)
=> 211x – 141y – 402z = 0(1)
=> x + y + z = 0,4 mol(2)
n H 2 = x + y + 1,5z = 31/70 (mol) (3)
Từ (1,2,3) => z = 0,0857 mol
=> mAl = 2,314g
Đúng 0
Bình luận (0)
Cho 23,8 gam hỗn hợp X (Cu, Fe, Al) tác dụng vừa đủ 14,56 lít khí Cl2 (đktc). Mặt khác cứ 0,25 Mol hỗn hợp tác dụng với dung dịch HCl dư thu được 0,2 Mol khí ( đktc). Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp X.
Gọi số mol của Cu, Fe, Al trong 23,8 gam hhX lần lượt là x, y, z mol
→ mX = 64x + 56y + 27z = 23,8 (1)
\(n_{Cl_2}\) = x + 1,5y + 1,5z = 0,65 (2)
0,25 mol X + HCl → 0,2 mol H2 nên 0,2.(x + y + z) = 0,25.(y + 1,5z) (3)
Từ (1), (2), (3) => x = 0,2 mol; y = 0,1 mol; z = 0,2 mol
\(\%_{Cu} = \dfrac{0,2. 64}{23,8} \approx 53,78\%\)
\(\%_{Fe} = \dfrac{0,1 .56}{23,8} \approx 23,53\%\)
%Al ≈ 22,69%
Đúng 3
Bình luận (1)
Hỗn hợp X gồm Zn, Fe, Cu. Cho 18,5 gam hỗn hợp X vào dung dịch HCl dư,sau khi phản ứng xẩy ra hoàn toàn thu được 4,48 lít H2 (đktc). Mặt khác 0,15 mol hỗn hợp X tác dụng vừa đủ với 3,92 lít Cl2 (đktc).a). Xác định thành phần trăm khối lượng của mỗi kim loại trong X.b). Cho 18,5 gam hỗn hợp X tác dụng với oxi thu được 23,7 gam hỗn hợp oxit Y ZnO, FeO, Fe2O3, Fe3O4, CuO. Để hòa tan hết 23,7 gam Y cần dùng vừa đủ V ml dd HCl 1M. Tính V?
Đọc tiếp
Hỗn hợp X gồm Zn, Fe, Cu. Cho 18,5 gam hỗn hợp X vào dung dịch HCl dư,sau khi phản ứng xẩy ra hoàn toàn thu được 4,48 lít H2 (đktc). Mặt khác 0,15 mol hỗn hợp X tác dụng vừa đủ với 3,92 lít Cl2 (đktc).
a). Xác định thành phần trăm khối lượng của mỗi kim loại trong X.
b). Cho 18,5 gam hỗn hợp X tác dụng với oxi thu được 23,7 gam hỗn hợp oxit Y ZnO, FeO, Fe2O3, Fe3O4, CuO. Để hòa tan hết 23,7 gam Y cần dùng vừa đủ V ml dd HCl 1M. Tính V?
a)
TN1: Gọi (nZn; nFe; nCu) = (a; b; c)
=> 65a + 56b + 64c = 18,5 (1)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
a---------------------->a
Fe + 2HCl --> FeCl2 + H2
b----------------------->b
=> a + b = 0,2 (2)
TN2: Gọi (nZn; nFe; nCu) = (ak; bk; ck)
=> ak + bk + ck = 0,15 (3)
PTHH: Zn + Cl2 --to--> ZnCl2
ak-->ak
2Fe + 3Cl2 --to--> 2FeCl3
bk--->1,5bk
Cu + Cl2 --to--> CuCl2
ck-->ck
=> \(ak+1,5bk+ck=\dfrac{3,92}{22,4}=0,175\)(4)
(1)(2)(3)(4) => \(\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,1\left(mol\right)\\c=0,1\left(mol\right)\\k=0,5\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,1.65}{18,5}.100\%=35,135\%\\\%m_{Fe}=\dfrac{0,1.56}{18,5}.100\%=30,27\%\\\%m_{Cu}=\dfrac{0,1.64}{18,5}.100\%=34,595\%\end{matrix}\right.\)
b) nO(oxit) = \(\dfrac{23,7-18,5}{16}=0,325\left(mol\right)\)
=> nH2O = 0,325 (mol)
=> nHCl = 0,65 (mol)
=> \(V=\dfrac{0,65}{1}=0,65\left(l\right)=650\left(ml\right)\)
Đúng 1
Bình luận (0)
Để tác dụng hết với 35,7 gam hỗn hợp X gồm Cu, Fe, Al ở dạng bột, nung nóng cần vừa đủ 21,84 lít khí Cl2. Mặt khác, khi cho 0,25 mol hỗn hợp X tác dụng với dung dịch HCl dư thì thu được 4,48 lít khí H2. Tính % khối lượng mỗi kim loại trong hỗn hợp X. Biết thể tích các khí đó ở đktc.
\(n_{Cu}=a\left(mol\right),n_{Fe}=b\left(mol\right),n_{Al}=c\left(mol\right)\)
\(m_X=64a+56b+27b=35.7\left(g\right)\left(1\right)\)
\(n_{Cl_2}=\dfrac{21.84}{22.4}=0.975\left(mol\right)\)
\(Cu+Cl_2\underrightarrow{^{^{t^0}}}CuCl_2\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}FeCl_3\)
\(Al+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}AlCl_3\)
\(n_{Cl_2}=a+1.5b+1.5c=0.975\left(mol\right)\left(2\right)\)
\(n_{hh}=ka+kb+kc=0.25\left(mol\right)\)
\(n_{H_2}=kb+k\cdot1.5c=0.2\left(mol\right)\)
\(\Leftrightarrow a-0.25b-0.875c=0\left(3\right)\)
\(\left(1\right),\left(2\right),\left(3\right):a=0.3,b=0.15,c=0.3\)
\(\%Cu=\dfrac{0.3\cdot64}{35.7}\cdot100\%=53.78\%\)
\(\%Fe=\dfrac{0.15\cdot56}{35.7}\cdot100\%=23.52\%\)
\(\text{%Al=22.7%}\)
Đúng 1
Bình luận (0)
Cho 20,4g hỗn hợp X gồm Al,Zn và Fe tác dụng với dd HCl dư , thu được 10,08 lít H2.Mặt khác 0,2 mol X tác dụng vừa đủ với 6,16 lít Cl2. Biết thể tích các khí đo ở đktc.Phần trăm khối lượng của Fe trong hỗn hợp X là? Cảm ơn nhiều nha
TN1: Gọi (nAl; nZn; nFe) = (a; b; c)
=>27a + 65b + 56c = 20,4 (1)
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a----------------------->1,5a
Zn + 2HCl --> ZnCl2 + H2
b--------------------->b
Fe + 2HCl --> FeCl2 + H2
c----------------------->c
=> \(1,5a+b+c=0,45\) (2)
TN2: Gọi (nAl; nZn; nFe) = (ak; bk; ck)
=> ak + bk + ck = 0,2 (3)
\(n_{Cl_2}=\dfrac{6,16}{22,4}=0,275\left(mol\right)\)
PTHH: 2Al + 3Cl2 --to--> 2AlCl3
ak-->1,5ak
Zn + Cl2 -to-> ZnCl2
bk--->bk
2Fe + 3Cl2 --to--> 2FeCl3
ck--->1,5ck
=> 1,5ak + bk + 1,5ck = 0,275 (4)
(1)(2)(3)(4) => \(\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,1\left(mol\right)\\c=0,2\left(mol\right)\end{matrix}\right.\)
=> \(\%Fe=\dfrac{0,2.56}{20,4}.100\%=54,9\%\)
Đúng 3
Bình luận (1)
hỗn hợp x gồm cu ,al ,fe cho 28,6 g x tác dụng với dung dịch hcl dư sau phản ứng thu được 13,44 lít khí h2(đktc) ở nhiệt đọ cao 0,6 mol x tác dụng vừa đủ với 8,96 lít o2 (đktc) tính thành phần phần trăm theo khối lượng của các chất trong hh x
\(n_{Cu} = a ; n_{Al} = b ; n_{Fe} = c(mol)\\ \Rightarrow 64a + 27b + 56c = 28,6(1)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = 1,5b + c = \dfrac{13,44}{22,4} = 0,6(2)\\ \text{Mặt khác} : n_{O_2} = \dfrac{8,96}{22,4} = 0,4(mol)\\ 2Cu + O_2 \xrightarrow{t^o} 2CuO\\ 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ 4Fe + 3O_2 \xrightarrow{t^o} 2Fe_2O_3\\ \)
Ta có :
\(\dfrac{n_X}{n_{O_2}}=\dfrac{a+b+c}{0,5a +0,75b + 0,75c} = \dfrac{0,6}{0,4}(3)\\ (1)(2)(3)\Rightarrow a = \dfrac{317}{1460} ; b = \dfrac{121}{365}; c = \dfrac{15}{146}\\ \%m_{Cu} = \dfrac{\dfrac{317}{1460}.64}{28,6}.100\% = 48,59\%\\ \%m_{Al} = \dfrac{\dfrac{121}{365}.27}{28,6}.100\% = 31,3\%\\ \%m_{Fe} = 100\% - 41,59\% - 31,3\% = 27,11\%\)
Đúng 3
Bình luận (2)
Hỗn hợp X gồm Cu, Fe, Mg. Nếu cho 10,88 gam X tác dụng với clo dư thì sau phản ứng thu được 28,275 gam hỗn hợp muối khan. Mặt khác, 0,44 mol X tác dụng với dung dịch HCl dư thì thu được 5,376 lít H2 (đktc). Phần trăm khối lượng của Cu trong X là: A. 67,92% B. 37,23% C. 43,52% D. 58,82%
Đọc tiếp
Hỗn hợp X gồm Cu, Fe, Mg. Nếu cho 10,88 gam X tác dụng với clo dư thì sau phản ứng thu được 28,275 gam hỗn hợp muối khan. Mặt khác, 0,44 mol X tác dụng với dung dịch HCl dư thì thu được 5,376 lít H2 (đktc). Phần trăm khối lượng của Cu trong X là:
A. 67,92%
B. 37,23%
C. 43,52%
D. 58,82%
Đáp án D
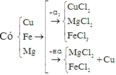
Theo định luật bảo toàn khối lượng ta có:
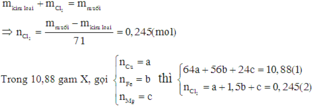
Khi cho (a + b + c) mol X tác dụng với dung dịch HCl dư thì thu được (b + c) mol H2.
Khi cho 0,44 mol X tác dụng với dung dịch HCl dư thì thu được 0,24 mol H2.
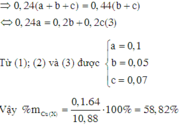
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Cu, Fe, Mg. Nếu cho 10,88 gam X tác dụng với clo dư thì sau phản ứng thu được 28,275g hỗn hợp muối khan. Mặt khác 0,44 mol X tác dụng với dung dịch HCl dư thì thu được 5,376 lít H2 (đktc). Phần trăm khối lượng của Cu trong X là: A. 67,92% B. 58,82% C. 37,23% D. 43,52%
Đọc tiếp
Hỗn hợp X gồm Cu, Fe, Mg. Nếu cho 10,88 gam X tác dụng với clo dư thì sau phản ứng thu được 28,275g hỗn hợp muối khan. Mặt khác 0,44 mol X tác dụng với dung dịch HCl dư thì thu được 5,376 lít H2 (đktc). Phần trăm khối lượng của Cu trong X là:
A. 67,92%
B. 58,82%
C. 37,23%
D. 43,52%
Đáp án B
Trong 10,88g X gọi số mol Cu, Fe và Mg là x, y, z
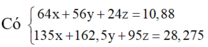
Trong 0,44 mol X có kx mol Cu, ky mol Fe và kz mol Mg (giữ đúng tỉ lệ)
Do đó kx + ky + kz = 0,44 (1)
Khi cho X tác dụng với HC1 thì
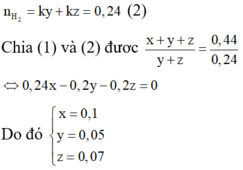
Vậy phần trăm khối lượng của Cu trong X là 58,82%
Đúng 0
Bình luận (0)















