hòa tan hoàn toàn 18,2 g hh hai muối cacbonnat trung hòa của hai kim loại hóa trị I bằng dd HCl dư, thu được 4,48 l khí CO2 (đktc). Hai kim loại đó là kim loại nào?

Những câu hỏi liên quan
5.Cho 9,1 gam hỗn hợp hai muối cacbonat trung hòa của 2 kim loại kiềm (1A) ở 2 chu kỳ liên tiếp tan hoàn toàn trong dung dịch HCl dư thu được 2,24 lít khí CO2 (đktc). Hai kim loại đó là?
Gọi công thức muối cacbonat trung hòa của 2 kim loại kiềm cần tìm là R2CO3
\(R_2CO_3+2HCl\rightarrow2RCl+H_2O+CO_2\)
\(n_{CO_2}=n_{R_2CO_3}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ \Rightarrow M_{R_2CO_3}=2M_R+60=\dfrac{9,1}{0,1}=91\\ \Rightarrow M_R=15,5\)
Do 2 kim loại kiềm ở chu kì liên tiếp nhau
=> 2 kim loại đó là Li, Na
Đúng 0
Bình luận (0)
hh X gồm 2 kim loại có hóa trị là I và II. Hòa tan hoàn toàn 19,9g hh X vào nước thu được V1 lít dd Y và 4,48 lít khí H2 (đktc). DD Z là dd hh của 2 axit HCl và H2SO4 trong đó số mol HCl gấp 2 lần số mol H2SO4
Trung hòa V1 lít dd Y bằng V2 lít dd Z tạo ra m (g) hh muối
Tính giá trị m (g)
Bài 24. Hòa tan 3,6g một kim loại A hóa trị II bằng một lượng dư axit HCl thu được 3,36 lít khí H2 (đktc). Xác định tên kim loại ABài 25. Hòa tan hoàn toàn 8,1g kim loại A hóa trị III trong dd HCl dư thu đucợ 10,08 lít khí H2 (đktc). Xác định tên A và m HCl đã dùng
Đọc tiếp
Bài 24. Hòa tan 3,6g một kim loại A hóa trị II bằng một lượng dư axit HCl thu được 3,36 lít khí H2 (đktc). Xác định tên kim loại A
Bài 25. Hòa tan hoàn toàn 8,1g kim loại A hóa trị III trong dd HCl dư thu đucợ 10,08 lít khí H2 (đktc). Xác định tên A và m HCl đã dùng
Bài 24:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:A+2HCl\rightarrow ACl_2+H_2\uparrow\)
Theo pthh: nA = nH2 = 0,15 (mol)
=> MA = \(\dfrac{3,6}{0,15}=24\left(\dfrac{g}{mol}\right)\)
=> A là Mg
Bài 25:
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\\ PTHH:2A+6HCl\rightarrow2ACl_3+3H_2\uparrow\\ Mol:0,3\leftarrow0,9\leftarrow0,3\leftarrow0,45\\ \rightarrow\left\{{}\begin{matrix}M_A=\dfrac{8,1}{0,3}=27\left(\dfrac{g}{mol}\right)\Rightarrow A:Al\\m_{HCl}=0,9.36,5=32,85\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (1)
Bài 24.
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(n_A=\dfrac{3,6}{M_A}\) mol
\(A+2HCl\rightarrow ACl_2+H_2\)
0,15 0,15 ( mol )
\(\Rightarrow\dfrac{3,6}{M_A}=0,15mol\)
\(\Leftrightarrow M_A=24\) ( g/mol )
=> A là Magie ( Mg )
Bài 25.
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45mol\)
\(n_A=\dfrac{8,1}{M_A}\) mol
\(2A+6HCl\rightarrow2ACl_3+3H_2\)
0,3 0,45 ( mol )
\(\Rightarrow\dfrac{8,1}{M_A}=0,3\)
\(\Leftrightarrow M_A=27\) g/mol
=> A là nhôm ( Al )
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn hai kim loại kiềm liên tiếp nhau bằng dung dịch HCl dư thu được 63,3g muối và 6,72 lít khí hidro (đktc) tìm kim loại kiềm đó
Gọi công thức chung 2 kim loại là R
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2R + 2HCl --> 2RCl + H2
_________________0,6<--0,3
=> \(M_{RCl}=\dfrac{63,3}{0,6}=105,5\left(g/mol\right)\)
=> MR = 70 (g/mol)
Mà 2 kim loại kiềm liên tiếp nhau
=> 2 kim loại là K, Rb
Đúng 2
Bình luận (0)
hòa tan hoàn toàn 18,4 gam hỗn hợp 2 muối cacbonat của 2 kim loại X,Y thuộc rnhóm IIA và thuộc hai chu kì liên tiếp bằng dung dịch HCl thu được 4,48 lít CO2 (đktc). Hai kim loại X,Y là ?
n muối = n CO2 = 0,2 mol
--> PTK muối = 18,4/0,2 = 92
--> NTK kim loại = 92 - 60 = 32
Vì 24 < 32 < 40 --> hai kim loại là Mg và Ca
Đúng 0
Bình luận (1)
Hòa tan hoàn toàn 23,8 gam hỗn hợp một muối cacbonat của các kim loại hóa trị I và muối cacbonat của kim loại hóa trị II trong dung dịch HCl. Sau phản ứng thu được 4,48 lít khí (đktc). Đem cô cạn dung dịch thu được thì khối lượng muối khan là: A. 13 g B. 15 g C. 26 g D. 30 g
Đọc tiếp
Hòa tan hoàn toàn 23,8 gam hỗn hợp một muối cacbonat của các kim loại hóa trị I và muối cacbonat của kim loại hóa trị II trong dung dịch HCl. Sau phản ứng thu được 4,48 lít khí (đktc). Đem cô cạn dung dịch thu được thì khối lượng muối khan là:
A. 13 g
B. 15 g
C. 26 g
D. 30 g
Đáp án C
Gọi công thức của hai muối trong hỗn hợp ban đầu là A2CO3 và BCO3.
Có các phản ứng:
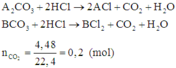
Quan sát phản ứng thấy khi cho hỗn hợp phản ứng với dung dịch HCl thì mỗi gốc C O 3 2 - trong muối được thay thế bởi hai gốc Cl-.
Có 1 mol C O 3 2 - bị thay thế bởi 2 mol Cl- thì khối lượng của muối tăng: (2.35,5 -60) = 11(gam)
Do đó khối lượng muối khan thu được khi cô cạn dung dịch là:
mmuối clorua = mmuối cacbonat + 0,2.11 = 23,8 + 0,2.11= 26 (gam)
Đúng 0
Bình luận (1)
hh d gồm fe và 1 kim loại m có hóa trị 2. hòa tan 9,6g hh d vào đ hcl dư.thì thu đc 4,48l khí (đktc). mặt khác khi hòa tan hoàn toàn 4,6g kim loại vào dd hcl dư thì thể tích h2 sinh ra chứa đến 5,6l (đktc). xác định kim loại m và tính khối lượng mỗi kim loại có trong hh
Gọi nFe=a(mol);nM=b(mol)⇒56a+Mb=9,6(1)
Fe+2HCl→FeCl2+H2
M+2HCl→MCl2+H2
nH2=a+b=0,2⇒a=0,2−b
Ta có :
56a+Mb=9,656a+Mb=9,6
⇔56(0,2−b)+Mb=9,6
⇔Mb−56b=−1,6
⇔b(56−M)=1,6
0<1,656−M<0,20<1,656−M<0,2
⇔M<48(1)
M+2HCl→MCl2+H2
⇒MM>4,60,25=18,4
+) Nếu M=24(Mg)
Ta có :
56a+24b=9,656a+24b=9,6
a+b=0,2a+b=0,2
Suy ra a = 0,15 ; b = 0,05
mFe=0,15.56=8,4(gam)
mMg=0,05.24=1,2(gam)
+) Nếu M=40(Ca)
56a+40b=9,656a+40b=9,6
a+b=0,2
Suy ra a = b = 0,1
mCa=0,1.40=4(gam)
mFe=0,1.56=5,6(gam)
Đúng 0
Bình luận (0)
Hòa tan 2,84g hh 2 muối cacbonat của 2 kim loại liên tiếp trong nhóm IIA bằng 120ml dd HCl 0,5M thu được 0,672 lít khí CO2 (đktc) và dung dịch X.
a, Tìm hai kim loại trên.
b,Tìm CM các chất trong dd X
a)
Gọi CTTQ hỗn hợp là $RCO_3$
$RCO_3 + 2HCl \to RCl_2 +C O_2 + H_2O$
$n_{hh} = n_{CO_2} = \dfrac{0,672}{22,4} = 0,03(mol)$
$\Rightarrow M_{hh} = R + 60 = \dfrac{2,84}{0,03} = 94,6 \Rightarrow R = 34,6$
Vậy hai kim loại trên là Magie và Canxi
b)
Gọi $n_{MgCO_3} = a ; n_{CaCO_3}= b$
Ta có :
$84a + 100b = 2,84$
$a + b = 0,03$
Suy ra : a = 0,01 ; b = 0,02
$n_{HCl\ dư} = 0,12.0,5 - 0,03.2 = 0$ nên HCl hết
$C_{M_{MgCl_2}} = \dfrac{0,01}{0,12} = 0,083M$
$C_{M_{CaCl_2}} = \dfrac{0,02}{0,12} = 0,167M$
Đúng 4
Bình luận (0)
4) Hòa tan hoàn toàn 14,4g một kim loại R (hóa trị II) bằng dd HCl thu được 13,44lit khí H2 (đktc). Kim loại R là:
nH2 = 13.44/22.4=0.6 (mol)
R + 2HCl => RCl2 + H2
0.6..............................0.6
MR = 14.4/0.6 = 24
=> R là : Mg
Đúng 2
Bình luận (0)
























