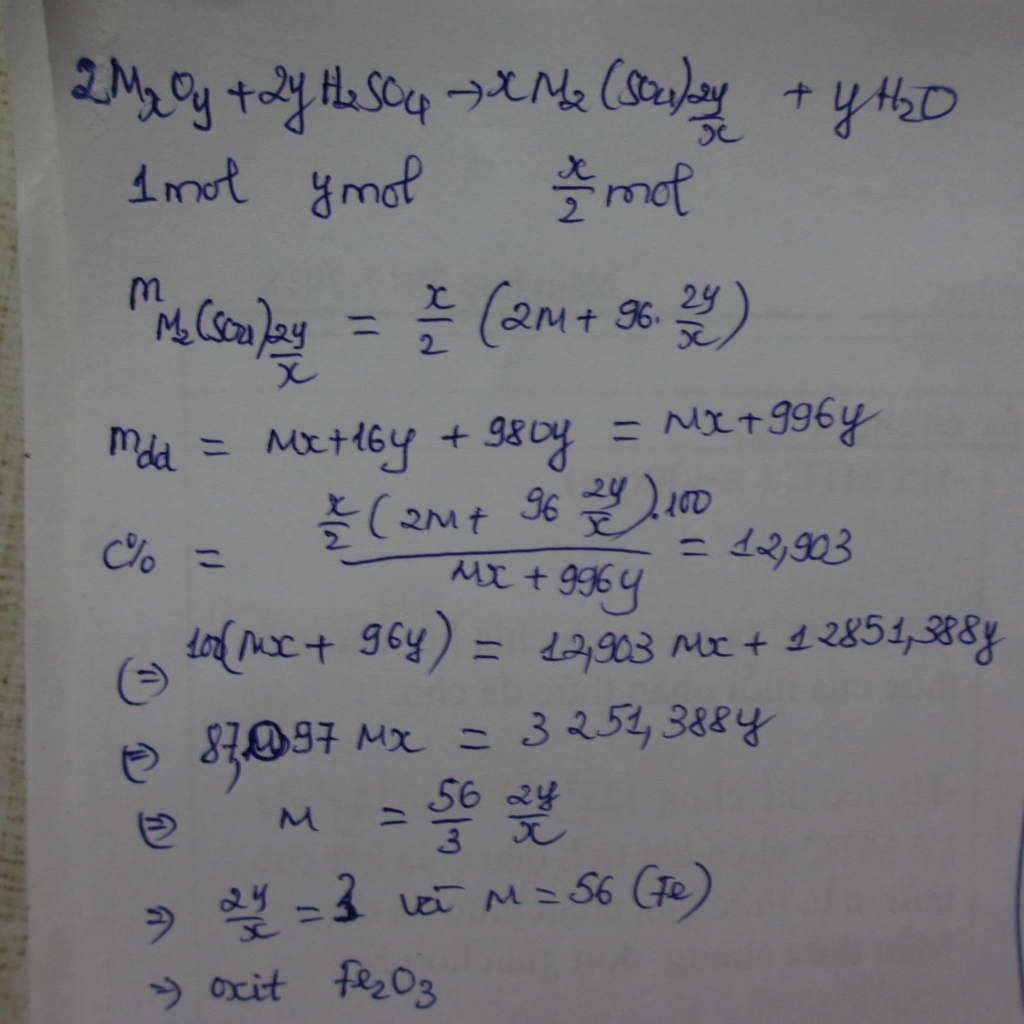Khi làm khô 27,8 gam tinh thể muối sắt (II) sunfat ngậm nước có dạng FeSO4.aH2O người ta thu được 15,5 gam FeSO4 khan. Hãy xác định giá trị a.

Những câu hỏi liên quan
khi cô cạn dd FeSO4 thì muối sunfat kết tinh với nước để tạo thành 69,5g muối ngậm nước FeSO4.nH2O. Xác định n
Em xem đề có thiếu không nè, do chỉ cho từng đấy gam muối thì chưa đủ dữ kiện đâu.
Đúng 0
Bình luận (2)
PTHH : Fe + H2SO4 →→ FeSO4 + H2
Có : nH2 = 8,4/22,4 = 0,375(mol)
Theo PT ⇒⇒ nA = nH2 = 0,375(mol)
*Gọi CTHH dạng TQ của hidrat hóa là FeSO4.nH2O
Theo PT ⇒⇒ nFeSO4 = nH2 = 0,375(mol)
⇒⇒ nFeSO4.nH2O = 0,375(mol)
⇒⇒ MFeSO4.nH2O = m/n = 104,25/0,375 = 278 (g)
hay 56 + 32+ 4.16 + x . 18= 278
⇒⇒ x = 7
Vậy CTHH của hidrat hóa là FeSO4.7H2O
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn m gam kim loại Fe bằng dung dịch H2SO4 loãng 10% vừa đủ thu được dung dịch A. Làm lạnh dung dịch A tách được 27,8 gam muối sunfat kết tinh ngậm nước và còn lại dung dịch muối sunfat bão hoà có nồng độ 10,765%. Tìm công thức muối sunfat ngậm nước. Huhu giúp mình với, mình đã tham khảo nhiều nguồn trên mạng nhưng vẫn không biết cách giải🥺
Khi kết tinh dung dịch
FeSO
4
, người ta sẽ thu được một tinh thể ở dạng ngậm nước. Công thức của tinh thể đó là A.
FeSO
4
.
6
H
2
O
B.
FeSO
4
.
4
H
2
O
C.
FeSO
4...
Đọc tiếp
Khi kết tinh dung dịch FeSO 4 , người ta sẽ thu được một tinh thể ở dạng ngậm nước. Công thức của tinh thể đó là
A. FeSO 4 . 6 H 2 O
B. FeSO 4 . 4 H 2 O
C. FeSO 4 . 7 H 2 O
D. FeSO 4 . 5 H 2 O
Câu 1. Cho 11,2 gam sắt vào dung dịch chứa 14,7 gam axit sunfuric H2SO4, sau phản ứng thu được m gam muối sắt (II) sunfat FeSO4 và V lít khí hiđro (đktc).a. Tính giá trị của m và V.b. Tính khối lượng chất còn dưCâu 2. Đốt cháy hoàn toàn 12,4 gam photpho trong bình chứa 13,44 lít khí oxi (đktc) tạo ra chất rắn màu trắng điphotpho pentaoxit (P2O5).a. Cho biết sau phản ứng, chất nào còn dư?b. Tính khối lượng sản phẩm tạo thành?
Đọc tiếp
Câu 1. Cho 11,2 gam sắt vào dung dịch chứa 14,7 gam axit sunfuric H2SO4, sau phản ứng thu được m gam muối sắt (II) sunfat FeSO4 và V lít khí hiđro (đktc).
a. Tính giá trị của m và V.
b. Tính khối lượng chất còn dư
Câu 2. Đốt cháy hoàn toàn 12,4 gam photpho trong bình chứa 13,44 lít khí oxi (đktc) tạo ra chất rắn màu trắng điphotpho pentaoxit (P2O5).
a. Cho biết sau phản ứng, chất nào còn dư?
b. Tính khối lượng sản phẩm tạo thành?
1a. PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{14,7}{1.2+32+16.4}=0,15\left(mol\right)\)
Do \(\dfrac{0,2}{1}>\dfrac{0,15}{1}\) => Fe dư, H2SO4 hết.
- Theo PTHH \(\Rightarrow n_{H_2SO_4}=n_{FeSO_4}=n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{FeSO_4}=0,15.152=22,8\left(g\right)\\V_{H_2}=0,15.22,4=3,36\left(l\right)\end{matrix}\right.\)
Đúng 4
Bình luận (0)
Hòa tan 19,6 gam Sắt vào dung dịch axit sunfuric H2 SO4 loãng thu được muối sắt(II) sunfat FeSO4 và khí hiđro.
$n_{Fe}=\frac{19,6}{56}=0,35(mol)$
$Fe+H_2SO_4\to FeSO_4+H_2$
Theo PT: $n_{H_2SO_4}=n_{FeSO_4}=n_{H_2}=0,35(mol)$
$\to m_{H_2SO_4}=0,35.98=34,3(g)$
$m_{FeSO_4}=0,35.152=53,2(g)$
$m_{H_2}=0,35.2=0,7(g)$
Đúng 1
Bình luận (0)
Bài 1 Hòa tan 3,2 gam oxit M2Om trong một lượng vừa đủ dd H2SO4 10% thu được dd muối Sunfat 12,9%. Cô cạn dd muối rồi l làm lạnh dd thấy thoát ra 7,868 gam tinh muối sunfat với hiệu suất muối kết tinh là 70%. Hãy xác định công thức của tinh thể ngậm nước
Để hòa tan hoàn toàn 20 gam 1 oxit kim loại hóa trị 2, cần dùng 100 gam dd H2SO4 24,5 %. Đun nhẹ dd sau phản ứng thu được 62,5 gam tinh thể muối ngậm nước . Xác định CTHH của oxit và tinh thể muối ngậm nước
\(n_{H_2SO_4}\) = \(\frac{100.24,5\%}{98}\) = 0,25 (mol)
Gọi CTHH của oxit kim loại hóa trị ll là MO
MO + H2SO4 \(\rightarrow\) MSO4 + H2O
0,25<--- 0,25 ---> 0,25 (mol)
MMO = \(\frac{20}{0,25}\) = 80 (g/mol)
\(\Rightarrow\) M = 80 - 16 = 64 (g/mol)
\(\Rightarrow\) M = 64 đvC (Cu : đồng)
\(\Rightarrow\) CuO
Gọi CTHH của tinh thể là CuSO4 . nH2O
ntinh thể = nCuSO4 = 0,25 (mol)
M tinh thể = \(\frac{62,5}{0,25}\) = 250 (g/mol)
\(\Rightarrow\) 160 + 18n = 250
\(\Rightarrow\) n =5
\(\Rightarrow\) CTHH của tinh thể là CuSO4.5H2O
Đúng 0
Bình luận (2)
Khi làm lạnh 29 gam dung dịch Fe(NO3)3 41,724%, người ta thu được 8,08 gam tinh thể Fe(NO3)3.nH2O và dung dịch muối còn lại có nồng độ 34,704%. Tìm công thức tinh thể ngậm nước. 9
$n_{Fe(NO_3)_3} = \dfrac{29.41,724\%}{242} = 0,05(mol)$
$m_{dd\ sau\ tách\ tinh\ thể} = 29 - 8,08 = 20,92(gam)$
$n_{Fe(NO_3)_3\ sau\ tách\ tinh\ thể} = \dfrac{20,92.34,704\%}{242} = 0,03(mol)$
$\Rightarrow n_{Fe(NO_3)_3.nH_2O} = 0,05 - 0,03 = 0,02(mol)$
$\Rightarrow M_{Fe(NO_3)_3.nH_2O} = 242 + 18n = \dfrac{8,08}{0,02} = 404$
$\Rightarrow n = 9$
Vậy CT của tinh thể là $Fe(NO_3)_3.9H_2O$
Đúng 2
Bình luận (0)
cho 7,32g tinh thể BaCl2.aH2O vào nước được 600ml dung dịch BaCl2 0,05M xác định muối ngậm nước
\(n_{BaCl_2}=0,6\cdot0,05=0,03mol\)
\(\Rightarrow n_{BaCl_2\cdot aH_2O}=n_{BaCl_2}=0,03mol\)
\(M_{BaCl_2.aH_2O}=\dfrac{7,32}{0,03}=244\)
\(\Rightarrow208+18a=244\Rightarrow a=2\)
Vậy muối là \(BaCl_2.2H_2O\)
Đúng 4
Bình luận (0)