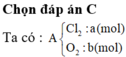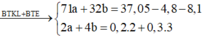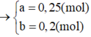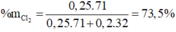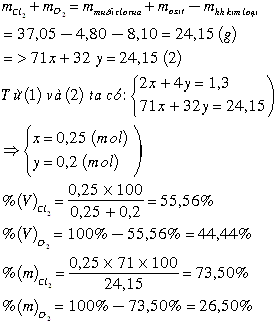Hỗn hợp khí A gồm clo và oxi. A phản ứng vừa hết với một hỗn hợp gồm 4,6 gam magie và 8,1 gam nhôm tạo ra 37.05 gam hỗn hợp các muối clorua và oxit của hai kim loại. Xác định thành phần phần trăm theo khối lượng và thể tích của hỗn hợp A

Những câu hỏi liên quan
Hỗn hợp khí A gồm clo và oxi. A phản ứng hết với hỗn hợp gồm 4,80 gam magie và 8,10 gam nhôm tạo ra 37,05 gam hỗn hợp các muối clorua và oxit của hai kim loại. Phần trăm theo khối lượng của clo trong A là A. 73,50%. B. 55,56%. C. 44,44%. D. 26,50%.
Đọc tiếp
Hỗn hợp khí A gồm clo và oxi. A phản ứng hết với hỗn hợp gồm 4,80 gam magie và 8,10 gam nhôm tạo ra 37,05 gam hỗn hợp các muối clorua và oxit của hai kim loại. Phần trăm theo khối lượng của clo trong A là
A. 73,50%.
B. 55,56%.
C. 44,44%.
D. 26,50%.
Đáp án A

Gọi số mol các chất trong A là Cl2 : a mol ; O2 : b mol
Sơ đồ phản ứng:

Tổ hợp (1) và (2) ta được : a = 0,25 mol ; b = 0,2 mol
Phần trăm khối lượng Cl2 trong A là:
![]()
Đúng 0
Bình luận (0)
Hỗn hợp khí A gồm clo và oxi. A phản ứng vừa hết với hỗn hợp gồm 4,8 gam magie và 8,1 gam nhôm tạo ra 37,05 gam hỗn hợp các muối clorua và oxit của 2 kim loại. Tính số mol clo và oxi trong A.
Gọi số mol Cl 2 và O 2 lần lượt là x và y, ta có hệ phương trình:
2x+4y = 0,4+0,9 ( ĐL bảo toàn e) x=0,25
71x+32y = 24,5 ( ĐL bảo toàn khối lượng) y=0,2
Đúng 0
Bình luận (0)
Hỗn hợp khí X gồm clo và oxi. Cho X phản ứng vừa hết với một hỗn hợp Y gồm 4,8 gam Mg và 8,1 gam Al, sau phản ứng thu được 37,05 gam hỗn hợp rắn Z gồm muối clorua và oxit của 2 kim loại. Phần trăm theo khối lượng của Clo trong hỗn hợp X là A. 26,5% B. 73,5% C. 62,5% D. 37,5%
Đọc tiếp
Hỗn hợp khí X gồm clo và oxi. Cho X phản ứng vừa hết với một hỗn hợp Y gồm 4,8 gam Mg và 8,1 gam Al, sau phản ứng thu được 37,05 gam hỗn hợp rắn Z gồm muối clorua và oxit của 2 kim loại. Phần trăm theo khối lượng của Clo trong hỗn hợp X là
A. 26,5%
B. 73,5%
C. 62,5%
D. 37,5%
Hỗn hợp khí A gồm Cl2 và O2. Cho A phản ứng vừa đủ với 1 hỗn hợp gồm 4,8 gam Mg và 8,1 gam Al thu được 37,05 gam hỗn hợp các muối clorua và các oxit của 2 kim loại. Thành phần % theo khối lượng của các khí trong A là: A. 90% và 10%. B. 15,5% và 84,5%. C. 73,5% và 26,5%. D. 56% và 35%.
Đọc tiếp
Hỗn hợp khí A gồm Cl2 và O2. Cho A phản ứng vừa đủ với 1 hỗn hợp gồm 4,8 gam Mg và 8,1 gam Al thu được 37,05 gam hỗn hợp các muối clorua và các oxit của 2 kim loại. Thành phần % theo khối lượng của các khí trong A là:
A. 90% và 10%.
B. 15,5% và 84,5%.
C. 73,5% và 26,5%.
D. 56% và 35%.
Hỗn hợp khí X gồm clo và oxi. Cho X phản ứng vừa hết với một hỗn hợp Y gồm 3,6
gam Mg và 5,4 gam Al, sau phản ứng thu được 29,95 gam hỗn hợp rắn Z gồm muối clorua và
oxit của 2 kim loại. Phần trăm theo khối lượng của Oxi trong hỗn hợp X là:
n Mg = 3,6/24 = 0,15(mol)
n Al = 5,4/27 = 0,2(mol)
Gọi n Cl2 = a(mol) ; n O2 = b(mol)
Bảo toàn e :
2n Cl2 + 4n O2 = 2n Mg + 3n Al
<=> 2a + 4b = 0,15.2 + 0,2.3 = 0,9(1)
Bảo toàn khối lượng :
m X + m Al + m Mg = m Z
=> 71a + 32b = 29,95 - 3,6 -5,4 = 20,95(2)
Từ (1)(2) suy ra a = 0,25 ; b = 0,1
%m O2 = 0,1.32/(0,25.71 + 0,1.32) .100% = 15,27%
Đúng 3
Bình luận (0)
Hỗn hợp khí A gồm clo và oxi. A phản ứng hết với 1 hỗn hợp gồm 4,80 gam magiê và 8,10 gam nhôm tạo ra 37,05 gam hỗn hợp các muối clorua và oxit của 2 kim loại. Xác định thành phần phần trăm theo khối lượng và theo thể tích của hỗn hợp A?
Câu 6: 11,2 lít(đktc) hỗn hợp A gồm clo và oxi tác dụng vừa hết với 16,98g hỗn hợp B gồm magie và nhôm tạo ra 42,34g hỗn hợp clorua và oxi của hai kim loại
a: Tính thành phần phần trăm về thể tích của từng chất trong hỗn hợp A
b: Tính thành phần phần trăm về khối lượng của từng chất trong hỗn hợp B
a)
\(n_{hhA}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\ Đặt:n_{Cl_2}=a\left(mol\right);n_{O_2}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow a+b=0,5\left(1\right)\\ Mà:m_{hhA}=m_{muối}-m_{hhB}=42,34-16,98=25,36\left(g\right)\left(2\right)\\ \left(1\right),\left(2\right)\Rightarrow\left\{{}\begin{matrix}a+b=0,5\\71a+32b=25,36\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,24\\b=0,26\end{matrix}\right.\\ \Rightarrow\%V_{Cl_2}=\dfrac{0,24}{0,5}.100=48\%\Rightarrow \%V_{O_2}=\dfrac{0,26}{0,5}.100=52\%\)
b) Đặt x,y là số mol của Mg, Al trong hhB (x,y>0) (mol)
=> 24x+27y=16,98(3)
Áp dụng ĐLBT electron:
\(n_{e.cho}=n_{e.nhận}\\ \Leftrightarrow2.n_{Mg}+3.n_{Al}=2.n_{Cl_2}+4.n_{O_2}\\ \Leftrightarrow2x+3y=2.0,24+4.0,26=1,52\left(4\right)\\ \left(3\right),\left(4\right)\Rightarrow\left\{{}\begin{matrix}2x+3y=1,52\\24x+27y=16,98\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,55\\y=0,14\end{matrix}\right.\\ \Rightarrow\%m_{Mg}=\dfrac{0,55.24}{16,98}.100\approx77,739\%\\ \Rightarrow\%m_{Al}\approx22,261\%\)
Đúng 3
Bình luận (0)
a)\(n_{Cl_2}=x\left(mol\right),n_{O_2}=y\left(mol\right)\)
\(\Rightarrow x+y=\dfrac{11,2}{22,4}=0,5\left(1\right)\)
BTKL: \(m_A=m_{hh}-m_B=42,34-16,98=25,36g\)
\(\Rightarrow35,5\cdot2x+16\cdot2y=25,36\left(2\right)\)
Từ (1) và (2)\(\Rightarrow\left\{{}\begin{matrix}x=0,24\\y=0,26\end{matrix}\right.\)
\(\%V_{Cl_2}=\dfrac{0,24}{0,24+0,26}\cdot100\%=48\%\)
\(\%V_{O_2}=100\%-48\%=52\%\)
b)\(n_{Mg}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(\Rightarrow24a+27b=16,98\left(1\right)\)
BTe: \(2n_{Mg}+3n_{Al}=2n_{Cl_2}+4n_{O_2}\)
\(\Rightarrow2x+3y=2\cdot0,24+4\cdot0,26=1,52\left(2\right)\)
Từ (1) và (2)\(\Rightarrow\left\{{}\begin{matrix}a=0,55\\b=0,14\end{matrix}\right.\)
\(\%m_{Mg}=\dfrac{0,55\cdot24}{16,98}\cdot100\%=77,74\%\)
\(\%m_{Al}=100\%-77,74\%=22,26\%\)
Đúng 0
Bình luận (0)
Câu 6: 11,2 lít(đktc) hỗn hợp A gồm clo và canxi tác dụng vừa hết với 16,98g hỗn hợp B gồm magie và nhôm tạo ra 42,34g hỗn hợp clorua và oxi của hai kim loại
a: Tính thành phần phần trăm về thể tích của từng chất trong hỗn hợp A
b: Tính thành phần phần trăm về khối lượng của từng chất trong hỗn hợp B
hh A là khí gồm Clo và Canxi
Mà canxi là kim loại mà em, nó không phải khí đâu
Đúng 0
Bình luận (0)
Canxi không tính bằng lít em ơi
Đúng 0
Bình luận (3)
Gọi \(n_{Cl_2}=x\left(mol\right),n_{Ca}=y\left(mol\right)\)
\(\Rightarrow x+y=\dfrac{11,2}{22,4}=0,5mol\left(1\right)\)
BTKL: \(m_A+m_B=m_{hh}\Rightarrow m_A=42,34-16,98=25,36g\)
\(\Rightarrow35,5\cdot2x+40y=25,36\left(2\right)\)
Từ (1) và (2)\(\Rightarrow\left\{{}\begin{matrix}x=0,17\\y=0,33\end{matrix}\right.\)
\(\%V_{Cl_2}=\dfrac{0,17}{0,17+0,33}\cdot100\%=34\%\)
\(\%V_{Ca}=100\%-34\%=56\%\)
Đúng 0
Bình luận (0)
Một hỗn hợp X gồm Cl2 và O2. X phản ứng vừa hết với 9,6 gam Mg và 16,2 gam Al tạo thành 74,1 gam hỗn hợp muối clorua và oxit. Thành phần phần trăm theo khối lượng của Cl2 trong X là A. 26,5% B. 55,56% C. 73,5% D. 44,44%
Đọc tiếp
Một hỗn hợp X gồm Cl2 và O2. X phản ứng vừa hết với 9,6 gam Mg và 16,2 gam Al tạo thành 74,1 gam hỗn hợp muối clorua và oxit. Thành phần phần trăm theo khối lượng của Cl2 trong X là
A. 26,5%
B. 55,56%
C. 73,5%
D. 44,44%