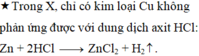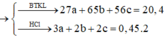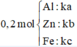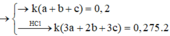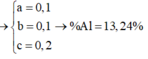Cho m gam hỗn hợp X gồm Al, Fe, Zn cùng số mol tác dụng với dung dịch HCl dư thu được dung dịch Y và V1 lít H2 (đktc). Mặt khác để oxi hóa m gam hỗn hợp X cần V lít Cl2 (đktc). Biết V1 – V2 = 2,016 lít. Cô cạn dung dịch Y thu được bao nhiêu gam muối khan?

Những câu hỏi liên quan
Cho 17,2 g hỗn hợp X gồm Al,Zn,Mg,Fe tác dụng với dung dịch Hcl dư thu V1 (lít) H2. Mặt khác để õi hóa hoàn toàn 17,2 g hỗn hợp X cần V2(lít) Cl2. Biết V2-V1=2,016.,các khí đều đo đktc.Tính phần trăm kl của Fe trong hỗn hợp X?
*Cho hỗn hợp tác dụng với HCl:
3nAl + 2nZn + 2nMg + 2nFe = 2* (V1/22,4) (1)
*Cho hỗn hợp tác dụng với Cl2:
3nAl + 2nZn + 2nMg + 3nFe = 2* (V2/22,4) (2)
(2) - (1) ta được nFe = 2* [(V2 - V1)/22,4] = 0,18 (mol)
%mFe/X = (0,18*56) / 17,2 = 58,60%
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Zn, Fe, Cu. Cho 18,5 gam hỗn hợp X tác dụng với dung dịch HCl dư thu được 4,48 lít H2 (đktc). Mặt khác cho 0,15 mol hỗn hợp X phản ứng vừa đủ với 3,92 lít khí Cl2 (đktc). Số mol Fe trong 18,5 gam hỗn hợp X là A. 0,1 mol B. 0,08 mol C. 0,12 mol D. 0,15 mol
Đọc tiếp
Hỗn hợp X gồm Zn, Fe, Cu. Cho 18,5 gam hỗn hợp X tác dụng với dung dịch HCl dư thu được 4,48 lít H2 (đktc). Mặt khác cho 0,15 mol hỗn hợp X phản ứng vừa đủ với 3,92 lít khí Cl2 (đktc). Số mol Fe trong 18,5 gam hỗn hợp X là
A. 0,1 mol
B. 0,08 mol
C. 0,12 mol
D. 0,15 mol
Hỗn hợp X gồm Zn, Fe, Cu. Cho 18,5 gam hỗn hợp X tác dụng với dung dịch HCl dư thu được 4,48 lit H2 (đktc). Mặt khác cho 0,15 mol hỗn hợp X phản ứng vừa đủ với 3,92 lít khí Cl2 (đktc). Số mol Fe có trong 18,5 gam hỗn hợp X là A. 0,12 mol B. 0,15 mol C. 0,1 mol D. 0,08 mol
Đọc tiếp
Hỗn hợp X gồm Zn, Fe, Cu. Cho 18,5 gam hỗn hợp X tác dụng với dung dịch HCl dư thu được 4,48 lit H2 (đktc). Mặt khác cho 0,15 mol hỗn hợp X phản ứng vừa đủ với 3,92 lít khí Cl2 (đktc). Số mol Fe có trong 18,5 gam hỗn hợp X là
A. 0,12 mol
B. 0,15 mol
C. 0,1 mol
D. 0,08 mol
Đáp án C
Đặt số mol mỗi kim loại trong 18,5 gam hỗn hợp lần lượt là a, b, c.
Ta có: mhh X =65a + 56b + 64c; n H 2 = a + b = 3 , 92 22 , 4 = 0 , 175 mol
Có số phân tử Cl2 phản ứng trung bình với hỗn hợp X:
n Cl 2 n X = 0 , 175 0 , 15 = 7 6 = ( a + 1 , 5 b + c ) ( a + b + c )
Từ đó ta có a - 2b + c = 0.
Tóm lại ta sẽ có a = b = c = 0,1 mol.
Vậy trong 18,5g hỗn họp X sẽ có 0,1 mol Fe
Chú ý:
Dung dịch axit như dung dịch HCl, HBr, HI hoặc dung dịch H2SO4 có khả năng phản ứng với các kim loại đứng trước H trong dãy điện hóa, tức là trong bài này phản ứng với Zn và Fe tạo ra ZnCl2 và FeCl2.
- Clo có khả năng phản ứng với hầu hết các kim loại (trừ Au, Pt) thậm chí còn có khả năng phản ứng với Ag ở điều kiên thích hợp và đưa kim loại lên số oxi hóa cao nhất vì vậy sản phẩm là ZnCl2,CuCl2,FeCl3
Đúng 0
Bình luận (0)
Cho 20,4 gam hỗn hợp A gồm Al, Zn và Fe tác dụng với dung dịch HCl dư, thu được 10,08 lít H2. Mặt khác 0,2 mol A tác dụng vừa đủ với 6,16 lít Cl2. Phần trăm của Al trong hỗn hợp A là (biết các khí đo ở đktc) A. 26,47%. B. 19,85%. C. 33,09%. D. 13,24%.
Đọc tiếp
Cho 20,4 gam hỗn hợp A gồm Al, Zn và Fe tác dụng với dung dịch HCl dư, thu được 10,08 lít H2. Mặt khác 0,2 mol A tác dụng vừa đủ với 6,16 lít Cl2. Phần trăm của Al trong hỗn hợp A là (biết các khí đo ở đktc)
A. 26,47%.
B. 19,85%.
C. 33,09%.
D. 13,24%.
Đáp án D
Xét trường hợp 20,4 gam A tác dụng với dung dịch HCl dư:
Gọi số mol các chất là Al: a mol; Zn: b mol; Fe: c mol
Ta có:

Các quá trình nhường, nhận electron:
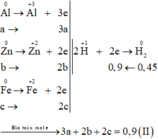
Xét trường hợp 0,2 mol A tác dụng với Cl2:
Gọi số mol các chất là Al: ka mol; Zn: kb mol; Fe: kc mol
Ta có:
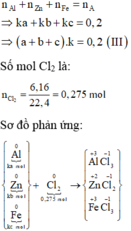
Các quá trình nhường, nhận electron:
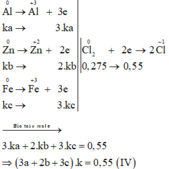
Lấy (IV) chia (III) vế với vế ta được:

Đúng 0
Bình luận (0)
Cho 20,4 gam hỗn hợp X gồm Fe, Zn, Al tác dụng với dung dịch H2SO4 dư thu được 10,08 lít H2 (đktc). Mặt khác cho 0,2 mol X tác dụng vừa đủ với 6,16 lít Cl2 (đktc). Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp X biết Fe + Cl2 ® FeCl3 Zn + Cl2 ® ZnCl2 Al + Cl2 ® AlCl3
Đọc tiếp
Cho 20,4 gam hỗn hợp X gồm Fe, Zn, Al tác dụng với dung dịch H2SO4 dư thu được 10,08 lít H2 (đktc). Mặt khác cho 0,2 mol X tác dụng vừa đủ với 6,16 lít Cl2 (đktc). Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp X biết
Fe + Cl2 ® FeCl3
Zn + Cl2 ® ZnCl2
Al + Cl2 ® AlCl3
Gọi $n_{Fe} = a(mol), n_{Zn} = b(mol) , n_{Al} = c(mol) \Rightarrow 56a + 65b + 27c = 20,4(1)$
$Fe + H_2SO_4 \to FeSO_4 + H_2$
$Zn + H_2SO_4 \to ZnSO_4 + H_2$
$2Al +3 H_2SO_4 \to Al_2(SO_4)_3 +3 H_2$
Theo PTHH : $n_{H_2} = a + b + 1,5c = \dfrac{10,08}{22,4} = 0,45(mol)(2)$
Mặt khác :
$2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
$Zn + Cl_2 \xrightarrow{t^o} ZnCl_2$
$2Al + 3Cl_2 \xrightarrow{t^o} 2AlCl_3$
Theo PTHH : $n_{Cl_2} = 1,5n_{Fe} + n_{Zn} + 1,5n_{Al}$
Suy ra : \dfrac{1,5a + b + 1,5c}{a + b + c} = \dfrac{0,275}{0,2}(3)$
Từ (1)(2)(3) suy ra : a = 0,2 ; b = 0,1 ; c = 0,1
$\%m_{Fe} = \dfrac{0,2.56}{20,4}.100\% = 54,9\%$
$\%m_{Zn} = \dfrac{0,1.65}{20,4}.100\% = 31,9\%$
$\%m_{Al} = 100\% - 54,9\% - 31,9\% = 13,2\%$
Đúng 2
Bình luận (0)
Cho 20,4 gam hỗn hợp A gồm Al, Zn và Fe tác dụng với dung dịch HCl dư, thu được 10,08 lít H2. Mặt khác 0,2 mol A tác dụng vừa đủ với 6,16 lít Cl2. Tính thành phần phần % về khối lượng của Al trong hỗn hợp A (biết khí đo được ở đktc) A.26,47% B. 19,85% C.33,09% D.13,24%
Đọc tiếp
Cho 20,4 gam hỗn hợp A gồm Al, Zn và Fe tác dụng với dung dịch HCl dư, thu được 10,08 lít H2. Mặt khác 0,2 mol A tác dụng vừa đủ với 6,16 lít Cl2. Tính thành phần phần % về khối lượng của Al trong hỗn hợp A (biết khí đo được ở đktc)
A.26,47%
B. 19,85%
C.33,09%
D.13,24%
Cho m gam hỗn hợp X gồm Fe, Al, Cr tác dụng hết với lượng dư khí Cl2, thu được (m + 31,95) gam muối. Mặt khác, cũng cho m gam X tan hết trong dung dịch HCl dư, thu được 7,84 lít khí H2 (đktc). Phần trăm số mol của Al trong X là A. 33,33% B. 75,00% C. 25,00% D. 66,67%.
Đọc tiếp
Cho m gam hỗn hợp X gồm Fe, Al, Cr tác dụng hết với lượng dư khí Cl2, thu được (m + 31,95) gam muối. Mặt khác, cũng cho m gam X tan hết trong dung dịch HCl dư, thu được 7,84 lít khí H2 (đktc). Phần trăm số mol của Al trong X là
A. 33,33%
B. 75,00%
C. 25,00%
D. 66,67%.
Đáp án : A
X + Cl2 :
Bảo toàn khối lượng : mCl2 = mmuối – mKL = 31,95g
3nFe + 3nCr + 3nAl = 2nCl2 = 0,9 mol
X + HCl : 2nFe + 2nCr + 3nAl = 2nH2 = 0,7 mol
=> nAl = 0,1 mol ; nFe + nCr = 0,2 mol
=> %nAl = 33,33%
Đúng 0
Bình luận (0)
Hòa tan 32 gam X gồm Fe, Mg, Al, Zn bằng dung dịch HCl dư thu được 2,24 lít H2(đktc). Mặt khác 32 gam X tác dụng với Cl2 dư thì có 3,36 lít Cl2 đktc ) tham gia phản ứng. Tính phần trăm khối lượng Fe trong hỗn hợp X
Hỗn hợp X gồm Na và Al. Hoà tan m gam hỗn hợp X vào nước dư thu được V lít H2 (đktc) và còn a gam chất rắn không tan. Cho a gam chất rắn tác dụng với dung dịch HNO3 dư, thu được 6,272 lít NO (đktc) và dung dịch Y. Cô cạn dung dịch Y thu được 3,4m gam muối khan. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 2V lít H2 (đktc). Giá trị của V gần với A. 12,7 B. 11,9. C. 14,2 D. 15,4
Đọc tiếp
Hỗn hợp X gồm Na và Al. Hoà tan m gam hỗn hợp X vào nước dư thu được V lít H2 (đktc) và còn a gam chất rắn không tan. Cho a gam chất rắn tác dụng với dung dịch HNO3 dư, thu được 6,272 lít NO (đktc) và dung dịch Y. Cô cạn dung dịch Y thu được 3,4m gam muối khan. Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 2V lít H2 (đktc). Giá trị của V gần với
A. 12,7
B. 11,9.
C. 14,2
D. 15,4