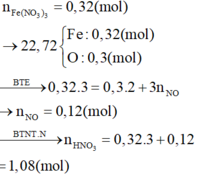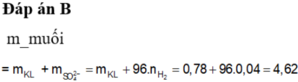Cho 10,08g kim loại R chưa biết hóa trị phản ứng với dung dịch HNO3 loãng dư sau phản ứng thu được dung dịch X và ko thấy khí thoát ra. Cô cạn X được 33,44g muối khan. Tìm R

Những câu hỏi liên quan
Cho 7,0 gam hỗn hợp hai muối cacbonat của kim loại hóa trị II tác dụng hết với dung dịch HCl thấy thoát ra V lít khí ở đktc. Cô cạn dung dịch sau phản ứng thu được 9,2 gam muối khan. Giá trị của V là:
A. 1,12 lít
B. 2,24 lít
C. 3,36 lít
D. 4,48 lít
Đáp án D
Đặt công thức của hai muối là RCO3: x mol
RCO3+ 2HCl → RCl2+ CO2+ H2O
x 2x x x mol
Theo định luật bảo toàn khối lượng:
mmuối cacbonat+ mHCl= m muối clorua+ mCO2+ mH2O
→ 7,0 + 2x. 36,5=9,2+ 44x+18x → x= 0,2 mol→ VCO2= 0,2.22,4= 4,48 lít
Đúng 1
Bình luận (0)
Cho 11,36 gam hỗn hợp gồm Fe, FeO,
Fe
2
O
3
và
Fe
3
O
4
phản ứng hết với dung dịch HNO3 loãng dư thu được 1,344 lít khí NO (sản phẩm khử duy nhất ở đktc) và dung dịch X. Cô cạn dung dịch X sau phản ứng được m gam muối khan. Giá trị m là A. 34,36 gam B. 35,50 gam C. 49,09 gam D. 38,72 gam
Đọc tiếp
Cho 11,36 gam hỗn hợp gồm Fe, FeO, Fe 2 O 3 và Fe 3 O 4 phản ứng hết với dung dịch HNO3 loãng dư thu được 1,344 lít khí NO (sản phẩm khử duy nhất ở đktc) và dung dịch X. Cô cạn dung dịch X sau phản ứng được m gam muối khan. Giá trị m là
A. 34,36 gam
B. 35,50 gam
C. 49,09 gam
D. 38,72 gam
Cho 34,8 gam hỗn hợp gồm Fe, FeO,
Fe
2
O
3
và
Fe
3
O
4
phản ứng hết với dung dịch
HNO
3
loãng dư thu được 1,12 lít khí NO (sản phẩm khử duy nhất ở đktc) và dung dịch X. Cô cạn dung dịch X sau phản ứng được m gam muối khan. Giá trị m là A. 54,45 gam B. 108,9 gam C. 49,09 gam D. 40,72 gam
Đọc tiếp
Cho 34,8 gam hỗn hợp gồm Fe, FeO, Fe 2 O 3 và Fe 3 O 4 phản ứng hết với dung dịch HNO 3 loãng dư thu được 1,12 lít khí NO (sản phẩm khử duy nhất ở đktc) và dung dịch X. Cô cạn dung dịch X sau phản ứng được m gam muối khan. Giá trị m là
A. 54,45 gam
B. 108,9 gam
C. 49,09 gam
D. 40,72 gam
hòa tan hoàn toàn 23.8 gam hỗn hợp một muối cacbonat của kim loại hóa trị 1 và một muối cacbonat của kim loại hóa trị 2 bằng dung dịch HCl thấy thoát ra 4,48l khí CO2. Cô cạn dung dịch thu được sau phản ứng thì khối lượng muối khan thu được là bao nhiêu?
giải gấp giúp mình với
23.8g MCO3+2HCL=>CO2 +MCL2 +H2O
nCO2=0.2mol
mMCL2=mM+mCL=23.8+0.2*2*35.5-0.2*44=29.2g
Đúng 0
Bình luận (0)
nCO2=4,48/22,4=0,2mol.
gọi muối 1 là A=)ct muối :A2CO3
------------2 là B=) ct muối :BCO3.
gọi mol muối 1 là x muối 2 là y
htan=hcl ta được:
A2CO3 + 2HCL==>2ACL+CO2+H2O
x => 2x => 2x => x =>x
BCO3 + 2HCL ==> BCL2 + CO2 + H2O
y => 2y => y => y => y
ta nhận thấy mol hỗn hợp 2 muối ban đầu bằng mol khí co2 thoát ra bằng mol h2o thu được.
mà mol co2 là 0,2 mol (1) => mol hỗn hợp muối cacbobat=0,2; mol h20=0,2mol.
có mol hcl = 2x+2y=2.(x+y)=2.0,2=0,4mol
theo ĐLBTKL ta có:
mhh+ mhcl= m muối mới( cần tìm)+m CO2 +m H2O
m muối mới= 23,8+ 0,4.36,5-0,2.44-0,2.18=26g
vậy kl muối là 26g . sai thì đừng ném gạch nhau
Đúng 0
Bình luận (2)
Cho kim loại X (hóa trị III) tác dụng với dung dịch HCl vừa đủ rồi cô cạn dung dịch sau phản ứng, thu được a gam muối khan. Nếu lấy cùng lượng X như trên cho tác dụng với dd H2SO4 loãng vừa đủ rồi cô cạn dung dịch, thì thu được b gam muối khan. Lập biểu thức tính số mol X theo a, b.
\(n_{XCl_3}=\dfrac{a}{M_X+106,5}\left(mol\right)\)
PTHH: 2X + 6HCl --> 2XCl3 + 3H2
=> \(n_X=\dfrac{a}{M_X+106,5}\left(mol\right)\)
\(n_{X_2\left(SO_4\right)_3}=\dfrac{b}{2.M_X+288}\left(mol\right)\)
PTHH: 2X + 3H2SO4 --> X2(SO4)3 + 3H2
=> \(n_X=\dfrac{b}{M_X+144}\left(mol\right)\)
Cho 22,72 gam hỗn hợp gồm Fe, FeO, Fe2O3 và Fe3O4 phản ứng hết với dung dịch HNO3 loãng dư thu được V lít khí NO(duy nhất ở đktc) và dung dịch X. Cô cạn dung dịch X thu được 77,44 gam muối khan. Số mol HNO3 phản ứng là: A. 0,96 B. 1,06 C. 1,08 D. 1,12
Đọc tiếp
Cho 22,72 gam hỗn hợp gồm Fe, FeO, Fe2O3 và Fe3O4 phản ứng hết với dung dịch HNO3 loãng dư thu được V lít khí NO(duy nhất ở đktc) và dung dịch X. Cô cạn dung dịch X thu được 77,44 gam muối khan. Số mol HNO3 phản ứng là:
A. 0,96
B. 1,06
C. 1,08
D. 1,12
Hòa tan 3,2 gam oxit của một kim loại hóa trị x bằng 200 gam dung dịch H2SO4 loãng. Khi thêm vào hỗn hợp sau phản ứng một lượng CaCO3 vừa đủ thấy thoát ra 0,224 dm3 CO2 (đktc), sau đó cô cạn dung dịch thu được 9,36 gam muối khan. Xác định oxit kim loại trên và nồng độ % H2SO4 đã dùng.
Gọi CT oxit : \(R_2O_x\)
Ta có \(n_{R_2O_x}=\dfrac{3,2}{2R+16x}\left(mol\right)\)
PTHH: \(R_2O_x+xH_2SO_4\rightarrow R_2\left(SO_4\right)_x+xH_2O\) (1)
\(\dfrac{3,2}{2R+16x}\)---->\(\dfrac{3,2}{2R+16x}.x\)-->\(\dfrac{3,2}{2R+16x}\) (mol)
\(H_2SO_{4\left(dư\right)}+CaCO_3\rightarrow CaSO_4+CO_2+H_2O\) (2)
\(n_{CO_2}=\dfrac{0,244}{22,4}=0,01\left(mol\right)\)
Theo PT (2) : \(n_{CO_2}=n_{CaSO_4}=n_{H_2SO_4dư}=0,01\left(mol\right)\)
Ta có : \(m_{muối}=\text{}\dfrac{3,2}{2R+16x}.\left(2R+96x\right)+0,01.136=9,36\left(g\right)\)
\(\dfrac{3,2}{2R+16x}\).(2R+96x)=8
Lập bảng :
| x | 1 | 2 | 3 |
| R | 18,67 | 37,33 | 56 |
| Kết luận | Loại | Loại | Chọn (Fe) |
=> Oxit là Fe2O3
\(\Sigma n_{H_2SO_4}=0,02.3+0,01=0,07\left(mol\right)\)
=> \(C\%_{H_2SO_4}=\dfrac{0,07.98}{200}.100=3,43\%\)
Đúng 1
Bình luận (0)
Hoà tan hoàn toàn 0,78 gam hỗn hợp kim loại Al, Mg bằng dung dịch H2SO4 loãng, thấy thoát ra 896 ml khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được bao nhiêu gam muối sunfat khan? A. 3,84 gam. B. 4,62 gam C. 46,2 gam D. 36,5 gam
Đọc tiếp
Hoà tan hoàn toàn 0,78 gam hỗn hợp kim loại Al, Mg bằng dung dịch H2SO4 loãng, thấy thoát ra 896 ml khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được bao nhiêu gam muối sunfat khan?
A. 3,84 gam.
B. 4,62 gam
C. 46,2 gam
D. 36,5 gam
Hòa tan hết 3,6 gam một kim loại M (có hóa trị II) trong dung dịch HCl dư, sau phản ứng thu được dung dịch X và V lít khí H2 (đktc). Cô cạn dung dịch X thu được 14,25 gam muối khan.
a. Tìm V và kim loại M.
b. Dẫn toàn bộ khí H2 thu được qua ống thủy tinh chứa 16 gam CuO nung nóng. Sau khi phản ứng xảy ra hoàn toàn thu được a gam chất rắn. Tính a.
Xem chi tiết
a) Ta có \(m_{muôi}=m_{KL}+m_{Cl^-}\\ \Leftrightarrow m_{Cl^-}=m_{muôi}-m_{KL}=14,25-3,6=10,65g\\ \Rightarrow n_{Cl^-}=\dfrac{10,65}{35,5}=0,3mol\)
Theo bảo toàn nguyên tố Cl: \(n_{HCl}=n_{Cl^-}=0,3mol\)
Theo bảo toàn nguyên tố H: \(n_{H_2}=\dfrac{1}{2}\cdot n_{HCl}=\dfrac{1}{2}\cdot0,3=0,15mol\\ \Rightarrow V=0,15\cdot22,4=3,36l\)
Ta có PTHH: \(M+2HCl\rightarrow MCl_2+H_2\uparrow\)
----------------0,15-------------------------0,15---(mol)
\(\Rightarrow M=\dfrac{3,6}{0,15}=24\)(g/mol) => M là Magie (Mg)
b) \(n_{CuO}=\dfrac{16}{80}=0,2mol\)
Ta có quá trình phản ứng:
\(CuO+H_2\rightarrow Cu+H_2O\)
-0,15---0,15-----0,15----------(mol)
\(\Rightarrow a=m_{CuO\left(dư\right)}+m_{Cu}=\left(16-0,15\cdot80\right)+64\cdot0,15=13,6g\)
Đúng 1
Bình luận (0)