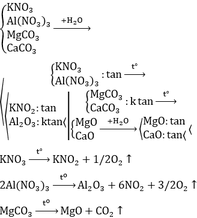Có 4 chất rắn màu tương tự nhau để riêng biệt đó là Na,Cao, P2O5, và MgO. Bằng pp hóa học có thể nhận ra chúng k nếu đc e hãy trình bày cách nhận biết chúng. Dụng cụ hóa chất, thuốc thử cần thiết có đ

Những câu hỏi liên quan
có 4 chất rắn màu trắng chứa trong 4 lọ riêng biệt:CaO,P2O5,Al2O3,MgO. Hãy trình bày phương trình hóa học , nhận biết 4 chất rắn trên
Trích mỗi chất một ít ra ống nghiệm làm thuốc thử :
Cho nước lần lượt vào từng mẫu thử :
- Tan , tỏa nhiều nhiệt : CaO
- Tan : P2O5
- Không tan : Al2O3 , MgO
Cho dung dịch NaOH lần lượt vào 2 chất còn lại :
- Tan : Al2O3
- Không tan : MgO
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
\(2NaOH+Al_2O_3\rightarrow2NaAlO_2+H_2O\)
Đúng 2
Bình luận (0)
Cho quỳ tím ẩm vào :
- mẫu thử hóa xanh là CaO
$CaO + H_2O \to Ca(OH)_2$
- mẫu thử hóa đỏ là P2O5
$P_2O_5 + 3H_2O \to 2H_3PO_4$
Cho hai mẫu thử còn dd NaOH
- mẫu thử tan là Al2O3
$Al_2O_3 + 2NaOH \to 2NaAlO_2 + H_2O$
- mẫu thử không tan là MgO
Đúng 2
Bình luận (0)
- Trích mẫu thử.
- Cho nước tác dụng với lần lượt từng mẫu thử:
+ Tan: CaO, P2O5
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\\ P_2O_5+3H_2O\rightarrow2H_3PO_4\)
CaO tan ít trong nước, dd vẩn đục. Phân biệt được 2 lọ đựng P2O5 và CaO
+ Không tan: Al2O3, MgO
- Cho sản phẩm thu được Ca(OH)2 tác dụng vào 2 mẫu thử còn lại:
+ Tan: Al2O3
\(Al_2O_3+Ca\left(OH\right)_2\rightarrow Ca\left(AlO_2\right)_2+H_2O\)
+ Không tác dụng: MgO
Phân biệt được 4 chất rắn.
Đúng 0
Bình luận (0)
Ch: có bốn chất rắn màu tương tự nhau đó là Na, CaO, P2O5, MgO. Bằng phương pháp hóa học có thể nhận ra chúng không nếu được e hãy cách nhận biết chúng. Dụng cụ, hóa chất, thuốc thử cần thiết có đủ?
các cậu giúp tớ với ạ
cảm ơn các c nhiều
tớ cần gấp lắm ạ
-Cho nước vào
+Tan có khí là Na
2Na+2H2O-->2NaOH+H2
+Tan là CaO,P2O5
CaO+H2O-->Ca(OH)2
P2O5+3H2O--->2H3PO4
+ko tan là MgO
-Cho quỳ tím vào 2 dd Ca(OH)2 và H3PO4
+Làm quỳ tím hóa xanh là Ca(OH)2----> Nhận biết dc là CaOs dc P2O5
+Làm quỳ tím hóa đỏ là H3PO4-->NHận biêt
https://i.imgur.com/HQvi8XB.jpg
chỉ dùng một hóa chất (ko dùng các chát đã nhận biết đc làm thuốc thử),hãy trình bày phương pháp hóa học để nhận biết các dd riêng biệt sau:HCl,H2SO4,NaNO3,Na2CO3.Nêu hiện tượng và viết phương trình phản ứng (nếu có)
Trích mẫu thử
Cho $Ba(HCO_3)_2$ vào các mẫu thử
- mẫu thử nào tạo khí không màu là HCl
$Ba(HCO_3)_2 + 2HCl \to BaCl_2 + 2CO_2 + 2H_2O$
- mẫu thử nào tạo khí không màu và kết tủa trắng là $H_2SO_4$
$Ba(HCO_3)_2 + H_2SO_4 \to BaSO_4 + 2CO_2 + 2H_2O$
- mẫu thử tạo kết tủa trắng là Na2CO3
$Na_2CO_3 + Ba(HCO_3)_2 \to BaCO_3 + 2NaHCO_3$
- mẫu thử không hiện tượng là NaNO3
Đúng 2
Bình luận (0)
Hãy trình bày phương pháp hóa học nhận biết các chất đựng riêng biệt trong các lọ mất nhãn:
a) Chất rắn: MgO, CaO, P2O5.
bằng pp hóa học hãy nhận biết các dd và các chất rắn sau:
1/ba chất rắn màu trắng là CaO, P2O5 và Na2O
2/ba chất rắn màu trắng là CaO, K2O và MgO
Tham khảo
a) Trích mỗi chất một ít làm mẫu thử, lần lượt cho vào nước:
+ Chất không tan là MgOMgO
+ Chất ta tan là Na2O,CaONa2O,CaO và P2O5P2O5
PTHH:
Na2O+H2O→2NaOHNa2O+H2O→2NaOH
CaO+H2O→Ca(OH)2CaO+H2O→Ca(OH)2
P2O5+3H2O→2H3PO4P2O5+3H2O→2H3PO4
Cho quỳ tím vào dung dịch thu được
+ Chất làm quỳ tím hóa đỏ là H3PO4H3PO4 → chất ban đầu là P2O5P2O5
+ Chất làm quỳ tím hóa xanh là NaOHNaOH và Ca(OH)2Ca(OH)2.
Sục khí CO2CO2 qua 22 dung dịch làm quỳ tím hóa xanh:
+ Dung dịch có kết tủa trắng là Ca(OH)2Ca(OH)2 → chất ban đầu là CaOCaO:
Ca(OH)2+CO2→CaCO3+H2OCa(OH)2+CO2→CaCO3+H2O
+ Dung dịch không có hiện tượng là NaOHNaOH → chất ban đầu là Na2ONa2O:
2NaOH+CO2→Na2CO3+H2O2NaOH+CO2→Na2CO3+H2O
b) Trích mẫu thử, đánh STT
Cho vài giọt dd HCl vào 33 ống đựng 33 mẫu thử. Ống nào thoát khí thì ống đó đựng CaCO3CaCO3:
CaCO3+2HCl→CaCl2+H2O+CO2CaCO3+2HCl→CaCl2+H2O+CO2
Cho vài giọt nước vào 22 mẫu còn lại. Ống nào sinh ra chất mới, toả nhiều nhiệt thì ống đó đựng CaOCaO
CaO+H2O→Ca(OH)2CaO+H2O→Ca(OH)2 (p/ứ toả nhiều nhiệt)
- Ống còn lại đựng Ca(OH)2Ca(OH)2
Đúng 0
Bình luận (0)
Bằng phương pháp hóa học hãy nhận biết các chất rắn riêng biệt sau: Na, Na2O ,BaO, P2o5,MgO, NaCl
Thả vào nước và cho thử QT:
- Tan, QT chuyển xanh -> Na2O, BaO (1)
Na2O + H2O ---> 2NaOH
BaO + H2O ---> Ba(OH)2
- Tan, QT ko đổi màu -> NaCl
- Tan, QT chuyển đỏ -> P2O5
P2O5 + 3H2O ---> 2H3PO4
Cho các chất (1) t/d vs dd H2SO4
- Có kết tủa màu trắng -> BaO
BaO + H2SO4 ---> BaSO4 + H2O
- Có t/d nhưng ko hiện tượng -> Na2O
Đúng 4
Bình luận (2)
Có 4 chất rắn Ba , K2O , P2O5 , Fe đựng trong 4 lọ riêng biệt . Hãy trình phương pháp hóa học nhận biết mỗi chất và viết phương trình hóa học xảy ra
Trích mẫu thử
Cho giấy quỳ tím ẩm vào mẫu thử
- mẫu thử nào hoá đỏ là $P_2O_5$
$P_2O_5 + 3H_2O \to 2H_3PO_4$
- mẫu thử nào hoá xanh là $Ba,K_2O$
$Ba + 2H_2O \to Ba(OH)_2 + H_2$
$K_2O + H_2O \to 2KOH$
- mẫu thử nào không đổi màu là $Fe$
Cho dung dịch $H_2SO_4$ vào hai mẫu thử :
- mẫu thử nào tạo khí và kết tủa trắng là $Ba$
$Ba + H_2SO_4 \to BaSO_4 + H_2$
- mẫu thử không hiện tượng gì là $K_2O$
Đúng 2
Bình luận (0)
cho nc vào từng mẫu thử tan trong nc la Ba,p2O5,K2O
ko tan Fe
cho quỳ tím tac dụng với từng mẫu thử tan trong nc
-làm quỳ tím hoá xanh là Ba(OH)2 chất bđ là Ba và KOH chất bđ là K2O
-làm quỳ tím hoá đỏ là H3PO4 bđ là P2O5
ta có PTHH
Ba+H2O-Ba(OH)2+H2O
K2O+H2O-KOH
P2O5+H2O-H3PO4
còn lại Ba và K2O
cho Al2O3 vào dd KOH và Ba(OH)2
tan là KOH
ko tan là Ba(OH)2
Al2O3 + 2KOH -H2O + 2KAlO2
Đúng 0
Bình luận (0)
Chỉ được dùng thêm nước và các thiết bị cần thiết (lò nung, đèn cồn…). Hãy trình bày cách phân biệt 4 chất bột màu trắng (tương tự nhau) đựng riêng biệt trong 4 lọ mất nhãn: KNO3, Al(NO3)3, MgCO3, CaCO3. Viết phương trình hóa học của các phản ứng xảy ra (ghi rõ điều kiện nếu có).
Bằng phương pháp hóa học, làm thế nào có thể nhận ra các chất rắn sau đựng trong các loại riêng biệt bị mất nhãn : CaO,p2o5, K2O ,MgO