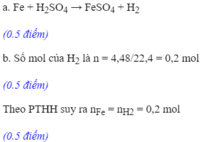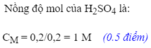Cho một lượng sắt dư vào 500 ml dung dịch axit sunfuric , sau khi phản ứng thu được 3,36 lít khí hiđrô ( đktc ).
a,Tính nồng độ mol của dung dịch axit đã dùng và tính khối lượng sắt tham gia phản ứng?
Viết cả CTHH hộ mình nhé!Thank!

Những câu hỏi liên quan
Cho một lượng bột kẽm dư vào 50 ml dung dịch axit sunfuric loãng, sau khi phản ứng thu được 3,36 lít khí hiđrô ( đktc )
a, Viết PTHH xảy ra?
b, Tính khối lượng kẽm đã tham gia phản ứng?
c, Tính nồng độ mol / lít của dung dịch axit đã dùng?
d, Tính khối lượng muối thu được sau phản ứng?
zn+ h2so4-> znso4+ h2
nh2=3,36/22,4=0,15
nzn= nh2=0,15mol
-> mzn=0,15*65=9,75g
nh2so4=nh2=0,15
cM h2so4=0,15/0,05=3M
nznso4=nh2=0,15
mznso4=0,15*161=24,15g
Đúng 0
Bình luận (0)
Cho một lượng bột sắt dư vào 200ml dung dịch axit H 2 S O 4 . Phản ứng xong thu được 4,48 lít khí hiđrô (đktc)
a. Viết phương trình phản ứng hoá học
b. Tính khối lượng sắt đã tham gia phản ứng
c. Tính nồng độ mol của dung dịch axit H 2 S O 4 đã dùng
Cho một lượng bột kẽm dư vào 50 ml dung dịch axit sunfuric loãng, sau phản ứng thu được 3,36 lít khí hiđro (đktc).
a. Viết PTHH xảy ra?
b. Tính khối lượng kẽm đã tham gia phản ứng?
c. Tính nồng độ mol/lít của dung dịch axit đã dùng?
d. Tính khối lượng muối thu được sau phản ứng?
a, PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2SO_4}=n_{ZnCl_2}=n_{H_2}=0,15\left(mol\right)\)
b, mZn = 0,15.65 = 9,75 (g)
c, CM (H2SO4) = 0,15/0,05 = 3 M
d, mZnSO4 = 0,15.161 = 24,15 (g)
Bạn tham khảo nhé!
Đúng 4
Bình luận (0)
Cho một lượng bột sắt dư vào 50 ml dung dịch axit sunfuric. Phản ứng xong, thu được 3,36 lít khí hiđro (đktc). Tính khối lượng sắt đã tham gia phản ứng.
Tìm số mol Fe tham gia phản ứng :
n Fe = n H = 0,15 mol, suy ra m Fe = 8,4 gam.
Đúng 0
Bình luận (0)
Cho một lượng bột sắt dư vào 50 ml dung dịch axit sunfuric. Phản ứng xong, thu được 3,36 lít khí hiđro (đktc). Tính nồng độ moi của dung dịch axit sunfuric đã dùng.
Tìm số mol H2SO4 có trong dung dịch :
n H 2 SO 4 = n H 2 = 0,15 mol, tính ra C M H 2 SO 4 = 3M.
Đúng 0
Bình luận (0)
: Cho một khối lượng mạt sắt dư vào 50 ml dung dịch HCl. Phản ứng xong, thu được 3,36 lít khí (đktc).
a. Tính khối lượng mạt sắt đã tham gia phản ứng.
b. Tìm nồng độ mol của dung dịch HCl đã dùng.
a) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
____0,15<--0,3<-------------0,15
=> mFe = 0,15.56 = 8,4 (g)
b) \(C_{M\left(ddHCl\right)}=\dfrac{0,3}{0,05}=6M\)
Đúng 2
Bình luận (0)
Cho một lượng bột kẽm dư vào 50ml dung dịch axit sunfuric loãng, sau phản ứng thu được 3,36 lít khí hidro( đktc)
a)Viết PTHH xảy ra?
b) tính khối lượng kẽm đã tham gia phản ứng?
c)tính nồng độ mol/lít của dung dịch axit đã dùng?
d)tính khối lượng muối thu được sau phản ứng?
a) PTHH: Zn + H2SO4 -> ZnSO4 + H2
nH2= 0,15(mol)
=> nZn=nH2SO4=nZnSO4=nH2=0,15(mol)
b) mZn=0,15.65=9,75(g)
c) CMddH2SO4= 0,15/ 0,05=3(M)
d) mZnSO4= 161. 0,15=24,15(g)
Đúng 2
Bình luận (1)
Cho một khối lượng mạt sắt dư vào 50 ml dung dịch HCl .Phản ứng xong thu được 3,36 lít khí (đktc) . Viết phương trình hóa học .Tính khối lượng mạt sắt đã tham gia phản ứng Tính nồng độ mol của dung dịch HCl đã dùng .
Giải giúp mik với ạ
\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,15 0,3 0,15
b) \(n_{Fe}=\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
⇒ \(m_{Fe}=0,15.56=8,4\left(g\right)\)
c) \(n_{HCl}=\dfrac{0,15.2}{1}=0,3\left(mol\right)\)
50ml = 0,05l
\(C_{M_{ddHCl}}=\dfrac{0,3}{0,05}=6\left(M\right)\)
Chúc bạn học tốt
Đúng 4
Bình luận (0)
Cho 1 khối lượng mạt sắt dư vào 200ml dung dịch H2SO4 loãng.phản ứng xong thu được 3,36 lít khí (đktc) a. Tính khối lượng math sắt đã tham gia phản ứng. b. Tính nồng độ mol của dung dịch H2SO4 đã dùng. c. Tính nồng độ của dung dịch thu được sau phản ứng.
\(Fe+H_2SO_4 \to FeSO_4+H_2\\ n_{H_2}=0,15(mol)\\ a/\\ n_{Fe}=n_{H_2}=0,15(mol)\\ m_{Fe}=0,15.56=8,4(g)\\ b/\\ n_{H_2SO_4}=n_{H_2}=0,15(mol)\\ CM_{H_2SO_4}=\dfrac{0,15}{2}=0,75M c/\\ n_{FeSO_4}=n_{H_2}=0,15(mol)\\ CM_{FeSO_4}=\dfrac{0,15}{0,2}=0,75M\\\)
Đúng 1
Bình luận (0)
Cho một lượng bột sắt dư vào 50ml dd axit sunfuric. Phản ứng xong thu được 3,36 lít khí H2 (đkc).
a. Tính khối lượng sắt đã tham gia phản ứng.
b. Tính nồng độ mol của dd axit sunfuric đã dùng.
c. Tính nồng độ mol của dd thu được sau phản ứng (thể tích dd thay đổi không đáng kể)
a)
$Fe + H_2SO_4 \to FeSO_4 + H_2$
Theo PTHH :
$n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)$
$m_{Fe} = 0,15.56 = 8,4(gam)$
b)
$n_{H_2SO_4} = n_{H_2} = 0,15(mol)$
$C_{M_{H_2SO_4}} = \dfrac{0,15}{0,05} = 3M$
c)
$n_{FeSO_4} = n_{H_2} = 0,15(mol)$
$C_{M_{FeSO_4}} = \dfrac{0,15}{0,05} = 3M$
Đúng 1
Bình luận (1)