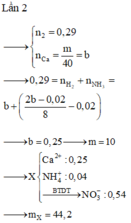tính khối lượng Al2S3 tạo thành khi trộn 5,4g Al vs 12g S rồi đun nóng để phản ứng xảy ra hoàn toàn,bt sau phản ứng tạo ra1 sản phẩm duy nhất

Những câu hỏi liên quan
Tính khối lượng Al2O3 tạo thành khi trộn 5,4 g Al vớ 12g S đun nóng để phản ứng xảy ra hoàn toàn, biết sau phản ứng tạo ra một sản phẩm duy nhất
a. nAl = 5,4 : 27 = 0,2 (mol)
nS = 12 : 32 = 0,375 (mol)
2Al + 3S → Al2S3
2mol 3mol 1mol
0,2mol 0,375mol ?
Có tỉ lệ : (0,2 / 2 ) < ( 0,375/ 3) nên S thừa sau phản ứng. Vậy Al2S3 được tính theo Al
Số mol Al2S3: 0,2 x1 :2 = 0,1(mol)
Vậy khối lượng Al2S3 tạo thành là : 0,1 x 150 = 15 (g)
Đúng 0
Bình luận (0)
2Al + 3S \(\underrightarrow{t^o}\)Al 2S3
nAl = 0,2 mol
nS = 0,375 mol
Đặt tỉ lệ ta có
\(\dfrac{0,2}{2}\) < \(\dfrac{0,375}{3}\)
\(\Rightarrow\) S dư
\(\Rightarrow\) mAl2S3 = 0,1.150 = 15 (g)
Đúng 0
Bình luận (0)
nAl = \(\dfrac{5,4}{27}\) = 0,2 mol
nS = \(\dfrac{12}{32}\) = 0,375 mol
2Al + 3S -> Al2S3
0,2(hết);0,375(dư)->0,1
=>mAl2S3 = 0,1 . 150 = 15 g
Đúng 0
Bình luận (0)
a,Tính khối lượng Al2S3 tạo thành khi trộn 5,4g Al với 12g S rồi đun nóng để phản ứng xảy ra hoàn toàn, biết sau khi phản ứng tạo ra một sản phẩn duy nhất.
b,Có một hỗn hợp khí gồm 15g NO và 2,2g Hidro
-Tính khối lượng của 1 mol hỗn hợp khí trên.
-Hỗn hợp khí trên nặng hay nhẹ hơn khí Metan (CH4) bao nhiêu lần
Cho 5,4g Al vào dung dịch CuCl2. biết phản ứng xảy ra hoàn toàn a.Tính khối lượng kim loại mới được tạo ra b.Tính khối lượng muối mới tạo ra thành có trong dung dịch sau phản ứng Cho biết : Al=27,Cu=64,Cl=35.5
\(2Al+3CuCl_2\rightarrow2AlCl_3+3Cu\\ n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\\ TheoPTHH:n_{AlCl_3}=n_{Al}=0,2\left(mol\right);n_{Cu}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.0,2=0,3\left(mol\right)\\ a,m_{Cu}=0,3.64=19,2\left(g\right)\\ b,m_{AlCl_3}=133,5.0,2=26,7\left(g\right)\)
Đúng 2
Bình luận (0)
Đun nóng 27 gam glucozơ với
AgNO
3
/
NH
3
dư, đun nóng. Lọc lấy Ag rồi cho vào dung dịch
HNO
3
đặc nóng, dư thì sau phản ứng thu được khí
NO
2
(sản phẩm khử duy nhất) và khối lượng dung dịch axit tăng a gam. Giả sử các phản ứng xảy ra hoàn toàn. Giá trị của a là A. 18,6 B. 32,4. C. 16,2. D. 9,3.
Đọc tiếp
Đun nóng 27 gam glucozơ với AgNO 3 / NH 3 dư, đun nóng. Lọc lấy Ag rồi cho vào dung dịch HNO 3 đặc nóng, dư thì sau phản ứng thu được khí NO 2 (sản phẩm khử duy nhất) và khối lượng dung dịch axit tăng a gam. Giả sử các phản ứng xảy ra hoàn toàn. Giá trị của a là
A. 18,6
B. 32,4.
C. 16,2.
D. 9,3.
Cho m gam Ca tan hoàn toàn trong dung dịch HNO3, thu được dung dịch X và 0,672 lít khí (ở đktc, phản ứng chỉ tạo một sản phẩm khử duy nhất của N+5). Sau khi các phản ứng xảy ra hoàn toàn cho tiếp m gam Ca vào dung dịch X (đun nóng nhẹ), thì thấy 6,496 khí (đktc) thoát ra. Khối lượng chất tan có trong dung dịch X là? A. 38,4 B. 44,2 C. 23,4 D. 22,8
Đọc tiếp
Cho m gam Ca tan hoàn toàn trong dung dịch HNO3, thu được dung dịch X và 0,672 lít khí (ở đktc, phản ứng chỉ tạo một sản phẩm khử duy nhất của N+5). Sau khi các phản ứng xảy ra hoàn toàn cho tiếp m gam Ca vào dung dịch X (đun nóng nhẹ), thì thấy 6,496 khí (đktc) thoát ra. Khối lượng chất tan có trong dung dịch X là?
A. 38,4
B. 44,2
C. 23,4
D. 22,8
Cho m gam Ca tan hoàn toàn trong dung dịch HNO3, thu được dung dịch X và 0,672 lít khí (ở đktc, phản ứng chỉ tạo một sản phẩm khử duy nhất của N+5). Sau khi các phản ứng xảy ra hoàn toàn cho tiếp m gam Ca vào dung dịch X (đun nóng nhẹ), thì thấy 6,496 khí (đktc) thoát ra. Khối lượng chất tan có trong dung dịch X là? A. 38,4. B. 44,2. C. 23,4. D. 22,8.
Đọc tiếp
Cho m gam Ca tan hoàn toàn trong dung dịch HNO3, thu được dung dịch X và 0,672 lít khí (ở đktc, phản ứng chỉ tạo một sản phẩm khử duy nhất của N+5). Sau khi các phản ứng xảy ra hoàn toàn cho tiếp m gam Ca vào dung dịch X (đun nóng nhẹ), thì thấy 6,496 khí (đktc) thoát ra. Khối lượng chất tan có trong dung dịch X là?
A. 38,4.
B. 44,2.
C. 23,4.
D. 22,8.
Đáp án B
Định hướng tư duy giải
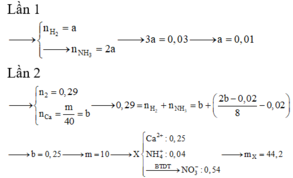
Nhận thấy, nếu Z chỉ là H2 sẽ vô lý ngay vì
không có sản phẩm khử nào thỏa mãn.
→ Khí thoát ra ở cả hai lần phải là hỗn hợp khí NH3 và H2.
Đúng 0
Bình luận (0)
Cho m gam Ca tan hoàn toàn trong dung dịch HNO3, thu được dung dịch X và 0,672 lít khí (ở đktc, phản ứng chỉ tạo một sản phẩm khử duy nhất của N+5). Sau khi các phản ứng xảy ra hoàn toàn cho tiếp m gam Ca vào dung dịch X (đun nóng nhẹ), thì thấy 6,496 khí (đktc) thoát ra. Khối lượng chất tan có trong dung dịch X là? A. 38,4 B. 44,2 C. 23,4 D. 22,8
Đọc tiếp
Cho m gam Ca tan hoàn toàn trong dung dịch HNO3, thu được dung dịch X và 0,672 lít khí (ở đktc, phản ứng chỉ tạo một sản phẩm khử duy nhất của N+5). Sau khi các phản ứng xảy ra hoàn toàn cho tiếp m gam Ca vào dung dịch X (đun nóng nhẹ), thì thấy 6,496 khí (đktc) thoát ra. Khối lượng chất tan có trong dung dịch X là?
A. 38,4
B. 44,2
C. 23,4
D. 22,8
Chọn đáp án B
Nhận thấy, nếu Z chỉ là H2 sẽ vô lý ngay vì không có sản phẩm khử nào thỏa mãn.
→ Khí thoát ra ở cả hai lần phải là hỗn hợp khí NH3 và H2.
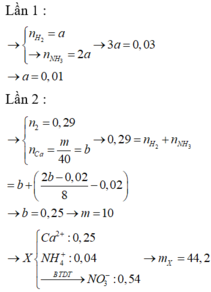
| GIẢI THÍCH THÊM + Lần đầu có hỗn hợp khí NH3 và H2 nên lần đầu NH4+ vẫn còn dư do đó với a mol H2 →2a mol OH →2a mol NH3. + Phương trình áp dụng ở lần 2 là BTE và 2 b - 0 , 02 8 là tổng số mol NH4+. |
Đúng 0
Bình luận (0)
Bài 2: Cho 10 g CaCO3 vào một bình kín rồi đun nóng tới khi phản ứng xảy ra hoàn toàn thì thu được CaO và CO2. a. Tìm thể tích khí CO2 ở đktc b. Tính khối lượng CaO tạo thành sau phản ứng
nCaCO3=10/100=0,1 mol
CaCO3 →CaO + CO2 (đk to)
0,1 0,1 0,1 mol
VCO2=0,1.22,4=2,24 l
mCaO=0,1.56=5,6 g
Đúng 0
Bình luận (0)
a, PTHH: CaCO3---> CaO+ CO2
Ta có nCaCO3=10/100=0,1mol
theo PTHH ta có nCO2=nCaCO3=0,1mol
=> VCO2=0,1.22,4=2,24 lít
b, Theo PTHH ta có : nCaO= nCaCO3=0,1mol
=> mCaO=0,1.56=5,6g
Đúng 3
Bình luận (0)
Cho 5,4g Là phản ứng hoàn toàn với dung dịch HCl,phản ứng hoá học xảy ra theo sơ đồ Al+HCl-->AlCl+H2 a)lập pthh của phản ứng trên b) tính thể tích khí H2 thu được ở đktc c)tính khối lượng muối AlCl3 tạo thành sau phản ứng
a, \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
b, \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
c, \(n_{AlCl_3}=n_{Al}=0,2\left(mol\right)\Rightarrow m_{AlCl_3}=0,2.133,5=26,7\left(g\right)\)
Đúng 1
Bình luận (0)