Cho a gam hỗn hợp gồm Al2O3,MgO, ZnO tác dụng vừa đủ với 0,6mol H2SO4 và tạo thành 74,3g hỗn hợp muối. Tính a?

Những câu hỏi liên quan
Cho 1,405 gam hỗn hợp Fe2O3, ZnO, MgO tác dụng vừa đủ với 250 ml dung dịch H2SO4 0,1M. Khối lượng muối tạo thành trong dung dịch là bao nhiêu?
\(n_{H_2SO_4}=0.1\cdot0.25=0.025\left(mol\right)\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\)
\(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(TừPTHH:\)
\(n_{H_2SO_4}=n_{H_2O}=0.025\left(mol\right)\)
\(BTKL:\)
\(m_{Muối}=1.405+0.025\cdot98-0.025\cdot18=3.405\left(g\right)\)
Đúng 2
Bình luận (0)
Chia 77,2 gam hỗn hợp X gồm MgO, Fe3O4, Al2O3,CuO thành hai phần bằng nhau.
Phần 1: tác dụng hết với dung dịch HCl dư được 78,2 gam muối khan.
Phần 2: tác dụng vừa đủ với dung dịch Y là hỗn hợp HCl, H2SO4 loãng thu được 88,7 gam muối khan
Tính số mol của H2SO4 trong dung dịch Y ?
Ta có:
m hh phần 1 = m hh phần 2 = 38,6 ( g )
Phần 1
Gọi n HCL phản ứng = a ( mol )
=> n H2O = 0,5a ( mol )
BTKL: 38,6 + 36,5a = 78,2 + 9a
=> a = 1,44 ( mol ) => n O ( hh phần 1 ) = 0,72 ( mol )
=> m O ( hh phần 1 ) = 11,52 ( g ) => m KL ( hh phần 1 ) = 27,08 ( g )
Phần 2
Quy hh phần 2 về: RO
PTHH
RO + 2HCl ===> RCL2 + H2O ( 1 )
RO + H2SO4 ===> RSO4 + H2O ( 2)
Gọi n RO ( 1 ) = x ( mol ) ; n RO ( 2 ) = y ( mol )
CÓ: m gốc CL + m gốc SO4 = 88,7 - 27,08 = 61,62 ( g )
Ta có hpt
\(\left\{{}\begin{matrix}x+y=0,72\\2x\times35,5+96y=61,62\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,3\\y=0,42\end{matrix}\right.\)
Có: y = 0,42 ( mol ) = > n H2SO4 = 0,42 ( mol )
Đúng 1
Bình luận (0)
cho 1.405 gam hỗn hợp gồm fe2o3,zno,mgo tác dụng vừa đủ với 500ml dung dịch hcl 0.1M. Khối lượng muối tạo ra của dung dịch
\(Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2O\\ ZnO + 2HCl \to ZnCl_2 + H_2O\\ MgO + 2HCl \to MgCl_2 + H_2O\\ n_{HCl} = 0,5.0,1 = 0,05(mol)\\ n_{H_2O} = \dfrac{1}{2}n_{HCl} = 0,025(mol)\\ \text{Bảo toàn khối lượng : }\\ m_{muối} = m_{hỗn\ hợp} + m_{HCl} - m_{H_2O} = 1,405 + 0,05.36,5 - 0,025.18 = 2,78(gam)\)
Đúng 2
Bình luận (1)
Cho 2,81 gam hỗn hợp A gồm 3 oxit Fe2O3, MgO, ZnO tan vừa đủ trong 300 ml dung dịch H2SO4 0,1M thì khối lượng hỗn hợp các muối sunfat khan tạo ra là
A. 5,21 gam.
B. 4,81 gam.
C. 4,8 gam.
D. 3,81gam.
Cho 2,64 gam hỗn hợp gồm ZnO và Al2O3 tác dụng vừa đủ với 61,25 gam dung dịch H2SO4
8%. Tính %m các oxit trong hỗn hợp ban đầu.
\(n_{H_2SO_4}=\dfrac{61,25.8}{100.98}=0,05mol\\ ZnO+H_2SO_4\rightarrow ZnSO_4+H_2\\ Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\\ \Rightarrow\left\{{}\begin{matrix}81n_{ZnO}+102n_{Al_2O_3}=2,64\\n_{ZnO}+3n_{Al_2O_3}=0,05\end{matrix}\right.\\ \Rightarrow n_{ZnO}=0,02mol;n_{Al_2O_3}=0,01mol\\ \%m_{ZnO}=\dfrac{81.0,02}{2,64}\cdot100=61,36\%\\ \%m_{Al_2O_3}=100-61,36=38,64\%\)
Đúng 2
Bình luận (0)
Cho 2,81 g hỗn hợp Fe2O3, ZnO, MgO tác dụng vừa đủ với 500 ml dung dịch H2SO4 0,1M. Tính khối lượng muối sunfat tạo ra trong dung dịch?
Tham khảo :
Oxit + H2SO4 = muối + H2O
Áp dụng định luật bảo toàn nguyên tố H
=> nH2O = nH2SO4 = 0,5.0,1 = 0,05 mol
Áp dụng định luật bảo toàn khối lượng ta có:
=> m(oxit) + mH2SO4 = m(muối) + mH2O
=> m(muối)= 2,81 + 0,05.98 - 0.05.18 = 6,81g
Đúng 1
Bình luận (0)
Cho 38,3 gam hỗn hợp gồm 4 oxit kim loại Fe2O3, MgO, ZnO, Al2O3 tan vừa đủ trong 800ml dung dịch H2SO4 1M. Cô cạn dung dịch thì thu được a gam muối khan. Giá trị của a là A. 68,1. B. 86,2. C. 102,3. D. 90,3.
Đọc tiếp
Cho 38,3 gam hỗn hợp gồm 4 oxit kim loại Fe2O3, MgO, ZnO, Al2O3 tan vừa đủ trong 800ml dung dịch H2SO4 1M. Cô cạn dung dịch thì thu được a gam muối khan. Giá trị của a là
A. 68,1.
B. 86,2.
C. 102,3.
D. 90,3.
Đáp án C
Số mol H2SO4 là: n H 2 S O 4 = 0 , 8 m o l
Đặt M2On là oxit chung cho Fe2O3, MgO, ZnO và Al2O3
Sơ đồ phản ứng :
![]()
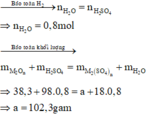
Đúng 0
Bình luận (0)
Cho x gam hỗn hợp gồm MgO,
F
e
2
O
3
, ZnO, CuO tác dụng vừa đủ với 50g dd
H
2
S
O
4
11,76%. Cô cạn dd sau phản ứng thu được 8,41 g muối khan. Giá trị của m là: A. 3,2g B. 3,5g C. 3,61g D. 4,2g
Đọc tiếp
Cho x gam hỗn hợp gồm MgO, F e 2 O 3 , ZnO, CuO tác dụng vừa đủ với 50g dd H 2 S O 4 11,76%. Cô cạn dd sau phản ứng thu được 8,41 g muối khan. Giá trị của m là:
A. 3,2g
B. 3,5g
C. 3,61g
D. 4,2g
Tương tự bài 1, ta có:
m 4 o x i t = m m u o i - m H 2 S O 4 + m H 2 O s a n p h a m
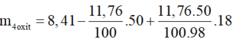
m 4 o x i t = 3,61g
⇒ Chọn C.
Đúng 0
Bình luận (0)
Cho 2,81 gam hỗn hợp gồm 3 oxit Fe2O3, MgO, ZnO tan vừa đủ trong 300 mL dung dịch H2SO4 0,1M thì khối lượng hỗn hợp các muối sunfat khan tạo ra là A. 3,81 g. B. 4,81 g. C. 5,21 g. D. 4,86 g
Đọc tiếp
Cho 2,81 gam hỗn hợp gồm 3 oxit Fe2O3, MgO, ZnO tan vừa đủ trong 300 mL dung dịch H2SO4 0,1M thì khối lượng hỗn hợp các muối sunfat khan tạo ra là
A. 3,81 g.
B. 4,81 g.
C. 5,21 g.
D. 4,86 g
Áp dụng phương pháp tăng giảm khối lượng.
Cứ 1 mol H2SO4 phản ứng, để thay thế O (trong oxit) bằng S O 4 2 - trong các kim loại, khối lượng tăng 96 - 16 = 80 g. Theo đề số mol H2SO4 phản ứng là 0,03 thì khối lượng tăng 0,24 g.
Vậy khối lượng muối khan thu được là: 2,81 + 2,4 = 5,21
Đáp án C
Đúng 0
Bình luận (0)
















