Trộn 100ml dung dịch NaOH 0,01M với 200ml dung dịch HCl 0,01M. Tính pH của dung dịch thu được sau phản ứng

Những câu hỏi liên quan
Trộn 100ml dung dịch axit HCl 0,01M với 200ml dung dịch NaOH 0,5M thu được dung dịch A sau phản ứng.Viết phương trình phân tử và ion rút gọn của phản ứng và tính pH của dung dịch sau phản ứng.
a)
$NaOH + HCl \to NaCl + H_2O$
$OH^- + H^+ \to H_2O$
b)
$n_{HCl} = 0,1.0,01 = 0,001(mol)$
$n_{NaOH} = 0,2.0,5= 0,1(mol)$
$\Rightarrow$ NaOH dư, HCl hết
$n_{NaOH\ pư} = 0,001 \Rightarrow n_{NaOH\ dư} = 0,1 - 0,001 = 0,099(mol)$
$\Rightarrow [OH^-] = \dfrac{0,099}{0,1 + 0,2} = 0,33M$
$\Rightarrow pOH = -log(0,33) = 0,48 $
$pH = 14 - pOH = 14 - 0,48 = 13,52$
Đúng 3
Bình luận (0)
Trộn 200ml dung dịch H2SO4 0,01M vào 100ml dung dịch NaOH 0,01M. Tính pH của dung dịch X sau phản ứng
\(n_{H^+}=0.2\cdot0.01\cdot2=0.004\left(mol\right)\)
\(n_{OH^-}=0.1\cdot0.01=0.001\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(0.001.....0.001\)
\(n_{H^+\left(dư\right)}=0.004-0.001=0.003\left(mol\right)\)
\(pH=-log\left(H^+\right)=-log\left(\dfrac{0.003}{0.2+0.1}\right)=2\)
Đúng 0
Bình luận (0)
Có: \(n_{H^+}=2n_{H_2SO_4}=2.0,2.0,01=0,004\left(mol\right)\)
\(n_{OH^-}=0,1.0,01=0,001\left(mol\right)\)
PT ion: \(H^++OH^-\rightarrow H_2O\)
____0,004___0,001 (mol)
\(\Rightarrow n_{H^+\left(dư\right)}=0,003\left(mol\right)\)\\(\Rightarrow\left[H^+\right]=\dfrac{0,003}{0,3}=0,01\)
\(\Rightarrow pH=2\)
Bạn tham khảo nhé!
Đúng 0
Bình luận (0)
Tính pH:
a) thêm 90ml H2O vào 10ml dunh dịch HCl cos pH=2. thu được 100ml dung dịch HCl có pH bằng bao nhiêu?
b) trộn 100ml dung dịch HCl có pH=2 với 100ml dung dịch HCl có pH=3 thu được 200ml dung dịch HCl có pH bằng bao nhiêu?
c) trộn 300ml dung dịch NaOH 0,01M với 200ml dung dịch HCl 0,01M thu được dung dịch có pH bằng bao nhiêu ?
a. nHCl = 10-2. 0,01 = 10-4 mol
=> Nồng độ H+ sau pha = 10-4: (0,09 + 0,01) = 10-3 => pH dd sau pha = 3
b. nồng độ H+ sau pha = [(10-2. 0,1) + (10-3. 0,1)] : 0,2 = 0,0055M
=> pH dd sau pha = -lg(0,0055) = 2,26
c. nOH- = 0,3. 0,01 = 0,003. nH+ = 0,2. 0,01 = 0,002
=> OH- dư = 0,003 - 0,002 = 0,001 => nồng độ OH- = 0,001: (0,3+0,2) = 0,002M => pOH = -lg0,002 = 2,7 => pH = 14 - 2,7 = 11,3
Đúng 0
Bình luận (0)
Trộn 100ml NaOH 0,01M với 150ml dd Ba(OH)2 0,01M . Tính pH của dung dịch sau khi trộn
$n_{NaOH} = 0,001(mol)$
$n_{Ba(OH)_2} = 0,01.0,15 = 0,0015(mol)$
$NaOH \to Na^+ + OH^-$
$Ba(OH)_2 \to Ba^{2+} + 2OH^-$
Ta có :
$n_{OH^-}= 0,001 + 0,0015.2 = 0,004(mol)$
$V_{dd} = 0,1 + 0,15 = 0,25(mol)$
$[OH^-] = \dfrac{0,004}{0,25} = 0,016M$
$pOH = -log(0,016) = 1,795 \Rightarrow pH = 14 - 1,795 = 12,205$
Đúng 3
Bình luận (1)
\(n_{OH^-}=0,1.0,01+0,15.0,01.2=0,004\left(mol\right)\\ V_{ddsau}=100+150=250\left(ml\right)=0,25\left(l\right)\\ \Rightarrow\left[OH^-\right]=\dfrac{0,004}{0,25}=0,016\left(M\right)\\ pH=14+log\left[0,016\right]\approx12,204\)
Đúng 1
Bình luận (0)
Trộn 250ml dung dịch hỗn hợp gồm H2SO4 0,005M và HCl 0,01M với 200ml dung dịch hỗn hợp gồm NaOH 0,001M và Ba(OH)2 0,0005M thu được dung dịch X. Dung dịch X có pH là:
A. 12,3
B. 1,18
C. 11,87
D. 2,13
Đáp án D
nH2SO4 = 0,005 .0,25 =0,00125(mol)
nHCl = 0,01. 0,25= 0,0025 (mol)
∑n= 0,00125 + 0,0025= 0,00375 (mol)
∑n= 0,001.0,2 + 0,0005.2.0,2=0,0004
H+ + OH- → H2O
Ban đầu: 0,00375 0,0004
Phản ứng: 0,0004 0,0004
Sau phản ứng: 0,00335 0
Vsau = 0,2 + 0,25= 0,45(lít)
Mà 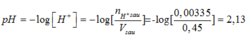
Đúng 0
Bình luận (0)
Trộn 100 ml dung dịch KOH có pH = 10 với 100ml dung dịch H2SO4 bằng 0,01m tính pH của dung dịch thu được
\(pH=10\)
\(\Rightarrow\left[H^+\right]=10^{-10}\)
\(\Rightarrow\left[OH^-\right]=10^{-4}\)
\(n_{OH^-}=10^{-4}.0,1=10^{-5}\left(mol\right)\)
\(n_{H^+}=0,1.2.0,01=0,003\left(mol\right)\)
\(\Rightarrow n_{H^+dư}=2,99.10^{-3}\left(mol\right)\)
\(\Rightarrow\left[H^+_{dư}\right]=\dfrac{2,99.10^{-3}}{0,2}=0,01495M\)
\(\Rightarrow pH\approx1,83\)
Đúng 0
Bình luận (0)
Mọi người giải giúp mk đc ko ạCâu 1: Trộn lẫn V ml dung dịch NaOH 0,01M với V ml dung dịch HCl 0,03M, thu được 2V ml dung dịch Y. Dung dịch Y có pH bằngCâu 2: Khi trộn những thể tích bằng nhau của dung dịch HNO3 0,01M và dung dịch NaOH 0,03M thì thu được dung dịch có giá trị pH bằng Câu 3: Trộn 100 ml dung dịch gồm Ba(OH)2 0,1M và NaOH 0,1M với 400 ml dung dịch gồm H2SO4 0,0375M và HCl 0,0125M thu được dung dịch X. Giá trị pH của dung dịch X làCâu 4: Hòa tan m gam Na vào nước được 100 ml dung...
Đọc tiếp
Mọi người giải giúp mk đc ko ạ
Câu 1: Trộn lẫn V ml dung dịch NaOH 0,01M với V ml dung dịch HCl 0,03M, thu được 2V ml dung dịch Y. Dung dịch Y có pH bằng
Câu 2: Khi trộn những thể tích bằng nhau của dung dịch HNO3 0,01M và dung dịch NaOH 0,03M thì thu được dung dịch có giá trị pH bằng
Câu 3: Trộn 100 ml dung dịch gồm Ba(OH)2 0,1M và NaOH 0,1M với 400 ml dung dịch gồm H2SO4 0,0375M và HCl 0,0125M thu được dung dịch X. Giá trị pH của dung dịch X là
Câu 4: Hòa tan m gam Na vào nước được 100 ml dung dịch có pH = 13. Giá trị của m bằng
Câu 5: Để trung hoà 100 gam dung dịch HCl 1,825% cần bao nhiêu ml dung dịch Ba(OH)2 có pH bằng 13?
Câu 6: Trộn 200 ml dung dịch hỗn hợp gồm HNO3 0,3M và HClO4 0,5M với 200 ml dung dịch Ba(OH)2 aM, thu được dung dịch có pH = 3. Vậy a có giá trị là
Câu 7: Trộn 100 ml dung dịch có pH=1 gồm HCl và HNO3 với 100 ml dung dịch NaOH nồng độ a (mol/l), thu được 200 ml dung dịch có pH=12. Giá trị của a
Câu 8: Trộn 250 ml dung dịch chứa hỗn hợp HCl 0,08M và H2SO4 0,01M với 250 ml dung dịch NaOH aM thu được 500 ml dung dịch có pH = 12. Giá trị a là
Câu 9: Trộn 3 dung dịch H2SO4 0,1M, HCl 0,2M và HNO3 0,3M với thể tích bằng nhau, thu được dung dịch X. Cho 300 ml dung dịch X tác dụng với V lít dung dịch Y chứa NaOH 0,2M và Ba(OH)2 0,1M được dung dịch Z có pH = 1. Giá trị của V là
Câu 10: Trộn 100ml dd H2SO4 0,01M với 400ml dd Ba(OH)2 nồng độ a mol/l thu được m gam kết tủa và dd còn lại có pH=12. Giá trị của m và a là
Câu 11: Trộn 300ml dd HCl 0,05M với 200ml dd Ba(OH)2 nồng độ a mol/l thu được 500ml dd có pH=x. Cô cạn dd sau phản ứng thu được 1,9875 gam chất rắn. Giá trị của a và x lần lượt là
Câu 12: Trộn 150 ml dd HCl nồng độ a mol/l với 250 ml dd hỗn hợp gồm NaOH 0,5M và Ba(OH)2 0,1M thu được dd có pH=12. Giá trị của a là
Câu 13: Trộn 250 ml dd hỗn hợp gồm HCl 0,08M và H2SO4 0,01M với 250 ml dd NaOH nồng độ b mol/l được 500 ml dd có pH=12. Giá trị của b là
Câu 14: Trộn 250 ml dd hỗn hợp gồm HCl 0,08M và H2SO4 0,01M với 250 ml dd Ba(OH)2 nồng độ x mol/l thu được m gam kết tủa và 500 ml dd có pH=12 . Giá trị của m và x tương ứng là
Câu 1: nOH-=0,01V(mol) nH+ =0,03V(mol)
nOH-<nH+ nên axit dư -->nH+dư =0,02V(mol)--->CM H+=0,01(M)=10-2->pH=2
Chú thích do thể tích như nhau nên ko cần đổi
Câu 2:nOH-=0,03a(mol) nH+=0,01a(mol)-->OH-dư
noh-dư=0,02a(mol) mà v=2a-->Cm oh-=0,01=10-2(M)->pH=12
Câu 3:nOH-=0,03 nH+=0,035->H+dư nH+dư=0,005 mol
V=0,5(l) CmH+=10^-2 pH=2
Đúng 0
Bình luận (0)
Trộn 100ml dung dịch HCl 0,05M với 100ml dung dịch NaOH 0,07M. Tính pH của dung
dịch thu được sau phản ứng?
\(H^++OH^-\rightarrow H_2O\\ n_{H^+}=0,05\left(mol\right);n_{OH^-}=0,07\left(mol\right)\\ Lậptỉlệ:\dfrac{0,05}{1}< \dfrac{0,07}{1}\\ \Rightarrow OH^-dư\\ \left[OH^-_{dư}\right]=\dfrac{0,07-0,05}{0,2}=0,1M\\ \Rightarrow pOH=-log\left(0,1\right)=1\\ \Rightarrow pH=14-1=13\)
Đúng 1
Bình luận (0)





















