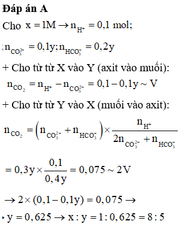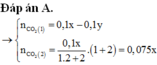BT về nhà. Cho x(g) Na2CO3 pứ đủ V(ml) ddHCl 2,5M ddA nồng độ y(M) + 4,48 lít khí B (đktc). a.tính x, V, y. b.Cho khí B hấp thụ hết vào 200g ddKOH 4,62%. Tính khối lượng muối tạo thành.

Những câu hỏi liên quan
Cho x(g) Na2CO3 pứ đủ V(ml) ddHCl 2,5M ddA nồng độ y(M) + 4,48 lít khí B (đktc). a.tính x, V, y. b.Cho khí B hấp thụ hết vào 200g ddKOH 4,62%. Tính khối lượng muối tạo thành
a, VddHCl=0,42,5=0,16(l)VddHCl=0,42,5=0,16(l)
Đúng 0
Bình luận (0)
Cho x(g) Na2CO3 pứ đủ V(ml) ddHCl 2,5M ddA nồng độ y(M) + 4,48 lít khí B (đktc). a.tính x, V, y. b.Cho khí B hấp thụ hết vào 200g ddKOH 4,62%. Tính khối lượng muối tạo thành. Mọi người giải cả a và b giúp mình nha
a, \(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
Mol: 0,2 0,4 0,4 0,2
\(m_{Na_2CO_3}=0,2.106=21,2\left(g\right)\)
\(V_{ddHCl}=\dfrac{0,4}{2,5}=0,16\left(l\right)=160\left(ml\right)\)
\(C_{M_{ddNaCl}}=\dfrac{0,4}{0,16}=2,5M\)
b, \(m_{KOH}=200.4,62\%=9,24\left(g\right)\Rightarrow n_{KOH}=\dfrac{9,24}{56}=0,165\left(mol\right)\)
PTHH: 2KOH + CO2 → K2CO3 + H2O
Mol: 0,165 0,0825
Ta có: \(\dfrac{0,2}{1}>\dfrac{0,165}{2}\) ⇒ KOH dư, CO2 hết
\(m_{K_2CO_3}=0,0825.138=11,385\left(g\right)\)
Đúng 0
Bình luận (0)
Cho a(g) Fe tan vừa đủ vào V(ml) ddHCl 3M → dd muối x(M) + 33,6 lít khí (đktc). Tính giá trị a, V, x.
Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\)
Pt : Fe + 2HCl → FeCl2 + H2\(|\)
1 2 1 1
1,5 3 1,5 1,5
Số mol của sắt
nFe = \(\dfrac{1,5.1}{1}=1,5\left(mol\right)\)
Khối lượng của sắt
mFe = nFe . MFe
= 1,5 . 56
= 84 (g)
Số mol của dung dịch axit clohidric
nHCl = \(\dfrac{1,5.2}{1}=3\left(mol\right)\)
Thể tích của dung dịch axit clohidric
CMHCl = \(\dfrac{n}{V}\Rightarrow V=\dfrac{n}{C_M}=\dfrac{3}{3}=1\left(l\right)\)
Số mol của muối sắt (II) clorua
nFeCl2 = \(\dfrac{1,5.1}{1}=1,5\left(mol\right)\)
Khối lượng của muối sắt (II) clorua
mFeCl2 = nFeCl2 . MFeCl2
= 1,5 .127
= 190,5 (g)
Chúc bạn học tốt
Đúng 0
Bình luận (0)
Cho a(g) Fe tan vừa đủ vào V(ml) ddHCl 3M → dd muối x(M) + 33,6 lít khí (đktc). Tính giá trị a, V, x.
Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\)
Pt : Fe + 2HCl → FeCl2 + H2\(|\)
1 2 1 1
1,5 3 1,5 1,5
Số mol của sắt
nFe = \(\dfrac{1,5.1}{1}=1,5\left(mol\right)\)
Khối lượng của sắt
mFe = nFe . MFe
= 1,5 . 56
= 84 (g)
Số mol của dung dịch axit clohidric
nHCl = \(\dfrac{1,5.2}{1}=3\left(mol\right)\)
Thể tích của dung dịch axit clohidric
CMHCl = \(\dfrac{n}{V}\Rightarrow V=\dfrac{n}{C_M}=\dfrac{3}{3}=1\left(l\right)\)
Số mol của muối sắt (II) clorua
nFeCl2 = \(\dfrac{1,5.1}{1}=1,5\left(mol\right)\)
Nồng độ mol của muối sắt (II) clorua
CMFeCl2 = \(\dfrac{n}{V}=\dfrac{1,5}{1}=1,5\left(M\right)\)
Chúc bạn học tốt
Đúng 0
Bình luận (0)
cho 8,4g sắt vào 200g đ H2SO4 dư thu đc m g muối và V lít khí hidro đktc
a tính m g muối và V lít khí đktc.
b. tính C% của đ axit ban đầu.
c, tính C% của các chất trong đ thu đc sau pứ.
d. cho muối thu đc tác dụng vs đ BaCl2 dư. tính khối lượng kết tủa tạo thành
nFe = 0,15 (mol)
Fe + H2SO4 \(\rightarrow\) FeSO4 + H2 \(\uparrow\)
0,15 \(\rightarrow\) 0,15 \(\rightarrow\) 0,15 \(\rightarrow\) 0,15 (mol)
a) mmuối = 0,15 . 152 = 22,8 (g)
VH2 = 0,15 . 22,4 = 3,36 (l)
b) Chỉ tính đc C% của axit pư thôi, đề ko cho gì thêm nên ko tính đc C% của axit ban đầu (vì dd axit dùng dư)
C%(H2SO4) = \(\frac{0,15.98}{200}\) . 100% = 7,35%
c) C%(FeSO4) = \(\frac{0,15.152}{8,4+200}\) . 100% = 10,94%
d) FeSO4 + BaCl2 \(\rightarrow\) BaSO4 \(\downarrow\) + FeCl2
0,15 \(\rightarrow\) 0,15 (mol)
mBaSO4 = 0,15 . 233 = 34,95 (g)
Đúng 0
Bình luận (2)
Fe td với H2SO4 đặc, nóng đâu có tạo khí H2
Đúng 0
Bình luận (0)
Hòa tan hết 4,68 g hỗn họp 2 muối ACO3 và BCO3 bằng dung dịch H2SO4 loangx , sau phản ứng thu được 1 dung dịch X và 1,12 lít CO2 ở đktc .a.Tính tổng khôi lượng các muối tạo thành trong dung dịch X.b.Tìm các kim loại A,B và tính thành phần phần trăm theo khối lượng của muối trong hỗn hợp đầu, biết nACO:nBCO32:3, MA:MB3:5.c. Cho toàn bộ lượng khí CO2 thu được ở trên hấp thụ vào 200 ml dung dịch Ba(OH)2. Tính nồng độ mol của dung dịch Ba(OH)2 để thu được 1,97 g kết tủa
Đọc tiếp
Hòa tan hết 4,68 g hỗn họp 2 muối ACO3 và BCO3 bằng dung dịch H2SO4 loangx , sau phản ứng thu được 1 dung dịch X và 1,12 lít CO2 ở đktc .
a.Tính tổng khôi lượng các muối tạo thành trong dung dịch X.
b.Tìm các kim loại A,B và tính thành phần phần trăm theo khối lượng của muối trong hỗn hợp đầu, biết nACO:nBCO3=2:3, MA:MB=3:5.
c. Cho toàn bộ lượng khí CO2 thu được ở trên hấp thụ vào 200 ml dung dịch Ba(OH)2. Tính nồng độ mol của dung dịch Ba(OH)2 để thu được 1,97 g kết tủa
a)
Do A và B đều là kim loại hóa trị II nên ta sử dụng phương pháp trung bình coi A và B là một chất gọi là X
=> CT chung của 2 muối là XCO3
Ta có nCO2 = \(\dfrac{1,12}{22,4}\) = 0,05 ( mol )
XCO3 + H2SO4 → XSO4 + H2O + CO2
0,05 <---- 0,05 <---0,05 <-- 0,05 < -0,05
bảo toàn khối lượng ta có
mXSO4 = mXCO3 + mH2SO4 - mH2O - mCO2
= 4,68 + ( 98 . 0,05 ) - ( 18 . 0,05 ) - ( 44 . 0,05 )
= 6,48 ( gam )
Đúng 0
Bình luận (0)
b) MXCO3 = mXCO3 : nXCO3 = 4,68 : 0,05 = 93,6
=> X = 93,6 - 12 - 16 . 3 = 33,6
có nACO3 : nBCO3 = 2 : 3
và nACO3 + nBCO3 = 0,05
=> nACO3 = 0,02 và nBCO3 = 0,03
=> nA = 0,02 và nB = 0,03
=> ( 0,02 . A + 5 : 3 . 0,03 . B) / 0,05 = 33,6
=> A = 24 ( là magie - Mg ) do B = A . 5 :3
=> B = 40 ( là canxi - Ca )
=> mMgCO3 = 1,68 ( gam )
=> %mMgCO3 = \(\dfrac{1,68}{4,68}\) . 100 \(\approx\) 36 %
=> %mCaCO3 = 100 - 36 = 64%
Đúng 1
Bình luận (0)
c) nCO2 = 0,05 ( mol )
Do tạo kết tủa nên có 2 trường hợp
=> tạo 2 muối : trung hòa và axit
2CO2 + Ba(OH)2 -------> Ba(HCO3)2
0,04 --> 0,02
CO2 + Ba(OH)2 --------> BaCO3 + H2O
0,01 <--- 0,01 <------- 0,01
=> nBa(OH)2 = 0,03
=> CM = n : V = 0,03 : 0,2 = 0,15 M
Đúng 0
Bình luận (0)
X là dung dịch HCl nồng độ x mol/l. V là dung dịch gồm Na2CO3 nồng độ y mol/l và NaHCO3 nồng độ 2y mol/l. Nhỏ từ từ đến hết 100 ml X vào 100 ml Y, thu được V lít khí CO2 (đktc). Nhỏ từ từ đến hết 100 ml Y vào 100 ml X, thu được 2V lít khí CO2 (đktc). Tỉ lệ x : y bằng A. 8 : 5 B. 6 : 5 C. 4 : 3 D. 3 : 2
Đọc tiếp
X là dung dịch HCl nồng độ x mol/l. V là dung dịch gồm Na2CO3 nồng độ y mol/l và NaHCO3 nồng độ 2y mol/l. Nhỏ từ từ đến hết 100 ml X vào 100 ml Y, thu được V lít khí CO2 (đktc). Nhỏ từ từ đến hết 100 ml Y vào 100 ml X, thu được 2V lít khí CO2 (đktc). Tỉ lệ x : y bằng
A. 8 : 5
B. 6 : 5
C. 4 : 3
D. 3 : 2
Cho 4,48 lít CO2 (đktc) hấp thụ hết trong 400 ml dd NaOH thu được dd X chứa nồng độ của muối Na2CO3 0,1M ( coi thể tích dung dịch không bị thay đổi khi hấp thụ). Tính nồng độ CM của dd NaOH?
$n_{CO_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$n_{Na_2CO_3} = 0,4.0,1 = 0,04(mol)$
Bảo toàn Cacbon : $n_{NaHCO_3} = 0,2 - 0,04 = 0,16(mol)$
Bảo toàn Natri :$n_{NaOH} = 0,16 + 0,04.2 = 0,24(mol)$
$C_{M_{NaOH}} = \dfrac{0,24}{0,4} = 0,6M$
Đúng 1
Bình luận (0)
\(n_{Na_2CO_3}=0.1\cdot0.4=0.04\left(mol\right)\)
\(n_{CO_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
\(0.08...........0.04.............0.04\)
\(NaOH+CO_2\rightarrow NaHCO_3\)
\(0.16......0.2-0.04\)
\(n_{NaOH}=0.08+0.16=0.24\left(mol\right)\)
\(C_{M_{NaOH}}=\dfrac{0.24}{0.4}=0.6\left(M\right)\)
Đúng 1
Bình luận (0)
X là dung dịch HCl nồng độ x mol/l. Y là dung dịch gồm Na2CO3 nồng độ y mol/l và NaHCO3 nồng độ 2y mol/l. Nhỏ từ từ đến hết 100 ml X vào 100 ml Y, thu được V lít khí CO2 (đktc). Nhỏ từ từ đến hết 100 ml Y vào 100 ml X, thu được 2V lít khí CO2 (đktc). Tỉ lệ x : y bằng
A. 8:5.
B. 6:5.
C. 4:3.
D. 3:2.