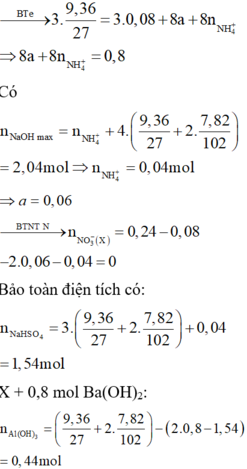cho 200ml dung dịchHCl 2M tác dụng với 300ml dung dịch NaOH.Sau phản ứng thu được dung dịch A.Cho Al2O3 vào dung dịch A thì thấy có 1,02g Al2O3 bị hòa tan.Tính CM dung dịch NaOH ban đầu

Những câu hỏi liên quan
Trộn 500ml dung dịch NaOH nồng độ xM với 500ml dung dịch H2SO4 nồng độ yM thu được dung dịch E. Dung dịch E có khả năng hòa tan hết 1,02g Al2O3. Mặt khác cho dung dịch E phản ứng với dung dịch BaCl2 dư thu được 23,3g kết tủa trắng. Xác định giá trị x,y
nH2SO4 = nBaSO4 = 0,1
-> y = 0,2 (mol/l)
nAl2O3 = 0,01
TH1: Axit dư:
H2SO4 + 2NaOH —> Na2SO4 + 2H2O
0,25x 0,5x
3H2SO4 + Al2O3 —> Al2(SO4)3 + 3H2O
0,03 0,01
-> nH2SO4 = 0,25x + 0,03 = 0,1
-> x = 0,28 (mol/l)
TH2: NaOH dư:
H2SO4 + 2NaOH —> Na2SO4 + 2H2O
0,1 0,2
Al2O3 + 2NaOH —> 2NaAlO2 + H2O
0,01 0,02
-> nNaOH tổng = 0,5x = 0,22
-> x = 0,44 (mol/l)
Vậy \(\left[{}\begin{matrix}x=0,28\\x=0,44\end{matrix}\right.\)(mol/l)
y = 0,2 (mol/l)
Đúng 3
Bình luận (1)
Cho 300ml dung dịch NaOh 1M tác dụng với 200ml dung dịch HCl a( mol/l) sau phản ứng thu được dung dịch X.Dung dịch X có thể hòa tan tối đa 1,02 gam Al2O3. Tính giá trị a.
Hòa tan hoàn toàn 6,12 gam Al2O3 trong 200ml dung dịch HCl 2M thu được dung dịch A. Tính thể tích dung dịch NaOH 2M cần thêm vào dung dịch A để thu được 7,8 gam kết tủa.
Giúp mình vs mình cần gấp. Thanks mn <3
PTHH: \(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\) (1)
\(HCl+NaOH\rightarrow NaCl+H_2O\) (2)
\(AlCl_3+3NaOH\rightarrow3NaCl+Al\left(OH\right)_3\downarrow\) (3)
Ta có: \(\left\{{}\begin{matrix}n_{Al_2O_3}=\dfrac{6,12}{102}=0,06\left(mol\right)\\\Sigma n_{HCl}=0,2\cdot2=0,4\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,06}{1}< \dfrac{0,4}{6}\) \(\Rightarrow\) HCl còn dư, Al2O3 p/ứ hết
Vì bazơ mạnh sẽ p/ứ với axit mạnh trước nên sẽ xảy ra p/ứ (2) và (3)
Lại có: \(n_{Al\left(OH\right)_3}=\dfrac{7,8}{78}=0,1\left(mol\right)=n_{AlCl_3\left(3\right)}\)
Theo PTHH (1): \(n_{AlCl_3\left(1\right)}=0,12\left(mol\right)\)
\(\Rightarrow\) AlCl3 còn dư nên tính theo Al(OH)3 \(\Rightarrow n_{NaOH\left(3\right)}=0,3\left(mol\right)\)
Mặt khác: \(n_{HCl\left(dư\right)}=n_{HCl\left(2\right)}=0,04\left(mol\right)=n_{NaOH\left(2\right)}\)
\(\Rightarrow\Sigma n_{NaOH}=0,34\left(mol\right)\) \(\Rightarrow V_{NaOH}=\dfrac{0,34}{2}=0,17\left(l\right)=170\left(ml\right)\)
Đúng 2
Bình luận (1)
Hòa tan hết hỗn hợp gồm 9,36 gam Al và 7,82 gam Al2O3 trong dung dịch chứa NaHSO4 và 0,24 mol HNO3. Sau khi kết thúc phản ứng thu được dung dịch X chỉ chứa các muối trung hòa và hỗn hợp khí Y gồm 0,08 mol NO và a mol N2O. Để tác dụng tối đa các chất tan có trong dung dịch X cần dùng dung dịch chứa 2,04 mol NaOH. Nếu cho 400ml dung dịch Ba(OH)2 2M vào dung dịch X, thu được kết tủa là. A. 221,50 gam B. 217,60 gam C. 225,40 gam D. 220,72 gam
Đọc tiếp
Hòa tan hết hỗn hợp gồm 9,36 gam Al và 7,82 gam Al2O3 trong dung dịch chứa NaHSO4 và 0,24 mol HNO3. Sau khi kết thúc phản ứng thu được dung dịch X chỉ chứa các muối trung hòa và hỗn hợp khí Y gồm 0,08 mol NO và a mol N2O. Để tác dụng tối đa các chất tan có trong dung dịch X cần dùng dung dịch chứa 2,04 mol NaOH. Nếu cho 400ml dung dịch Ba(OH)2 2M vào dung dịch X, thu được kết tủa là.
A. 221,50 gam
B. 217,60 gam
C. 225,40 gam
D. 220,72 gam
Cho 200ml dung dịch NaOH 1M tác dụng với 150ml dung dịch H2SO4 2M. Sau phản ứng thu được dung dịch A
a) Tính khối lượng muối thu được
b) Tính nồng độ mol có trong dung dịch A
a) \(n_{NaOH}=0,2.1=0,2\left(mol\right);n_{H_2SO_4}=0,15.2=0,3\left(mol\right)\)
PTHH: 2NaOH + H2SO4 → Na2SO4 + 2H2O
Mol: 0,2 0,1
Ta có: \(\dfrac{0,2}{2}< \dfrac{0,3}{1}\) ⇒ NaOH hết, H2SO4 dư
\(m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\)
b) Vdd sau pứ = 0,2 + 0,15 = 0,35 (l)
\(C_{M_{ddNa_2SO_4}}=\dfrac{0,1}{0,35}=\dfrac{2}{7}\approx0,2857M\)
\(C_{M_{ddH_2SO_4dư}}=\dfrac{0,3-0,1}{0,35}=\dfrac{4}{7}\approx0,57M\)
Đúng 1
Bình luận (0)
Cho 200ml dung dịch A chứa HCl 1M và HNO3 2M tác dụng với 300ml dung dịch B chứa NaOH 0,8M và KOH xM thu được dung dịch C. Để trung hòa dung dịch C cần 60ml dung dịch HCl 1M.Tính x trong B và khối lượng rắn thu được sau khi cô cạn dung dịch sau pw
Cho 200ml dung dịch
H
3
PO
4
1,5M tác dụng với 200ml dung dịch NaOH 2M. Muối thu được sau phản ứng là A.
NaH
2
PO
4
và
Na
2
HPO
4
.
B.
Na
2
HPO
4
và...
Đọc tiếp
Cho 200ml dung dịch H 3 PO 4 1,5M tác dụng với 200ml dung dịch NaOH 2M. Muối thu được sau phản ứng là
A. NaH 2 PO 4 và Na 2 HPO 4 .
B. Na 2 HPO 4 và Na 3 PO 4 .
C. NaH 2 PO 4 và Na 3 PO 4 .
D. NaHPO 4 .
Chọn A
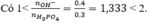
Vậy sau phản ứng thu được 2 muối NaH 2 PO 4 và Na 2 HPO 4 .
Đúng 0
Bình luận (0)
Tiến hành các thí nghiệm sau: (a) Hòa tan hỗn hợp chứa a mol Al2O3 và 2a mol Na2O vào H2O (dư). (b) Cho CrO3 tác dụng với H2O (dư). (c) Sục khí CO2 đến dư vào dung dịch chứa NaAlO2 và NaOH. (d) Cho Cu vào dung dịch Fe2(SO4)3 dư. (e) Cho dung dịch chứa a mol KHSO4 vào dung dịch chứa a mol BaCl2. (g) Cho Al dư vào dung dịch HNO3 (phản ứng không thu được chất khí). (h) Cho KHS vào dung dịch NaOH vừa đủ. Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được dung dịch chứa hai chất ta...
Đọc tiếp
Tiến hành các thí nghiệm sau:
(a) Hòa tan hỗn hợp chứa a mol Al2O3 và 2a mol Na2O vào H2O (dư).
(b) Cho CrO3 tác dụng với H2O (dư).
(c) Sục khí CO2 đến dư vào dung dịch chứa NaAlO2 và NaOH.
(d) Cho Cu vào dung dịch Fe2(SO4)3 dư.
(e) Cho dung dịch chứa a mol KHSO4 vào dung dịch chứa a mol BaCl2.
(g) Cho Al dư vào dung dịch HNO3 (phản ứng không thu được chất khí).
(h) Cho KHS vào dung dịch NaOH vừa đủ.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được dung dịch chứa hai chất tan là
A. 3
B. 2
C. 5
D. 4
Chọn C
Các mệnh đề đúng là a, b, e, g, h.
Câu c:
CO2 dư + NaOH → NaHCO3.
CO2 dư + NaAlO2 + 2H2O → Al(OH)3 + NaHCO3.
→ Chỉ có 1 chất tan là NaHCO3.
Câu d:
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4.
Ngoài ra còn có Fe2(SO4)3 dư → có 3 chất tan.
Đúng 0
Bình luận (0)
Tiến hành các thí nghiệm sau: (a) Hòa tan hỗn hợp chứa a mol Al2O3 và 2a mol Na2O vào H2O (dư). (b) Cho CrO3 tác dụng với H2O (dư). (c) Sục khí CO2 đến dư vào dung dịch chứa NaAlO2 và NaOH. (d) Cho Cu vào dung dịch Fe2(SO4)3 dư. (e) Cho dung dịch chứa a mol KHSO4 vào dung dịch chứa a mol BaCl2. (g) Cho Al dư vào dung dịch HNO3 (phản ứng không thu được chất khí). (h) Cho KHS vào dung dịch NaOH vừa đủ. Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được dung dịch chứa hai chất ta...
Đọc tiếp
Tiến hành các thí nghiệm sau:
(a) Hòa tan hỗn hợp chứa a mol Al2O3 và 2a mol Na2O vào H2O (dư).
(b) Cho CrO3 tác dụng với H2O (dư).
(c) Sục khí CO2 đến dư vào dung dịch chứa NaAlO2 và NaOH.
(d) Cho Cu vào dung dịch Fe2(SO4)3 dư.
(e) Cho dung dịch chứa a mol KHSO4 vào dung dịch chứa a mol BaCl2.
(g) Cho Al dư vào dung dịch HNO3 (phản ứng không thu được chất khí).
(h) Cho KHS vào dung dịch NaOH vừa đủ.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được dung dịch chứa hai chất tan là
![]()
![]()
![]()
![]()
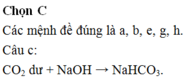
C O 2 d ư + N a A l O 2 + 2 H 2 O → A l O H 3 + N a H C O 3

Đúng 0
Bình luận (0)