Lập phương trình hoá học của các phản ứng sau:
a)Sắt+khí oxi ->Sắt(III)oxit
b)Kali+Nước->Kali hidroxit+ Khí Hidro
Câu 3. Lập phương trình hóa học của các phản ứng sau:
a. Khí hidro + sắt (III) oxit (Fe2O3) Sắt + nước
b. Sắt + khí oxi Sắt từ oxit (Fe3O4)
c. Khí hidro + khí oxi Nước
d. Kali + khí clo Kali clorua
e. Cacbon + oxit sắt từ (Fe3O4) sắt + khí cacbonic
f. Photpho + khí oxi Điphotpho pentaoxit (P2O5)
g. Canxi + axit photphoric (H3PO4) Canxi photphat (Ca3(PO4)2) + khí hidro
h. Canxi cacbonat (CaCO3) + axit clohidric (HCl) Canxi clorua (CaCl2)+ nước + khí cacbonic
i. Nhôm oxit (Al2O3) + axit sunfuruc (H2SO4) Nhôm sunfat (Al2(SO4)3) + nước
Câu 4. Hãy lập các phương trình hóa học của các phản ứng sau :
a. Na + O2 Na2O
b. Fe + HCl FeCl2 + H2
c. Al + CuCl2 AlCl3 + Cu
d. BaCl2 + AgNO3 AgCl + Ba(NO3)2
e. NaOH + Fe2(SO4)3 Fe(OH)3 + Na2SO4
f. Pb(NO3)2 + Al2(SO4)3 Al(NO3)3 + PbSO4
g. Fe(OH)3 Fe2O3 + H2O
các bạn giúp mik chạy deadline nốt 2 bài
Vui lòng tách 2 bài ra để đc hỗ trợ nhanh nhất
Câu 3:
a. 3H2 + Fe2O3 ---to---> 2Fe + 3H2O
b. 3Fe + 2O2 ---to---> Fe3O4
c. 2H2 + O2 ---to---> 2H2O
d. 2K + Cl2 ---> 2KCl
e. 2C + Fe3O4 ---> 3Fe + 2CO2
f. 4P + 5O2 ---to---> 2P2O5
g. 3Ca + 2H3PO4 ---> Ca3(PO4)2 + 3H2
h. CaCO3 + 2HCl ---> CaCl2 + H2O + CO2
i. Al2O3 + 3H2SO4 ---> Al2(SO4)3 + 3H2O
Câu 4:
a. 4Na + O2 ---to---> 2Na2O
b. Fe + 2HCl ---> FeCl2 + H2
c. 2Al + 3CuCl2 ---> 2AlCl3 + 3Cu
d. \(BaCl_2+2AgNO_3--->2AgCl\downarrow+Ba\left(NO_3\right)_2\)
e. \(3NaOH+Fe_2\left(SO_4\right)_3--->Fe\left(OH\right)_3\downarrow+3Na_2SO_4\)
f. 3Pb(NO3)2 + Al2(SO4)3 ---> 2Al(NO3)3 + 3PbSO4
g. 2Fe(OH)3 ---to---> Fe2O3 + 3H2O
Bài 2 (1,5 điểm): Lập phương trình hóa học của các phản ứng sau (không cần trình bày):
(1) Sắt + Khí ôxi → Sắt(III) ôxit.
(2) Kali + Nước → Kali hiđrôxit + Khí Hiđrô
(3) Al + … -----> AlCl3
(4) KClO3 -----> KCl + …
(5) Fe2O3 + H2SO4 -----> … + H2O
(6) Na + … -----> NaOH + H2
\(\left(1\right)4Fe+3O_2\rightarrow2Fe_2O_3\\ \left(2\right)K+H_2O\rightarrow KOH+H_2\\ \left(3\right)2Al+6HCl\rightarrow2AlCl_3+3H_2\\ \left(4\right)2KClO_3\rightarrow2KCl+3O_2\\ \left(5\right)Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ \left(6\right)Na+H_2O\rightarrow NaOH+H_2\)
1) Sắt + Khí ôxi → Sắt(III) ôxit.
4Fe + 3O2------> 2Fe2O3
(2) Kali + Nước → Kali hiđrôxit + Khí Hiđrô
K+H2O ------> KOH +H2
(3) Al + 3Cl -----> AlCl3
(4) 2KClO3 -----> 2KCl + 3O2
(5) Fe2O3 + 3H2SO4 -----> Fe2(SO4)3 + 3H2O
(6) 2Na + 2 H2O -----> 2 NaOH +H2
1. Hoàn thành phương trình phản ứng sau:
a. Sắt + oxi à sắt III oxit
b. Lưu huỳnh + oxi à lưu huỳnh đi oxit
c. Nhôm + đồng II clo rua à nhôm clo rua + đồng
d. Sắt + axit sunfuric à sắt II sunfat + khí hiđrô
e. Canxi oxit + nước à canxi hiđrôxit
f. Kali + nước à kali hiđrôxit + khí hiđrô.
2. Tính % khối lượng mỗi nguyên tố trong các hợp chất sau:
a. Fe2O3
b. SO3
c. Fe2 (SO4)3
3.Các chất sau thuộc loại hợp chất nào :
CO2, CuO, Fe2O3, SO3,Fe2 (SO4)3,H3PO4, KOH, NaCl,
BaSO4, Al(OH)3.
Cho sắt (III) clorua FeCl3 tác dụng với 3,36 gam kali hidroxit thu được 2,14gam sắt (III) hidroxit Fe(OH)3 và 4,47 kali clorua. a) Viết phương trình hóa học của phản ứng b) Khối lượng FeCl3 đã tham gia vào phản ứng trên
a) PTHH: FeCl3 + 3KOH → Fe(OH)3 + 3KCl
b) Theo ĐLBTKL ta có:
\(m_{FeCl_3}+m_{KOH}=m_{Fe\left(OH\right)_3}+m_{KCl}\)
\(\Leftrightarrow m_{FeCl_3}=m_{Fe\left(OH\right)_3}+m_{KCl}-m_{KOH}=2,14+4,47-3,36=3,25\left(g\right)\)
Bài 9: Lập phương trình hóa học của các phản ứng sau:
a) Photpho + khí Oxi-------> Photpho(V) oxit.
b) Khí hidro + oxit sắt từ (Fe3O4)-------> Sắt + Nước.
c) Canxi + axit Photphoric (H3PO4)-------> Canxi photphat + khí hidro.
d) Canxi cacbonat + axit clohidric ------->Canxi clorua + nước + khí cacbonic.
e) Kẽm + axit clohidric-------> Kẽm clorua + hidro.
f) Magie clorua + natri cacbonat-------> Magie cacbonat + natri clorua.
g) Sắt + đồng(II) sunfat ------->Sắt(II) sunfat + đồng.
h) Khí cacbonic + canxi hidroxit ( Ca(OH)2 )-------> Canxi cacbonat + nước
\(a,4P+5O_2\xrightarrow{t^o}2P_2O_5\\ b,Fe_3O_4+4H_2\to 3Fe+4H_2O\\ c,3Ca+2H_3PO_4\to Ca_3(PO_4)_2+3H_2\\ d,CaCO_3+2HCl\to CaCl_2+H_2O+CO_2\uparrow\\ e,Zn+2HCl\to ZnCl_2+H_2\\ f,MgCl_2+Na_2CO_3\to MgCO_3\downarrow+2NaCl\\ g,Fe+CuSO_4\to FeSO_4+Cu\\ h,CO_2+Ca(OH)_2\to CaCO_3\downarrow+H_2O\)
Câu 1: Lập phương trình hóa học của các phản ứng sau:
a, khí hidro + sắt (II) oxit
b, điphotpho pentaoxit + nước
c, magie + axit clohidric
d, natri + nước
e, canxi oxit + nước
f, sắt từ oxit + khí hidro
Câu 2: khử 12g sắt (III) oxit bằng khí hidro
a, tính thể tích khí hidro (đktc) cần dùng
b, tính khối lượng sắt thu được sau phản ứng
Câu 3: để đốt cháy 1mol khí hidro thì cần bao nhiêu lít khí oxit? giả sử các chất khí đo ở đktc
Câu 1 :
\(a.\) \(Fe_2O_3+3H_2\underrightarrow{^{^{t^0}}}2Fe+3H_2O\)
\(b.P_2O_5+3H_2O\rightarrow2H_3PO_4\)
\(c.Mg+2HCl\rightarrow MgCl_2+H_2\)
\(d.Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(e.CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(f.Fe_3O_4+4H_2\underrightarrow{^{^{t^0}}}3Fe+4H_2O\)
Câu 2 :
\(n_{Fe_2O_3}=\dfrac{12}{160}=0.075\left(mol\right)\)
\(Fe_2O_3+3H_2\underrightarrow{^{^{t^0}}}2Fe+3H_2O\)
\(0.075......0.225..0.15\)
\(V_{H_2}=0.225\cdot22.4=5.04\left(l\right)\)
\(m_{Fe}=0.15\cdot56=8.4\left(g\right)\)
Câu 3 :
\(2H_2+O_2\underrightarrow{^{^{t^0}}}2H_2O\)
\(1.........0.5\)
\(V_{O_2}=0.5\cdot22.4=11.2\left(l\right)\)
Câu 3 Lập Phương trình hoá học của các phản ứng sau rồi xác Định loại phản ứng
A.Đốt khí hidro,cacbon,sắt,photpho,lưu huỳnh,nhôm,canxi,magie
B.Dẫn khí hidro đi qua bột sắt(III)oxit,chì (II)oxit,Đồng(II)oxit,sắt từ oxit nung nóng.
C.Cho hidro tác dụng cới clo va brom(Br\(_2\))
a)\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
\(C+O_2\underrightarrow{t^o}CO_2\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
\(S+O_2\underrightarrow{t^o}SO_2\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(2Ca+O_2\underrightarrow{t^o}2CaO\)
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
\(\Rightarrow\)phản ứng hóa hợp.
b)\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
\(PbO+H_2\rightarrow Pb+H_2O\)
\(CuO+H_2\rightarrow Cu+H_2O\)
\(Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\)
\(\Rightarrow\)phản ứng thế.
c)\(H_2+Cl_2\underrightarrow{askt}2HCl\)
\(H_2+Br_2\underrightarrow{350^oC,xtPt}2HBr\)
\(\Rightarrow\)phản ứng hóa hợp
: Từ các phản ứng hoá học được ghi theo phương trình chữ sau đây, em hãy lập các PTHH và cho biết tỉ lệ số nguyên tử, số phân tử chất tham gia phản ứng.
a) Sắt + khí clo → Sắt (III) clorua
b) Sắt + khí oxi → Sắt từ oxit.
c) Kali cacbonat + axit sunfuric → Kali sunfat + khí cacbonic + nước.
Cho biết:
gốc cacbonat: CO3; gốc clrua: Cl; gốc sunfat: SO4; axit sunfuric: H2SO4; Sắt từ oxit: Fe3O4.
\(a,2Fe+3Cl_2\xrightarrow{t^o}2FeCl_3\\ 2:3:2\\ b,3Fe+2O_2\xrightarrow{t^o}Fe_3O_4\\ 3:2:1\\ c,K_2CO_3+H_2SO_4\to K_2SO_4+H_2O+CO_2\uparrow\\ 1:1:1:1:1\)
II- BÀI TẬP TỰ LUẬN :
Bài 1: Viết phương trình hóa học cho các phản ứng giữa hidro và các oxit sau:a. Sắt (III) oxitb. Thủy ngân (II) oxitc. Chì (II) oxit
Bài 2: Khử 48 gam đồng(II) oxit bằng khí hiđro. Hãy:
a) Tính số gam đồng kim loại thu được.
b) Tính thể tích khí hiđro (đktc) cần dùng
Bài 3: Khử 21,7 gam thủy ngân(II) oxit bằng hiđro. Hãy:
a) Tính số gam thủy ngân thu được.
b) Tính số mol và thể tích khí hiđro (đktc) cần dùng
Bài 4: Tính thể tích oxi (đktc) thu được khi phân hủy 4,9 gam KClO3 trong phòng thí
nghiệm?
Bài 5: Tính số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít oxi (các thể tích đo ở đktc).
Bài 6: Cho các kim loại kẽm, nhôm, sắt, lần lượt tác dụng với dung dịch H2SO4 loãng.
a, Viết phản ứng hóa học?
b, Cho cùng một khối lượng kim loại trên tác dụng hết với axit thì kim loại nào cho nhiều khí hiđro nhất?
c, Nêú thu được cùng một thể tích khí H2 thì khối lượng của kim loại nào đã phản ứng là nhỏ nhất?
Bài 7: Dẫn 2,24 lít khí H2 ở đktc vào một ống có chứa 12g CuO đã nung nóng tới nhiệt độ thích hợp. Kết thúc phản ứng trong ống còn a(g) chất rắn.
a. Viết phương trình phản ứng.
b. Tính khối lượng nước tạo thành sau phản ứng trên.
c. Tính a.
3.
nHgO = 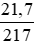
Phương trình hóa học của phản ứng khử HgO:
HgO + H2 → Hg + H2O
nHg = 0,1 mol.
mHg = 0,1 .201 = 20,1g.
nH2 = 0,1 mol.
VH2 = 0,1 .22,4 =2,24l.
1.
Phương trình phản ứng:
Fe3O4 + 4H2 → 4H2O + 3Fe
HgO + H2 → H2O + Hg
PbO + H2 → H2O + Pb
2.
a. Số mol đồng (II) oxit: n = m/M = 48/80 = 0,6 (mol)
Phương trình phản ứng:
CuO + H2 to→ H2O + Cu
1 mol 1 mol 1 mol
0,6 0,6 0,6
Khối lượng đồng kim loại thu được: m = n.M = 0,6.64 = 38,4 (g)
b. Thể tích khí hiđro cần dùng ở đktc là:
V = 22,4.n = 22,4.0,6 = 13,44 (lít).