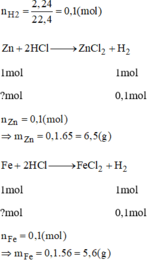b) Điều chế hidro bằng cách đổ dung dịch axit clohidric loãng vào phễu. Mở khóa cho dung dịch axit chảy xuống lọ và tác dụng với kẽm. Thu khí hidro bằng 2 cách:
C1: gọi là phương pháp đẩy nước.
C2: Gọi là phương pháp đẩy không khí
Giải thích vì sao có thể thu khí hidro bằng hai cách trên? Khi thu khí hidro bằng phương pháp đẩy không khí, người ta phải úp ngược dụng cụ thu ( ống nghiệm hoặc lọ......)
c) Phản ứng thế
Cho hai phản ứng hóa học:
Zn + 2HCl → ZnCl2 + H2↑
Fe + H2SO4 → FeSO4 + H2↑
Trong hai phản ứng này, nguyên tử của đơn chất Zn hoặc Fe đã thay thế nguyên tử nào trong axit?
Hai phản ứng háo học trên đc gọi là phản ứng thế. Vậy phản ứng thế là gì?
Chọn từ/ cụm từ điển vào chỗ trống
( nguyên tử của nguyên tố clo, nguyên tử của nguyên tố hidro, hai chất, đơn chất và hợp chất, đơn chất, hợp chất)
- Nguyên tử của đơn chất Zn hoặc Fe đã thay thế .....(1)...... trong hợp chất axit
- Phản ứng thế là phản ứng hóa học giữa .....(2)......., trong đó nguyên tử của .....(3)...... thay thế nguyên tử của nguyên tố khác trong ......(4)........