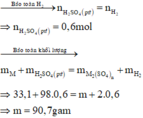hòa tan hoàn toàn 8.4g kim loại Fe vào dd H2SO4 loãng, dư. kết thúc phản ứng thấy có thoát ra V lít khí H2 (dktc), cô cạn dd thu được m gam muối
a) Viết PTPƯ xảy ra
b) tính giá trị V và m
c) nếu thay axit H2SO4 bằng axit HCl. tính thể tích HCl 1M cần dùng để phản ứng vừa đủ với lượng kim loại Fe trên