Nêu nguyên tắn điều chế khí clo trog phòng TN . Viết PTHH điều chế khí clo trong phòng TN ( ghi rõ điều kiện ) để minh họa .
Hoàn thành bảng sau: (viết các PTHH minh họa, ghi rõ điều kiện)
| Nguyên tố Halogen | Flo | Clo | Brom | Iot | |
| Tính chất vật lí | |||||
| Độ âm điện | |||||
| Tính oxi hóa | |||||
| Tính chất hóa học ( tác dụng với: kim loại, hidro, nước) | |||||
| Điều chế (trong phòng TN và trong công nghiệp) |
Nêu phương pháp và vẽ hình mô tả quá trình điều chế khí clo trong phòng thí nghiệm? Viết phương trình hóa học minh họa và giải thích quá trình để thu được khí clo tinh khiết.
- Phương pháp điều chế clo trong phòng thí nghiệm: Đun nóng nhẹ dung dịch HCl đậm đặc với chất oxi hóa mạnh như MnO2 (hoặc KMnO4).
MnO2 + 4HCl \(\underrightarrow{t^o}\) MnCl2 + Cl2 + 2H2O
Để thu được khí clo tinh khiết:
- Bình H2SO4 đặc có tác dụng làm khô khí clo.
- Clo nặng hơn không khí Þ Thu bằng cách đẩy không khí.
- Bông tẩm xút: tránh để clo độc bay ra ngoài.
Nêu nguyên liệu dùng để điều chế oxi, hidro trong phòng thí nghiệm. Viết pthh minh họa? Nguyên liệu dùng để điều chế oxi trong phòng thí nghiệm phải có đặc điểm gì? Không khí có thành phần như thế nào? Có thể thu khí oxi và hidro bằng những cách nào, tại sao?
Viết PTHH điều chế khí Clo trong công nghiệp và trong phòng thí nghiệm
Nguyên liệu được dùng để điều chế khí clo trong phòng thí nghiệm là:
A. H 2 SO 4
B. HCl đặc
C. HNO 3
D. H 2 SO 3
Nguyên liệu được dùng để điều chế khí clo trong phòng thí nghiệm là HCl đặc
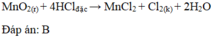
Nêu nguyên tắc của việc điều chế khí Cl2 trong phòng thí nghiệm. Viết PTHH của 5 phản ứng minh hoạ.
Cho chất oxi hoá mạnh tác dụng với dung dịch HCl đặc (từng chất oxi hoá mạnh để oxi hoá ion clorua Cl - thành đơn chất clo).
Mn O 2 + 4HCl → Mn Cl 2 + Cl 2 + 2 H 2 O
2KMn O 4 + 16HCl → 2KCl + 2Mn Cl 2 + 5 Cl 2 + 8 H 2 O
KCl O 3 + 6HCl → KCl + 3 Cl 2 + 3 H 2 O
CaO Cl 2 + 2HCl → Ca Cl 2 + Cl 2 + H 2 O
K 2 Cr 2 O 7 + 14HCl → 2KCl + 2Cr Cl 3 + 3 Cl 2 + 7 H 2 O
Làm sao để điều chế Clo. Viết 3 PTHH minh họa !!!
2NaCl + 2H2O \(\underrightarrow{đpddcmn}\) 2NaOH + H2 + Cl2
2NaCl \(\underrightarrow{đpnc}\) 2Na + Cl2
MnO2 + 4HCl \(\rightarrow\) MnCl2 + 2H2O + Cl2
Chúng ta có thể điều chế clo bằng cách cho những chất có tính oxi hóa mạnh tác dụng với hợp chất của clo
VD: 6HCl+KClO3→3Cl2+3H2O+KCl
4HCl+MnO2→Cl2+2H2O+MnCl2
16HCl+2KMnO4→5Cl2+8H2O+2KCl+2MnCl2
Hiđro clorua (HCl) là một chất khí được dùng để sản xuất axit clohiđric (một trong các axit được dùng phổ biến trong phòng thí nghiệm). Trong công nghiệp, hiđro clorua được điều chế bằng cách đốt khí hiđro trong khí clo. Tính thể tích khí clo (ở điều kiện tiêu chuẩn ) cần dùng để phản ứng vừa đủ với 67,2 lít khí hiđro ( ở đktc) và khối lượng khí hiđro clorua thu được sau phản ứng.
Nêu các bước giải bài toán theo phương trình hoá học.
b1: viết pthh
cl2+ h2-> 2hcl
b2: tính số mol cá chất dựa vào khối lượng hoăc thể tích đề bài cho
nH2= 67,2/224=3 mol
b3: dựa vào phương trình tính số mol các chất còn lại
theo pthh: ncl2=nh2=3 mol
nhcl=2nh2=3*2=6 mol
b4: tính khối lượng hoặc thể tích chất đề bài yêu cầu
=> Vcl2= 3*22,4=67,2l
mhcl=6* 36,5= 219g
CHÚC BẠN HỌC TỐT!
Bước 1: Tìm số mol chất đã cho trong đề bài.
nH2 = VH2/22,4 = 67,2/22,4 = 3 (mol)
Bước 2: Viết PTHH, cân bằng.
H2 + Cl2 -> 2HCl
Bước 3: Từ hệ số trong PTHH => số mol chất cần tìm.
3 mol -> 3 mol -> 6 mol
Bước 4: Tính theo yêu cầu đề bài.
- VCl2 = nCl2 . 22,4 = 3 . 22,4 = 67,2 (lít)
* Bài giải hoàn chỉnh:
- nH2 = VH2/22,4 = 67,2/22,4 = 3 (mol)
- H2 + Cl2 -> 2HCl
- 3 mol -> 3 mol -> 6 mol
- VCl2 = nCl2 . 22,4 = 3 . 22,4 = 67,2 (lít)
- mHCl = nHCl . MHCl = 6 . 36,5 = 219 (g)
Nếu bạn nào thắc mắc về câu trả lời của mk hay không hiểu chỗ nào, cứ việc bình luận. Mk sẽ nói rõ hơn! Mơn nhìu! >3<
Hiđro clorua (HCl) là một chất khí được dùng để sản xuất axit clohiđric (một trong các axit được dùng phổ biến trong phòng thí nghiệm). Trong công nghiệp, hiđro clorua được điều chế bằng cách đốt khí hiđro trong khí clo. Tính thể tích khí clo (ở điều kiện tiêu chuẩn ) cần dùng để phản ứng vừa đủ với 67,2 lít khí hiđro ( ở đktc) và khối lượng khí hiđro clorua thu được sau phản ứng.
Nêu các bước giải bài toán theo phương trình hoá học.
Có: nH2= 67,2:22,4=3(mol)
PTPƯ: H2 + Cl2 --to--> 2 HCl
(mol) 1 1 2
(mol) 3 3 6
(l) 67,2 67,2 134,4
(g) 6 213 219
Bước 1: Viet PTHH
H2 + Cl2 \(\rightarrow\) 2HCl
Bước 2: Ta tính số mol các chất đã cho theo gia thiết
Số mol H2 la
\(n_{H_2}=\)\(V_{H_2}\): 22,4= 67,2 : 22,4 = 3 (mol)
Bước 3: Dựa vào PTHH, ta có thể tính số mol các chất còn lại
Theo PTHH: \(n_{H_2=}2n_{HCl}=3\cdot2=6\left(mol\right)\)
Bước 4: Tính khối lượng (m) hay thể tích (V) các chất cần tìm.
Thể tích Cl cần dùng là
\(V_{Cl}=n_{Cl}\cdot22,4=3\cdot22,4=67,2\left(l\right)\)
Khối lượng HCl thu được là
\(m_{HCl}=M_{HCl}\cdot n_{HCl}=36,5\cdot6=219\left(g\right)\)
Chúc bạn học giỏi.![]()