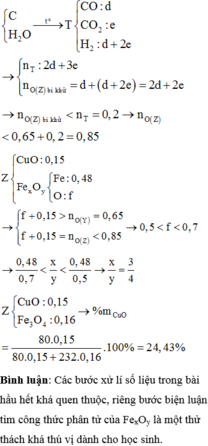Dẫn 6,72 lít khí H2 đi qua ống có chứa CuO nung nóng, sau phản ứng xảy ra hoàn toàn. a, tính khối lượng kim loại đồng và nước thu được. b, tính mCuO đã dùng

Những câu hỏi liên quan
Cho 11g hỗn hợp Al, Fe tác dụng với một lượng dư dung dịch axit Clohidric. Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít H2 (đktc). Dẫn toàn bộ lượng khí H2 này đi chậm qua ống sứ đựng 32g CuO nung nóng. Sau một thời gian, thấy trong ống sứ còn lại 26,88g chất rắn và chỉ có 80% H2 đã phản ứng.a) Viết phương trình hóa học của các phản ứng xảy ra.b) Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Đọc tiếp
Cho 11g hỗn hợp Al, Fe tác dụng với một lượng dư dung dịch axit Clohidric. Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít H2 (đktc). Dẫn toàn bộ lượng khí H2 này đi chậm qua ống sứ đựng 32g CuO nung nóng. Sau một thời gian, thấy trong ống sứ còn lại 26,88g chất rắn và chỉ có 80% H2 đã phản ứng.
a) Viết phương trình hóa học của các phản ứng xảy ra.
b) Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
a) PTHH : \(2Al+6HCl-->2AlCl_3+3H_2\) (1)
\(Fe+2HCl-->FeCl_2+H_2\) (2)
\(H_2+CuO-t^o->Cu+H_2O\) (3)
b) Ta có : \(m_{CR\left(giảm\right)}=m_{O\left(lay.di\right)}\)
=> \(m_{O\left(lay.di\right)}=32-26,88=5,12\left(g\right)\)
=> \(n_{O\left(lay.di\right)}=\frac{5,12}{16}=0,32\left(mol\right)\)
Theo pthh (3) : \(n_{H_2\left(pứ\right)}=n_{O\left(lay.di\right)}=0,32\left(mol\right)\)
=> \(tổng.n_{H_2}=\frac{0,32}{80}\cdot100=0,4\left(mol\right)\)
Đặt \(\hept{\begin{cases}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{cases}}\) => \(27a+56b=11\left(I\right)\)
Theo pthh (1) và (2) : \(n_{H_2\left(1\right)}=\frac{3}{2}n_{Al}=\frac{3}{2}a\left(mol\right)\)
\(n_{H_2\left(2\right)}=n_{Fe}=b\left(mol\right)\)
=> \(\frac{3}{2}a+b=0,4\left(II\right)\)
Từ (I) và (II) => \(\hept{\begin{cases}a=0,2\\b=0,1\end{cases}}\)
=> \(\hept{\begin{cases}m_{Al}=27\cdot0,2=5,4\left(g\right)\\m_{Fe}=56\cdot0,1=5,6\left(g\right)\end{cases}}\)
Đưa 1.344 lít khí H2 qua ống nghiệm chứa CuO nung nóng, sau khi phản ứng hoàn toàn thấy vẫn còn dư 0.448 lít H2.
- Tính khối lượng Cu thu được sau pư
- Tính khối lượng NaCl cần dùng để điện phân ra lượng H2 đã phản ứng trong quá trình trên.
\(n_{H_2\left(bđ\right)}=\dfrac{1.344}{22.4}=0.06\left(mol\right)\)
\(n_{H_2\left(dư\right)}=\dfrac{0.448}{22.4}=0.02\left(mol\right)\)
\(\Rightarrow n_{H_2\left(pư\right)}=0.06-0.02=0.04\left(mol\right)\)
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
\(.......0.04..0.04\)
\(m_{Cu}=0.04\cdot64=2.56\left(g\right)\)
\(2NaCl+2H_2O\underrightarrow{^{^{dpcmn}}}2NaOH+2H_2+Cl_2\)
\(0.04...........................................0.04\)
\(m_{NaCl}=0.04\cdot58.5=2.34\left(g\right)\)
Đúng 1
Bình luận (0)
Dẫn 6,72 lít H2 (đktc) qua ống thủy tinh nung nóng chứa 8g CuO phản ứng xảy ra hoàn toàn
a) Viết PTHH
b) Tính khối lượng Cu
c) Số phân tử H2O tạo thành
nH2 = 6,72/22,4 = 0,3 (mol)
nCuO = 8/80 = 0,1 (mol)
PTHH: CuO + H2 -> (t°) Cu + H2O
LTL: 0,1 < 0,3 => H2 dư
nCu = nH2O = nCuO = 0,1 (mol)
mCu = 0,1 . 64 = 6,4 (g)
Số phân tử H2O: 0,1 . 6.10^23 = 0,6.10^23 (phân tử)
Đúng 2
Bình luận (1)
a. \(n_{H_2}=\dfrac{6.72}{22,4}=0,3\left(mol\right)\)
\(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
PTHH : CuO + H2 -to-> Cu + H2O
0,1 0,1 0,1
Xét tỉ lệ : 0,3 > 0,1 => H2 dư , CuO đủ
b. \(m_{Cu}=0,1.64=6,4\left(g\right)\)
c. \(A=n.N=0,1.6.10^{23}=0,6.10^{23}\) phân tử
Đúng 1
Bình luận (1)
H2+CuO-to>Cu+H2O
0,1-------0,1----0,1
n H2=\(\dfrac{6,72}{22,4}\)=0,3 mol
n CuO=\(\dfrac{8}{80}\)=0,1 mol
=>H2 dư
=>m Cu=0,1.64=6,4g
=>soospt H2O= 0,1.6.1023=6.1022pt
Đúng 2
Bình luận (1)
Cho kim loại Fe phản ứng vừa đủ với dung dịch H2SO4, thu được 3,7185 lít khí H2 ở đkc
a) Tính khối lượng kim loại đã phản ứng
b) Tính khối lượng muối tạo thành
c) Dẫn toàn bộ khí H2 sinh ra ở trên đi qua ống đựng 24g CuO đun nóng. Tính khối lượng chất rắn thu được sau phản ứng ? Biết phản ứng xảy ra hoàn toàn
a, \(n_{H_2}=\dfrac{3,7185}{24,79}=0,15\left(mol\right)\)
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Theo PT: \(n_{Fe}=n_{H_2}=0,15\left(mol\right)\Rightarrow m_{Fe}=0,15.56=8,4\left(g\right)\)
b, Theo PT: \(n_{FeSO_4}=n_{H_2}=0,15\left(mol\right)\Rightarrow m_{FeSO_4}=0,15.152=22,8\left(g\right)\)
c, \(n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,15}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{CuO\left(pư\right)}=n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow n_{CuO\left(dư\right)}=0,3-0,15=0,15\left(mol\right)\)
Chất rắn thu được sau pư gồm Cu và CuO dư.
⇒ m chất rắn = mCu + mCuO (dư) = 0,15.64 + 0,15.80 = 21,6 (g)
Đúng 3
Bình luận (0)
hoà tan hoàn toàn 6,3g hỗn hợp gồm Al và Mg vào V ml dung dịch h2so4 0,5M sau phản ứng thu được 6,72 lít khí h2 a) tính phần trăm khối lượng kim loại có trong hỗn hợp đầu b) tính V c) dẫn toàn bộ lượng h2 thu được qua a gam fe203 nung nóng sau phản ứng thu được 27,68g chất rắn A gồm Fe và Fe203. Biết hiêu suất phản ứng là 90%
a, Gọi \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Mg}=b\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH:
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
a---->1,5a--------------------------->1,5a
Mg + H2SO4 ---> MgSO4 + H2
b------>b----------------------->b
Hệ pt \(\left\{{}\begin{matrix}27a+24b=6,3\\1,5a+b=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,15\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Al}=0,1.27=2,7\left(g\right)\\m_{Mg}=0,15.24=3,6\left(g\right)\end{matrix}\right.\\ \rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{2,7}{6,3}=42,86\%\\\%m_{Mg}=100\%-42,86\%=57,14\%\end{matrix}\right.\)
b, \(n_{H_2SO_4}=0,1.1,5+0,15=0,3\left(mol\right)\)
\(\rightarrow V_{ddH_2SO_4}=\dfrac{0,3}{0,5}=0,6\left(l\right)=600\left(ml\right)\)
c, đề yêu cầu jv?
Đúng 2
Bình luận (1)
Cho 26 gam Zn vào dung dịch HCl dư sau khi phản ứng xảy ra hoàn toàn thu được V lít H2 (đktc)a, Tính V và khối lượng ZnCl2 thu được?b, Dẫn V lít khí H2 trên qua ống nghiệm đựng 46,4 gam nung nóng đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Tính m và % theo khối lượng mỗi chất trong m?c, Nếu dẫn khí H2 trên qua ống nghiệm đựng 46,4 gam chất rắn sau khi kết thúc phản ứng thu được 41,28 gam chất rắn. Tính hiệu suất phản ứng?
Đọc tiếp
Cho 26 gam Zn vào dung dịch HCl dư sau khi phản ứng xảy ra hoàn toàn thu được V lít H2 (đktc)
a, Tính V và khối lượng ZnCl2 thu được?
b, Dẫn V lít khí H2 trên qua ống nghiệm đựng 46,4 gam nung nóng đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Tính m và % theo khối lượng mỗi chất trong m?
c, Nếu dẫn khí H2 trên qua ống nghiệm đựng 46,4 gam chất rắn sau khi kết thúc phản ứng thu được 41,28 gam chất rắn. Tính hiệu suất phản ứng?
Cho 26 gam Zn vào dung dịch HCl dư sau khi phản ứng xảy ra hoàn toàn thu được V lít H2 (đktc)a, Tính V và khối lượng ZnCl2 thu được?b, Dẫn V lít khí H2 trên qua ống nghiệm đựng 46,4 gam nung nóng đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Tính m và % theo khối lượng mỗi chất trong m?c, Nếu dẫn khí H2 trên qua ống nghiệm đựng 46,4 gam chất rắn sau khi kết thúc phản ứng thu được 41,28 gam chất rắn. Tính hiệu suất phản ứng?
Đọc tiếp
Cho 26 gam Zn vào dung dịch HCl dư sau khi phản ứng xảy ra hoàn toàn thu được V lít H2 (đktc)
a, Tính V và khối lượng ZnCl2 thu được?
b, Dẫn V lít khí H2 trên qua ống nghiệm đựng 46,4 gam nung nóng đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Tính m và % theo khối lượng mỗi chất trong m?
c, Nếu dẫn khí H2 trên qua ống nghiệm đựng 46,4 gam chất rắn sau khi kết thúc phản ứng thu được 41,28 gam chất rắn. Tính hiệu suất phản ứng?
Cho 26 gam Zn vào dung dịch HCl dư sau khi phản ứng xảy ra hoàn toàn thu được V lít H2 (đktc)a, Tính V và khối lượng ZnCl2 thu được?b, Dẫn V lít khí H2 trên qua ống nghiệm đựng 46,4 gam Fe2O3 nung nóng đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Tính m và % theo khối lượng mỗi chất trong m?c, Nếu dẫn khí H2 trên qua ống nghiệm đựng 46,4 gam chất rắn sau khi kết thúc phản ứng thu được 41,28 gam chất rắn. Tính hiệu suất phản ứng?
Đọc tiếp
Cho 26 gam Zn vào dung dịch HCl dư sau khi phản ứng xảy ra hoàn toàn thu được V lít H2 (đktc)
a, Tính V và khối lượng ZnCl2 thu được?
b, Dẫn V lít khí H2 trên qua ống nghiệm đựng 46,4 gam Fe2O3 nung nóng đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Tính m và % theo khối lượng mỗi chất trong m?
c, Nếu dẫn khí H2 trên qua ống nghiệm đựng 46,4 gam chất rắn sau khi kết thúc phản ứng thu được 41,28 gam chất rắn. Tính hiệu suất phản ứng?
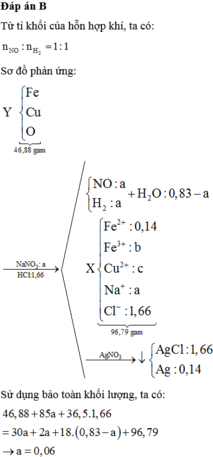
Cho hơi nước đi qua than nóng đỏ, thu được 4,48 lít (đktc) hỗn hợp khí T gồm CO, CO2 và H2. Dẫn toàn bộ T đi qua m gam hỗn hợp Z gồm FexOy và CuO nung nóng, sau khi các phản ứng xảy ra hoàn toàn, thu được 46,88 gam hỗn hợp rắn Y. Cho Y tan hoàn toàn trong dung dịch chứa NaNO3 và 1,66 mol HCl, thu được dung dịch X chỉ chứa 96,79 gam muối của kim loại và hỗn hợp hai khí gồm NO và H2, có tỉ khối so với He là 4. Cho X phản ứng hoàn toàn với dung dịch AgNO3 dư, thu được 253,33 gam kết tủa. Phần trăm...
Đọc tiếp
Cho hơi nước đi qua than nóng đỏ, thu được 4,48 lít (đktc) hỗn hợp khí T gồm CO, CO2 và H2. Dẫn toàn bộ T đi qua m gam hỗn hợp Z gồm FexOy và CuO nung nóng, sau khi các phản ứng xảy ra hoàn toàn, thu được 46,88 gam hỗn hợp rắn Y. Cho Y tan hoàn toàn trong dung dịch chứa NaNO3 và 1,66 mol HCl, thu được dung dịch X chỉ chứa 96,79 gam muối của kim loại và hỗn hợp hai khí gồm NO và H2, có tỉ khối so với He là 4. Cho X phản ứng hoàn toàn với dung dịch AgNO3 dư, thu được 253,33 gam kết tủa. Phần trăm khối lượng của CuO trong Z là
A. 25,77%
B. 24,43%
C. 23,81%
D. 25,60%