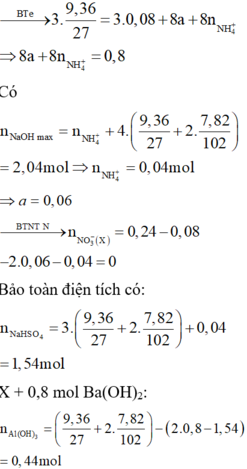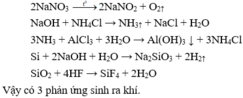Trung hòa 400ml dung dịch H2SO4 1,5M bằng dung dịch 900g dung dịch NaOH 5,6% Tính nông độ % chất tan trong dung dịch sau khi phản ứng kết thúc

Những câu hỏi liên quan
Trung hòa 100 ml dung dịch CH3COOH 0,3M bằng dung dịch NaOH 1,5M. a) Tính thể tích dung dịch NaOH đã dùng ? b) Tính khối lượng muối thu được sau phản ứng ? c) Tính nồng độ mol của chất tan có trong dung dịch sau phản ứng ( biết thể tích thay đổi không đáng kể) ? Biết C= 12; O= 16; H = 1 ; Na=23
a) \(n_{CH_3COOH}=0,1.0,3=0,03\left(mol\right)\)
PTHH: CH3COOH + NaOH --> CH3COONa + H2O
0,03---->0,03--------->0,03
=> \(V_{dd.NaOH}=\dfrac{0,03}{1,5}=0,02\left(l\right)\)
b) mCH3COONa = 0,03.82 = 2,46 (g)
c) \(C_{M\left(CH_3COONa\right)}=\dfrac{0,03}{0,1+0,02}=0,25M\)
Đúng 2
Bình luận (0)
Bài 5. Cho 100ml dung dịch H2SO4 2M tác dụng với 400ml dung dịch NaOH 1,5M thu được dung dịch A. Tính nồng độ mol các chất tan trong dung dịch A.Bài 6. Cho 100ml dung dịch H2SO4 2M tác dụng với 400ml dung dịch NaOH 1,5M ta thu được dung dịch A. Tính nồng độ mol các chất trong dung dịch A.Bài 7. Trộn 300ml dung dịch Ba(OH)2 1M với 200ml dung dịch H2SO4 1M ta thu được dung dịch A và mg kết tủa. Tính giá trị của m và nồng độ mol các chất trong dd A.Bài 8. Trộn 200ml dung dịch Na2CO3 với 300ml dung...
Đọc tiếp
Bài 5. Cho 100ml dung dịch H2SO4 2M tác dụng với 400ml dung dịch NaOH 1,5M thu được dung dịch A. Tính nồng độ mol các chất tan trong dung dịch A.
Bài 6. Cho 100ml dung dịch H2SO4 2M tác dụng với 400ml dung dịch NaOH 1,5M ta thu được dung dịch A. Tính nồng độ mol các chất trong dung dịch A.
Bài 7. Trộn 300ml dung dịch Ba(OH)2 1M với 200ml dung dịch H2SO4 1M ta thu được dung dịch A và mg kết tủa. Tính giá trị của m và nồng độ mol các chất trong dd A.
Bài 8. Trộn 200ml dung dịch Na2CO3 với 300ml dung dịch HCl 1M ta thu được dung dịch A và V lít khí CO2 ở đktc. Tính V và nồng độ mol các chất trong dung dịch A.
các bạn giúp mình với ạ
Trung hòa 400ml dung dịch H2SO4 1M bằng dung dịch NaOH 0,5M.
a/ Viết phương trình phản ứng hóa học xảy ra?
b/ Tính thể tích dung dịch NaOH 0,5M đã dùng?
c/Tính nồng độ mol/l dung dịch thu được phản ứng sau?
\(n_{H_2SO_4}=0,4\cdot1=0,4mol\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+H_2O\)
0,8 0,4
\(V_{NaOH}=\dfrac{0,8}{0,5}=1,6l\)
Đúng 2
Bình luận (1)
\(n_{H_2SO_4}=0.4\cdot1=0.4\left(mol\right)\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
\(0.8.............0.4..............0.4\)
\(V_{dd_{NaOH}}=\dfrac{0.8}{0.5}=1.6\left(l\right)\)
\(V_{dd}=0.4+1.6=2\left(l\right)\)
\(C_{M_{Na_2SO_4}}=\dfrac{0.4}{2}=0.2\left(M\right)\)
Đúng 1
Bình luận (0)
Hòa tan hết hỗn hợp gồm 9,36 gam Al và 7,82 gam Al2O3 trong dung dịch chứa NaHSO4 và 0,24 mol HNO3. Sau khi kết thúc phản ứng thu được dung dịch X chỉ chứa các muối trung hòa và hỗn hợp khí Y gồm 0,08 mol NO và a mol N2O. Để tác dụng tối đa các chất tan có trong dung dịch X cần dùng dung dịch chứa 2,04 mol NaOH. Nếu cho 400ml dung dịch Ba(OH)2 2M vào dung dịch X, thu được kết tủa là. A. 221,50 gam B. 217,60 gam C. 225,40 gam D. 220,72 gam
Đọc tiếp
Hòa tan hết hỗn hợp gồm 9,36 gam Al và 7,82 gam Al2O3 trong dung dịch chứa NaHSO4 và 0,24 mol HNO3. Sau khi kết thúc phản ứng thu được dung dịch X chỉ chứa các muối trung hòa và hỗn hợp khí Y gồm 0,08 mol NO và a mol N2O. Để tác dụng tối đa các chất tan có trong dung dịch X cần dùng dung dịch chứa 2,04 mol NaOH. Nếu cho 400ml dung dịch Ba(OH)2 2M vào dung dịch X, thu được kết tủa là.
A. 221,50 gam
B. 217,60 gam
C. 225,40 gam
D. 220,72 gam
cho 200ml dung dịch NaOH 0,5M vào 300ml dung dịch H2SO4 1,5M theo pt:
2NaOH + H2SO4 -> Na2SO4 + 2H2O
A. chất nào còn dư sau phản ứng có khối lượng bao nhiêu
B. tính nồng độ mol các chất tan trong dung dịch sau phản ứng
Ta có: \(\left\{{}\begin{matrix}n_{NaOH}=0,2\cdot0,5=0,1\left(mol\right)\\n_{H_2SO_4}=0,3\cdot1,5=0,45\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{2}< \dfrac{0,45}{1}\) \(\Rightarrow\) Axit còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{Na_2SO_4}=0,05\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{Na_2SO_4}}=\dfrac{0,05}{0,2+0,3}=0,1\left(M\right)\\C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0,4}{0,5}=0,8\left(M\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
200ml = 0,2l
300ml = 0,3l
Số mol của dung dịch natri hidroxit
CMNaOH = \(\dfrac{n}{V}\Rightarrow n=C_M.V=0,5.0,2=0,1\left(mol\right)\)
Số mol của dung dịch axit sunfuric
CMH2SO4 = \(\dfrac{n}{V}\Rightarrow n=C_M.V=1,5.0,3=0,45\left(mol\right)\)
Pt : 2NaOH + H2SO4 → Na2SO4 + 2H2O\(|\)
2 1 1 2
0,1 0,45 0,05
a) Lập tỉ số so sánh : \(\dfrac{0,1}{2}< \dfrac{0,45}{1}\)
⇒ NaOH phản ứng hết , H2SO4 dư
⇒ Tính toán dựa vào số mol của NaOH
Số mol dư của dung dịch axit sunfuric
ndư= nban đầu - nmol
= 0,45 - \(\left(\dfrac{0,1.1}{2}\right)\)
= 0,4 (mol)
Khối lượng dư của dung dịch xxit sunfuric
mdư = ndư . MH2SO4
= 0,4. 98
= 39,2 (g)
b) Số mol của natri sunfat
nNa2SO4= \(\dfrac{0,1.1}{2}=0,05\left(mol\right)\)
Thể tích của dung dịch sau phản ứng
Vdung dịch sau phản ứng= 0,2 + 0,3
= 0,5 (l)
Nồng độ mol của natri sunfat
CMNa2SO4 = \(\dfrac{n}{V}=\dfrac{0,05}{0,5}=0,1\left(M\right)\)
Nồng độ mol của dung dịch axit sunfuric
CMH2SO4 = \(\dfrac{n}{V}=\dfrac{0,4}{0,5}=0,8\left(M\right)\)
Chúc bạn học tốt
Đúng 0
Bình luận (0)
Cho 300 g dd HCl 7,3% tác dụng với dung dịch NaOH 5% sau phản ứng kết thúc, trung hòa dung dịch sau phản ứng cần dùng 200g dung dịch H2SO4 9,8%.Tính khối lượng dung dịch NaOH cần dùng.
Xem chi tiết
\(m_{HCl}=\dfrac{300.7,3\%}{100\%}=21,9g\\ n_{HCl}=\dfrac{21,9}{36,5}=0,6mol\\ HCl+NaOH\rightarrow NaCl+H_2O\left(1\right)\\ n_{NaOH\left(1\right)}=n_{HCl}=0,6mol\\ m_{H_2SO_4}=\dfrac{200.9,8\%}{100\%}=19,6g\\ n_{H_2SO_4}=\dfrac{19,6}{98}=0,2mol\\ H_2SO_4+2NaOH\rightarrow Na_2SO_4+2H_2O\left(2\right)\\ n_{NaOH\left(2\right)}=0,2.2=0,4mol\\ n_{NaOH}=0,4+0,6=1mol\\ m_{NaOH}=1.40=40g\\ m_{ddNaOH}=\dfrac{40}{5\%}\cdot100\%=800g\)
Đúng 1
Bình luận (0)
Câu 12. Trung hòa vừa đủ 500ml dung dịch gồm NaOH 0,5M và Ba(OH)2 1M với dung dịch H2SO4 15%. Sau khi phản ứng kết thúc thấy tạo ra chất kết tủa màu trắng. Hãy :a) Tính khối lượng dung dịch H2SO4 đã dùng .b) Tính khối lượng chất kết tủa thu được.c) Tính CM của Na2SO4 biết D H2SO4 1,14 g/cm3
Đọc tiếp
Câu 12. Trung hòa vừa đủ 500ml dung dịch gồm NaOH 0,5M và Ba(OH)2 1M với dung dịch H2SO4 15%. Sau khi phản ứng kết thúc thấy tạo ra chất kết tủa màu trắng. Hãy :
a) Tính khối lượng dung dịch H2SO4 đã dùng .
b) Tính khối lượng chất kết tủa thu được.
c) Tính CM của Na2SO4 biết D H2SO4 = 1,14 g/cm3
hòa tan hoàn toàn 5,12g hỗn hợp X gồm mg và fe trong mg dung dịch hcl 36,5% đến khi phản ứng kết thúc thu được 2,688l H2 dttc và dung dịch Y. để trung hòa hết lượng hcl dư trong Y cần dùng 60ml naoh 1M tính nồng độ % các chất tan trong dung dịch Y.
Đặt \(\left\{{}\begin{matrix}n_{Mg}=n_{MgCl_2}=a\left(mol\right)\\n_{Fe}=n_{FeCl_2}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow24a+56b=5,12\) (1)
Ta có: \(n_{H_2}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
Bảo toàn electron: \(2a+2b=0,24\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=n_{MgCl_2}=0,05\left(mol\right)\\b=n_{FeCl_2}=0,07\left(mol\right)\end{matrix}\right.\)
Bảo toàn nguyên tố: \(n_{HCl\left(p/ứ\right)}=2n_{MgCl_2}+2n_{FeCl_2}=0,24\left(mol\right)\)
PTHH: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Theo PTHH: \(n_{HCl\left(dư\right)}=n_{NaOH}=0,06\left(mol\right)\)
\(\Rightarrow\Sigma n_{HCl}=0,3\left(mol\right)\) \(\Rightarrow m_{ddHCl}=\dfrac{0,3\cdot36,5}{36,5\%}=30\left(g\right)\)
Mặt khác: \(m_{H_2}=0,12\cdot2=0,24\left(g\right)\)
\(\Rightarrow m_{dd}=m_{KL}+m_{ddHCl}-m_{H_2}=34,88\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{0,07\cdot127}{34,88}\cdot100\%\approx25,49\%\\C\%_{MgCl_2}=\dfrac{0,05\cdot95}{34,88}\cdot100\%\approx13,62\%\\C\%_{HCl\left(dư\right)}=\dfrac{0,04\cdot36,5}{34,88}\cdot100\%\approx4,19\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Thực hiện các thí nghiệm sau: (1) Nhiệt phân muối
NaNO
3
.
(2) Nhỏ dung dịch NaOH vào dung dịch
NH
4
Cl
.
(3) Cho dung dịch
NH
3
vào dung dịch
AlCl
3
dư. (4) Hòa tan Si trong dung dịch NaOH (5) Hòa tan
SiO
2
trong dung dịch HF. Sau khi các phản ứng kế...
Đọc tiếp
Thực hiện các thí nghiệm sau:
(1) Nhiệt phân muối NaNO 3 . (2) Nhỏ dung dịch NaOH vào dung dịch NH 4 Cl . (3) Cho dung dịch NH 3 vào dung dịch AlCl 3 dư. (4) Hòa tan Si trong dung dịch NaOH (5) Hòa tan SiO 2 trong dung dịch HF. Sau khi các phản ứng kết thúc, số thí nghiệm sinh ra chất khí là
A. 5
B. 3
C. 2
D. 4