Cho m gam Fe tác dụng với dung dịch H2 SO4 loãng dư thu được 30,4 gam Fe2 SO4. giá trị của m là?

Những câu hỏi liên quan
Cho 8,50 gam hỗn hợp Na và K tác dụng hết với nước thu được 3,36 lít khí H2 (đktc) và dung dịch X. Cho X tác dụng vừa đủ với dung dịch Fe2(SO4)3 thu được m gam kết tủa. Giá trị của m là: A.5,35. B.16,05. C. 10,70. D. 21,40.
Đọc tiếp
Cho 8,50 gam hỗn hợp Na và K tác dụng hết với nước thu được 3,36 lít khí H2 (đktc) và dung dịch X. Cho X tác dụng vừa đủ với dung dịch Fe2(SO4)3 thu được m gam kết tủa. Giá trị của m là:
A.5,35.
B.16,05.
C. 10,70.
D. 21,40.
Đáp án C
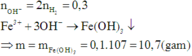
Nhận xét:Ở bài này, giả thiết cho thừa dữ kiện về tổng khối lượng hai kim loại. Đề bài sẽ hay hơn khi thay một trong hai kim loại kiềm trong hỗn hợp bằng kim loại Ba, khi đó kết tủa tạo thành gồm Fe(OH)3 và BaSO4. Để tính n F e ( O H ) 3 ta vẫn có cách làm như trên, tuy nhiên để tính được n B a S O 4 thì ta cần biết nBa , khi đó ta cần lập và giải hệ 2 phương trình bậc nhất 2 ẩn là nBa và nNa (hoặc nK ) theo giả thiết về khối lượng và n H 2 .
Đúng 0
Bình luận (0)
cho 26,92 g hỗn hợp A gồm Mg Al Fe tác dụng vừa hết với 160 gam dung dịch H2 SO4 98% thu được dung dịch B chứa m gam muối sunfat 9,6 gam S và V lít khí SO2.giá trị của m là
Ta có: \(m_{H_2SO_4}=160.98\%=156,8\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{156,8}{98}=1,6\left(mol\right)\)
\(n_S=\dfrac{9,6}{32}=0,3\left(mol\right)\)
\(4H_2SO_4+6e\rightarrow3SO_4^{2-}+S+4H_2O\)
1,2_______________0,9___0,3 (mol)
\(2H_2SO_4+2e\rightarrow SO_4^{2-}+SO_2+2H_2O\)
0,4______________0,2_____0,2 (mol)
⇒ m muối = mA + mSO42- = 26,92 + (0,9 + 0,2).96 = 132,52 (g)
Đúng 3
Bình luận (0)
Cho 3,66 gam hỗn hợp gồm Na và Ba tác dụng với nước dư thu được dung dịch X và 0,896 lít H2 (đktc). Cho 100ml dung dịch Al2(SO4)3 0,1M vào dung dịch X, thu được m gam kết tủa. Giá trị của m là:
A. 4,66.
B. 1,56.
C. 6,22.
D. 5,44.
Cho 22,4g Fe tác dụng với dung dịch loãng có chứa 24,5 g H2SO4 sau phản ứng hãy cho biết: a, Chất nào dư sau phản ứng và dư bao nhiêu gam? b, Tính thể tích H2 thu được ở đktc. Có đc ghi fe +h2so4--->fe2(so4)3 +h2 đc ko ạ
`Fe + H_2 SO_4 -> FeSO_4 + H_2`
`0,25` `0,25` `0,25` `(mol)`
`a)n_[Fe]=[22,4]/56=0,4(mol)`
`n_[H_2 SO_4]=[24,5]/98=0,25(mol)`
Có: `[0,4]/1 > [0,25]/1=>Fe` hết, `H_2 SO_4`
`=>m_[Fe(dư)]=(0,4-0,25).56=8,4(g)`
`b)V_[H_2]=0,25.22,4=5,6(l)`
Ko được ghi `Fe+H_2 SO_4->Fe_2 (SO_4)_3+H_2` vì đây là `H_2 SO_4` loãng
Đúng 4
Bình luận (2)
Cho m gam Fe tác dụng với O2 thu được 27,2 gam hỗn hợp A gồm FeO, Fe3O4, Fe2O3, Fe dư. Cho hỗn hợp A tác dụng hết với dung dịch H2SO4 98% đun nóng thu được 6,72 lít khí SO2 (đktc) và dd B chỉ chứa muối Fe2(SO4)3 .Khối lượng m và khối lượng dung dịch H2SO4 đã dùng lần lượt là?
Hòa tan 30 gam hợp X gồm FeO, Fe2O3, Fe3O4 bằng H2SO4 đặc, dư thu được 11,2 lít khí SO2 duy nhất (thấp nhất) và dung dịch X Cô cạn dung dịch X thu được m gam muối khan. Mặt khác, cho 30 gam X trên tác dụng với H2SO4 loãng, dư thu x gam Fe2(SO4)3. Tìm m, x
Coi hỗn hợp X gồm : Fe , O
\(n_{Fe}=a\left(mol\right),n_O=b\left(mol\right)\)
\(m_X=56a+16b=30\left(g\right)\left(1\right)\)
\(n_{SO_2}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
\(\text{Bảo toàn e : }\)
\(3n_{Fe}=2n_O+2n_{SO_2}\)
\(\Rightarrow3a=2b+1\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.475,b=0.2125\)
\(n_{Fe_2\left(SO_4\right)_3}=\dfrac{0.475}{2}=0.2375\left(mol\right)\)
\(m_{Fe_2\left(SO_4\right)_3}=0.2375\cdot400=95\left(g\right)\)
Đúng 2
Bình luận (0)
Coi X gồm Fe(a mol) ; O(b mol)
=> 56a + 16b = 30(1)
n SO2 = 11,2/22,4 = 0,5(mol)
Bảo toàn e : 3n Fe = 2n O + 2n SO2
<=> 3a - 2b = 1(2)
Từ (1)(2) suy ra a = 0,475 ; b = 0,2125
n Fe2(SO4)3 = 0,5a = 0,2375(mol)
=> m = 0,2375.400 = 95(gam)
Thí nghiệm 2 :
Gọi n FeSO4 = y(mol) ; n Fe2(SO4)3 = x(mol)
Bảo toàn nguyên tố Fe : x + y = 0,475
Bảo toàn e : 2x.3 + 2y = 0,2125.2
=> x = -0,13125 <0
(Sai đề)
Đúng 1
Bình luận (0)
Cho 10 gam Fe và Cu tác dụng với dung dịch H2SO4 loãng (dư). Sau phản ứng thu được 2,24 lít H2 (đktc), dung dịch X và m gam chất rắn không tan. Giá trị m là A. 3,4 gam B. 4,4 gam C. 5,6 gam D. 6,4 gam.
Đọc tiếp
Cho 10 gam Fe và Cu tác dụng với dung dịch H2SO4 loãng (dư). Sau phản ứng thu được 2,24 lít H2 (đktc), dung dịch X và m gam chất rắn không tan. Giá trị m là
A. 3,4 gam
B. 4,4 gam
C. 5,6 gam
D. 6,4 gam.
Cho m gam hỗn hợp gồm Fe và Fe2O3 tác dụng với dung dịch H2SO4 vừa đủ thu được dung dịch A chứa 55,2 gam muối và 2,24 lit H2. a. Tính m b. Tính khối lượng H2SO4 phản ứngBiết Fe2O3 + H2SO4 ® Fe2(SO4)3 + H2O
Đọc tiếp
Cho m gam hỗn hợp gồm Fe và Fe2O3 tác dụng với dung dịch H2SO4 vừa đủ thu được dung dịch A chứa 55,2 gam muối và 2,24 lit H2.
a. Tính m
b. Tính khối lượng H2SO4 phản ứng
Biết Fe2O3 + H2SO4 ® Fe2(SO4)3 + H2O
Dẫn 3,584 lít CO (đktc) đi qua m gam hỗn hợp FeO và CuO nung nóng. Sau một thời gian, thu được hỗn hợp rắn X và hỗn hợp khí Y có tỉ khối so với H2 là 16. Hòa tan hoàn toàn X trong dung dịch H SO4 đặc, nóng, dư, thu được 1,68 lít khí SO2 (sản phẩm khử duy nhất của S+6) và dung dịch Z. Cho Z tác dụng hoàn toàn với dụng dịch KOH loãng dư, thu được 12,39 gam kết tủa. Giá trị của m là A. 9,20. B. 9,60. C. 8,64. D. 9,04.
Đọc tiếp
Dẫn 3,584 lít CO (đktc) đi qua m gam hỗn hợp FeO và CuO nung nóng. Sau một thời gian, thu được hỗn hợp rắn X và hỗn hợp khí Y có tỉ khối so với H2 là 16. Hòa tan hoàn toàn X trong dung dịch H SO4 đặc, nóng, dư, thu được 1,68 lít khí SO2 (sản phẩm khử duy nhất của S+6) và dung dịch Z. Cho Z tác dụng hoàn toàn với dụng dịch KOH loãng dư, thu được 12,39 gam kết tủa. Giá trị của m là
A. 9,20.
B. 9,60.
C. 8,64.
D. 9,04.