Câu 4 (1 điểm):
(a) Đá vôi có công thức CaCO3. Công thức trên cho biết những gì?
(b) Tính phần trăm khối lượng của P trong hợp chất P2O5.
(c) Trong hợp chất X của lưu huỳnh với oxi thì lưu huỳnh chiếm 40% về khối lượng. Hãy tìm công thức của X.
thực hiền cho biết nguyên tố Natri chiếm 59 phần trăm về khối lượng trong hợp chất lưu huỳnh .hãy viết công thức hóa học và tính phân tử khối trong hợp chất của lưu huỳnh và Oxi ,lưu huỳnh chiếm 50 phần trăm về khối lượng . hãy xác định phân tử khối của hợp chất
Đặt CTHH của hợp chất là NaxSyNaxSy
Theo bài ra :
x:y=%MNa23:%MS32=59%23:41%32=2:1x:y=%MNa23:%MS32=59%23:41%32=2:1
Vậy CTHH của hợp chất là Na2SNa2S
PTK=2.23+32=78(ĐvC)
Theo để, suy ra %mS = 100% - 59% = 41%
Đặt CTHH là NaxSy
=> x : y = 5923:4132=2,56:1,28=2:15923:4132=2,56:1,28=2:1
=> CTHH: Na2S
Dạng bài tập 4: Tính theo công thức hóa học
Câu 1: Tính phần trăm khối lượng của các nguyên tố trong hợp chất: NaNO3; K2CO3 , Al(OH)3, SO2, SO3, Fe2O3.
Câu 2: Một oxit của lưu huỳnh có thành phần trăm của lưu huỳnh là 50% và Oxi là 50%. Biết oxit này có khối lượng mol phân tử là 64 g/mol. Hãy tìm công thức hóa học của oxit
Câu 1 :
\(M_{K_2CO_3}=39.2+12+16.3=138\left(dvC\right)\)
\(\%K=\dfrac{39.2}{138}.100\%=56,52\%\)
\(\%C=\dfrac{12}{138}.100\%=8,69\%\)
\(\%O=100\%-56,52\%-8,69\%=34,79\%\)
Còn lại cậu làm tương tự nhá
Bài 2 :
\(M_S=\dfrac{64.50\%}{100\%}=32\left(g\right)\)
\(n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(M_O=64-32=32\left(g\right)\\ n_O=\dfrac{32}{16}=2\left(mol\right)\)
\(=>CTHH:SO_2\)
Hãy lập công thức phân tử của khí hydrogen sulfide, biết lưu huỳnh trong hợp chất này có hóa trị II. Tính thành phần phần trăm về khối lượng của lưu huỳnh và của hydrogen trong hợp chất đó.
Gọi ct chung: \(H^I_xS^{II}_y\)
Theo qui tắc hóa trị: `I.x = II.y =>`\(\dfrac{x}{y}=\dfrac{II}{I}\)
`-> x=2, y=1`
`-> CTHH: H_2S`
\(K.L.P.T_{H_2S}=1.2+32=34< amu>.\)
\(\%H=\dfrac{1.2.100}{34}\approx5,88\%\)
`%S = 100%-5,88% =94,12%`
Câu 25: a) Hợp chất X chứa 94,12% lưu huỳnh, còn lại là hiđro. Hãy lập công thức hoá học của
hợp chất trên và cho biết ý nghĩa của công thức hoá học đó.
b) Hợp chất Y có thành phần phần trăm theo khối lượng các nguyên tố lần lượt là: 28% Na, 33%Al
và 39%O. Xác định công thức hoá học của hợp chất Y.
a) CTHH: \(H_xS\)
Ta có : \(\dfrac{32}{x+32}=94,12\%\Rightarrow x=2\)
=> CTHH: \(H_2S\)
Ý nghĩa : hợp chất được tạo từ 2 nguyên tố H, S
Trong 1 phân tử chất có 1 nguyên tử H và 2 nguyên tử S
Phân tử khối của hợp chất là 2 + 32 = 34 đvC
b) Gọi CTHH của hợp chất là \(Na_xAl_yO_z\)
Ta có : \(x:y:z=\dfrac{28}{23}:\dfrac{33}{27}:\dfrac{39}{16}=1:1:2\)
Vậy CTHH của hợp chất là \(NaAlO_2\)
Câu 21. Trong hợp chất của lưu huỳnh hàm lượng lưu huỳnh chiếm 50% . Hợp chất đó có công thức là:
a.SO3 b. H2SO4 c. CuS. d. SO2.
Câu 22. Đốt hoàn toàn 6,72 gam than trong không khí. Thể tích CO2 thu được ở đktc là :
a. 12,445 lít b. 125,44 lít c. 12,544 lít d. 12,454 lít.
Câu 23: Trong những oxit sau. Những oxit nào tác dụng được với dung dịch bazơ?
a. CaO, CO2 Fe2O3 . b. K2O, Fe2O3, CaO
c. K2O, SO3, CaO d. CO2, P2O5, SO2
Câu 24: Khí lưu huỳnh đioxit SO2 được tạo thành từ cặp chất nào sau đây?
a. K2SO4 và HCl. b. K2SO4 và NaCl.
c. Na2SO4 và CuCl2 d.Na2SO3 và H2SO4
Câu 25. Để nhận biết 2 lọ mất nhãn H2SO4 và Na2SO4, ta sử dụng thuốc thử nào sau đây:
a. HCl b. Giấy quỳ tím c. NaOH d.BaCl2
Câu 26: Dung dịch H2SO4 có thể tác dụng được những dãy chất nào sau đây?
a. CO2, Mg, KOH. b. Mg, Na2O, Fe2(OH)3
c. SO2, Na2SO4, Cu(OH)2 d. Zn, HCl, CuO.
Câu 27: Hòa tan 2,4gam oxit của kim loại hoá trị II vào 21,9gam dung dịch HCl 10% thì vừa đủ. Oxit đó là oxit nào sau đây:
a. CuO b. CaO c. MgO d. FeO
Câu 28: Cho dung dịch BaCl2 vào dung dịch H2SO4. Sau phản ứng có hiện tượng kết tủa:
a. Màu xanh b. Màu đỏ c. Màu vàng d.Màu trắng.
Câu29: Dãy chất nào sau đây gồm toàn oxit bazơ :
a. canxioxit; lưu huỳnhđioxit; sắt(III)oxit. b. kalioxit; magiêoxit; sắt từ oxit.
c. Silicoxit; chì(II)oxit; cacbon oxit. d. kalioxit; natrioxit; nitơoxit.
![]() Câu 30: Cho phương trình phản ứng sau: 2NaOH + X 2Y + H2O. X, Y lần lượt là:
Câu 30: Cho phương trình phản ứng sau: 2NaOH + X 2Y + H2O. X, Y lần lượt là:
a. H2SO4; Na2SO4 . b. N2O5 ; NaNO3.
c. HCl ; NaCl . d. (A) và (B) đều đúng.
Câu 31: Để loại bỏ khí CO2 có lẫn trong hỗn hợp ( O2; CO2). Người ta cho hỗn hợpđi qua dung dịch chứa:
a. HCl b. Na2SO4 c. NaCl d. Ca(OH)2 .
Câu 32: Các nguyên tố hóa học dưới đây, nguyên tố nào có oxit, oxit này tác dụng với nước, tạo ra dung dịch có PH > 7 a. Mg b. Cu c. Na d. S
Câu 33: Dung dịch của chất X có PH >7 và khi tác dụng với dung dịch kalisunfat tạo ra chất không tan. Chất X là. a. BaCl2 b. NaOH c. Ba(OH)2 d. H2SO4 .
Câu 34: Để thu được 5,6 tấn vôi sống với hiệu suất đạt 95% thì lượng CaCO3 cần là:
a. 10 tấn b. 9,5 tấn c. 10,526 tấn d. 111,11 tấn .
Câu 35: Nhỏ một giọt quỳ tím vào dung dịch NaOH, dung dịch có màu xanh; nhỏ từ từ dung dịch HCl cho tới dư, vào dung dịch có màu xanh trên thì.
a. Màu xanh vẫn không thay đổi. b. Màu xanh nhạt dần rồi mất hẳn.
c. Màu xanh nhạt dần rồi mất hẳn, rồi chuyển sanh màu đỏ d. Màu xanh đậm thêm dần.
Câu 36. Có hai lọ đựng dung dịch bazơ NaOH và Ca(OH)2. Dùng các chất nào sau đây để phân biệt hai chất trên: a. Na2CO3 b. NaCl c. MgO d. HCl .
Câu 37: Những cặp chất nào sau đây cũng tồn tại trong một dung dịch.
a. KCl và NaNO3. b. KOH và HCl
c. Na3PO4 và CaCl2 d. HBr và AgNO3.
Câu 38: Có những chất khí sau: CO2; H2; O2; SO2; CO. Khi nào làm đục nước vôi trong .
a. CO2 b. CO2; CO; H2 c. CO2 ; SO2 d. CO2; CO; O2 Câu 39: Hòa tan hoàn toàn 1,44g kim loại hóa trị II bằng 250ml dung dịch H2SO4 0,3M. Để truing hòa lượng axit dư cần dùng 60ml dung dịch NaOH 0,5M. Đó là kim loại gì ?
a. Ca b. Mg c. Zn d. Ba.
Câu 40.Phản ứng nào sau đây xảy ra trong quá trình sản xuất lưu huỳnh đioxit trong công nghiệp?
a/ S + O2 àSO2 b/CaO + H2O à Ca(OH)2
c/ 4FeS2 + 11O2 à 4Fe2O3 + 8SO2 d/ cả a và c
21. D
22. C
23. D
24. D
25. B
26. B
27. A
28. D
29. C
Câu 21. Trong hợp chất của lưu huỳnh hàm lượng lưu huỳnh chiếm 50% . Hợp chất đó có công thức là:
a.SO3 b. H2SO4 c. CuS. d. SO2.
Câu 22. Đốt hoàn toàn 6,72 gam than trong không khí. Thể tích CO2 thu được ở đktc là :
a. 12,445 lít b. 125,44 lít c. 12,544 lít d. 12,454 lít.
Câu 23: Trong những oxit sau. Những oxit nào tác dụng được với dung dịch bazơ?
a. CaO, CO2 Fe2O3 . b. K2O, Fe2O3, CaO
c. K2O, SO3, CaO d. CO2, P2O5, SO2
Câu 24: Khí lưu huỳnh đioxit SO2 được tạo thành từ cặp chất nào sau đây?
a. K2SO4 và HCl. b. K2SO4 và NaCl.
c. Na2SO4 và CuCl2 d.Na2SO3 và H2SO4
Câu 25. Để nhận biết 2 lọ mất nhãn H2SO4 và Na2SO4, ta sử dụng thuốc thử nào sau đây:
a. HCl b. Giấy quỳ tím c. NaOH d.BaCl2
Câu 26: Dung dịch H2SO4 có thể tác dụng được những dãy chất nào sau đây?
a. CO2, Mg, KOH. b. Mg, Na2O, Fe(OH)3
c. SO2, Na2SO4, Cu(OH)2 d. Zn, HCl, CuO.
Câu 27: Hòa tan 2,4gam oxit của kim loại hoá trị II vào 21,9gam dung dịch HCl 10% thì vừa đủ. Oxit đó là oxit nào sau đây:
a. CuO b. CaO c. MgO d. FeO
Câu 28: Cho dung dịch BaCl2 vào dung dịch H2SO4. Sau phản ứng có hiện tượng kết tủa:
a. Màu xanh b. Màu đỏ c. Màu vàng d.Màu trắng.
Câu29: Dãy chất nào sau đây gồm toàn oxit bazơ :
a. canxioxit; lưu huỳnhđioxit; sắt(III)oxit. b. kalioxit; magiêoxit; sắt từ oxit.
c. Silicoxit; chì(II)oxit; cacbon oxit. d. kalioxit; natrioxit; nitơoxit.
Câu 30: Cho phương trình phản ứng sau: 2NaOH + X 2Y + H2O. X, Y lần lượt là:
a. H2SO4; Na2SO4 . b. N2O5 ; NaNO3.
c. HCl ; NaCl . d. (A) và (B) đều đúng.
Câu 31: Để loại bỏ khí CO2 có lẫn trong hỗn hợp ( O2; CO2). Người ta cho hỗn hợpđi qua dung dịch chứa:
a. HCl b. Na2SO4 c. NaCl d. Ca(OH)2 .
Câu 32: Các nguyên tố hóa học dưới đây, nguyên tố nào có oxit, oxit này tác dụng với nước, tạo ra dung dịch có PH > 7 a. Mg b. Cu c. Na d. S
Câu 33: Dung dịch của chất X có PH >7 và khi tác dụng với dung dịch kalisunfat tạo ra chất không tan. Chất X là. a. BaCl2 b. NaOH c. Ba(OH)2 d. H2SO4 .
Câu 34: Để thu được 5,6 tấn vôi sống với hiệu suất đạt 95% thì lượng CaCO3 cần là:
a. 10 tấn b. 9,5 tấn c. 10,526 tấn d. 111,11 tấn .
Câu 35: Nhỏ một giọt quỳ tím vào dung dịch NaOH, dung dịch có màu xanh; nhỏ từ từ dung dịch HCl cho tới dư, vào dung dịch có màu xanh trên thì.
a. Màu xanh vẫn không thay đổi. b. Màu xanh nhạt dần rồi mất hẳn.
c. Màu xanh nhạt dần rồi mất hẳn, rồi chuyển sanh màu đỏ d. Màu xanh đậm thêm dần.
Câu 36. Có hai lọ đựng dung dịch bazơ NaOH và Ca(OH)2. Dùng các chất nào sau đây để phân biệt hai chất trên: a. Na2CO3 b. NaCl c. MgO d. HCl .
Câu 37: Những cặp chất nào sau đây cũng tồn tại trong một dung dịch.
a. KCl và NaNO3. b. KOH và HCl
c. Na3PO4 và CaCl2 d. HBr và AgNO3.
Câu 38: Có những chất khí sau: CO2; H2; O2; SO2; CO. Khi nào làm đục nước vôi trong .
a. CO2 b. CO2; CO; H2 c. CO2 ; SO2 d. CO2; CO; O2
Câu 39: Hòa tan hoàn toàn 1,44g kim loại hóa trị II bằng 250ml dung dịch H2SO4 0,3M. Để truing hòa lượng axit dư cần dùng 60ml dung dịch NaOH 0,5M. Đó là kim loại gì ?
a. Ca b. Mg c. Zn d. Ba.
Câu 40.Phản ứng nào sau đây xảy ra trong quá trình sản xuất lưu huỳnh đioxit trong công nghiệp?
a/ S + O2 àSO2 b/CaO + H2O à Ca(OH)2
c/ 4FeS2 + 11O2 à 4Fe2O3 + 8SO2 d/ cả a và c
Câu 25: a) Hợp chất X chứa 94,12% lưu huỳnh, còn lại là hiđro. Hãy lập công thức hoá học của hợp chất trên và cho biết ý nghĩa của công thức hoá học đó.
b) Hợp chất Y có thành phần phần trăm theo khối lượng các nguyên tố lần lượt là: 28% Na, 33%Al và 39%O. Xác định công thức hoá học của hợp chất Y.
a) CTHH: HxS
Ta có : =94,12%⇒x=2
=> CTHH: H2S
Ý nghĩa : hợp chất được tạo từ 2 nguyên tố H, S
Trong 1 phân tử chất có 1 nguyên tử H và 2 nguyên tử S
Phân tử khối của hợp chất là 2 + 32 = 34 đvC
b) Gọi CTHH của hợp chất là NaxAlyOz
Ta có :
a, Hợp chất A được tạo bởi nguyên tố lưu huỳnh và nguyên tố oxi. Tỉ khối của A so với Hidro là 32. Tìm công thức hóa học của A biết trong A, lưu huỳnh chiếm 50%.
b, Chất khí A có thành phần nguyên tố là: 5,88%H; 94,12% S. Khí A nặng hơn khí hidro 17 lần. Công thức hóa học của hợp chất đó là ?
a) MA = 32.2 = 64(g/mol)
\(m_S=\dfrac{64.50}{100}=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=64-32=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> CTHH: SO2
b) MA = 2.17 = 34 (g/mol)
\(m_H=\dfrac{34.5,88}{100}=2\left(g\right)=>n_H=\dfrac{2}{1}=2\left(mol\right)\)
\(m_S=34-2=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
=> CTHH: H2S
Thực nghiệm cho biết nguyên tố natri chiếm 59% về khối lượng trong hợp chất với nguyên tố lưu huỳnh. Viết công thức hóa học và tính phân tử khối của hợp chất.
Gọi công thức của hợp chất là N a x S y .
Theo đề bài, ta có:
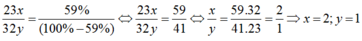
Vậy công thức của hợp chất là: N a 2 S .
Phân tử khối: 2 . 23 + 32 = 78đvC.
một hợp chất của lưu huỳnh và oxi có thành phần khối lượng là 50% lưu huỳnh vào 50% oxi. Vậy Công thức hóa học là
Gọi số nguyên tử lưu huỳnh trong phân tử hợp chất là x (nguyên tử), số nguyên tử oxi là y (nguyên tử). ĐK: \(x;y\in \mathbb N^*\)
Ta có:
\(\left\{{}\begin{matrix}\dfrac{32x}{32x+16y}\cdot100=50\\\dfrac{16y}{32x+16y}\cdot100=50\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=1\\y=2\end{matrix}\right.\) (TMĐK)
Vậy công thức hoá học của hợp chất đã cho là SO2.