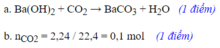Hoà tan 6,2g Na2O vào 2 lít nước . Tính nồng độ mol của dung dịch thu được

Những câu hỏi liên quan
Hòa tan 7,8 gam một kim loại R vào nước thu được 100ml dung dịch D và 2,24 lít H2 (đktc). Vậy R và nồng độ mol của dung dịch D là:
A. Na và 1M.
B. K và 2M.
C. K và 1M.
D. K và 1,5M.
Đáp án B
Số mol H2 = 0,1 mol
Phương trình phản ứng:
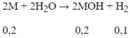
Tính được M = m : n = 7,8 : 0,2 = 39. Vậy kim loại cần tìm là K.
C M = 0 , 2 0 , 1 = 2 M
Đúng 0
Bình luận (0)
Hấp thụ hoàn toàn 3,36 lít CO2 (đktc) vào 125 ml dung dịch Ba(OH)2 1M, thu được dung dịch X. Coi thể tích dung dịch không thay đổi, nồng độ mol của chất tan trong dung dịch X là:
A. 0,4M
B. 0,2M
C. 0,6M
D. 0,1M
Đáp án B
Ta có: nCO2= 0,15 mol; nBa(OH)2= 0,125 mol; nOH-= 0,25 mol
Ta thấy 1 < n OH - n CO 2 = 0 , 25 1 , 5 = 1,67 < 2 à tạo ra 2 muối.
PTPỨ:
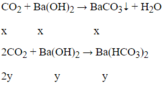
Ta có hệ
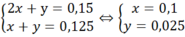
![]()
Đúng 0
Bình luận (0)
Biết 2,24 lít khí Cacbonic (đktc) tác dụng hết với 200 ml dung dịch
B
a
(
O
H
)
2
, sản phẩm thu được là muối trung hòa và nước.a. Viết phương trình xảy ra.b. Tính nồng độ mol của dung dịch
B
a
(
O
H
)
2
cần dùng.c. Tính khối lượng kết tủa...
Đọc tiếp
Biết 2,24 lít khí Cacbonic (đktc) tác dụng hết với 200 ml dung dịch B a ( O H ) 2 , sản phẩm thu được là muối trung hòa và nước.
a. Viết phương trình xảy ra.
b. Tính nồng độ mol của dung dịch B a ( O H ) 2 cần dùng.
c. Tính khối lượng kết tủa thu được
giúp mình câu này được không ạ , mình cần gấp lắm,chiều thi rồi Hoà tan 3,1 gam Na2O VÀO cố nước chứa 46,9 gam nước a) Tính nồng độ phần trăm dung dịch thu được b)Tính nồng độ mol của dung dịch. Biết sự hoà tan chất rắn vào nước thì thể tích thay đổi không đang kể ( D H2O = 1G/ML )
md d =mct + mdm =3,1+46,9=50(gam)
=> \(C\%=\dfrac{m_{ct}.100\%}{m_{dd}}=\dfrac{3,1.100}{50}=6,2\left(\%\right)\)
b) Vì Dnước=1g/mol nên mnước=Vnước
Theo bài ,sự hòa tan chất rắn vào nước thay đổi không đáng kể nên Vd d=Vnước=46,9(lít)
nd d=\(\dfrac{m_{dd}}{M_{dd}}=\dfrac{50}{40}=1,25\left(mol\right)\)
=> \(C_M=\dfrac{n}{V}=\dfrac{1,25}{46,9}\approx0,03\left(M\right)\)
Bạn kiểm tra lại giùm mình đi ,sai chỗ nào thì nhận xét giùm mình nhé
Đúng 0
Bình luận (6)
a)
Na2O + H2O \(\rightarrow\) 2NaOH
Ta có :
nNa2O = 0,05(mol)
nH2O = 2,6(mol)
Ta thấy : 0,05 : 1 < 2,6 : 1
=> Na2O hết
=>nNaOH = 0,05 . 2 = 0,1(mol)
=> mNaOH = 0,1 . 40 = 4(g)
Khối lượng dung dịch thu được là :
3,1 + 46,9 = 50(g)
=> C% = 4 . 100 : 50 = 8%
Vậy nồng độ phần trăm thu được là 8%
b)
Ta có :
Vì sự hòa tan chất rắn vào nước thì thể tích thay đổi không đáng kể
=> Vdd = 3,1 + 46,9 = 50(ml)
=> CM = 0,05 : 50 = 0,001(M)
Đúng 0
Bình luận (1)
hào tan 10g KNO3 vào 150g nước. Tính nồng độ % của dung dịch
\(C\%_{dd}=\dfrac{10}{10+150}.100\%=6,25\%\)
Đúng 0
Bình luận (0)
Hấp thụ hoàn toàn 2,688 lít CO2 (đktc) vào 2,5 lít dung dịch Ba(OH)2 có nồng độ a mol/l, thu được 15,76 gam kết tủa. Giá trị của a là:
A. 0,032
B. 0,048
C. 0,06
D. 0,04
Đáp án D
Ta có: nCO2 = 2,688/22,4 = 0,12 mol;
nBaCO3 = 11,82/197 = 0,06 mol
Do n CO 2 ≠ n BaCO 3 nên ngoài BaCO3 còn có Ba(HCO3)2 được tạo thành.
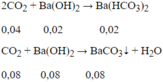
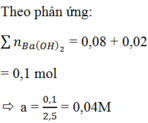
Đúng 0
Bình luận (0)
Cho m gam kim loại gồm Fe tác dụng vừa đủ với 600 ml dung dịch HCl, thu được 13,44 lít khí H2 (ở đktc)
a) Xác định giá trị m và khối lượng muối thu được sau phản ứng
b) Tính nồng độ mol/lít của dung dịch HCl đã dùng
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,6 1,2 0,6 0,6 ( mol )
\(m_{Fe}=0,6.56=33,6g\)
\(m_{FeCl_2}=0,6.127=76,2g\)
\(C_{M_{HCl}}=\dfrac{1,2}{0,6}=2M\)
Đúng 2
Bình luận (2)
Cho m gam kim loại gồm Fe tác dụng vừa đủ với 300 ml dung dịch HCl, thu được 6,72 lít khí H2 (ở đktc)
a) Xác định giá trị m và khối lượng muối thu được sau phản ứng
b) Tính nồng độ mol/lít của dung dịch HCl đã dùng
`Fe + 2HCl -> FeCl_2 + H_2↑`
`0,3` `0,6` `0,3` `0,3` `(mol)`
`n_[H_2] = [ 6,72 ] / [ 22,4 ] = 0,3 (mol)`
`-> m_[Fe] = 0,3 . 56 = 16,8 (g)`
`-> m_[FeCl_2] = 0,3 . 127 = 38,1 (g)`
`b) C_[M_[HCl]] = [ 0,6 ] / [ 0,3 ] = 2 (M)`
Đúng 2
Bình luận (0)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
0,3<---0,6<------0,3<-----0,3
=> \(\left\{{}\begin{matrix}m_{Fe}=0,3.56=16,8\left(g\right)\\m_{FeCl_2}=127.0,3=38,1\left(g\right)\\C_{M\left(HCl\right)}=\dfrac{0,6}{0,3}=2M\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Trộn 2 lít dung dịch đường 0,5M với 3 lít dung dịch đường 1M. Tính nồng độ mol của dung dịch sau khi trộn.
ndd đường = 2*0,5=1mol
ndd đường = 3*1=3mol
tổng ndd đường = 1+3=4mol
tổng vdd đường =2+3=5 l
CM=4/5=0,8 M
Đúng 0
Bình luận (0)
CM = ( 2 * 0.5 + 3 * 1 ) / ( 2 + 3 ) = 0.8 (M)
Đúng 0
Bình luận (1)
CM = ( 2 * 0.5 + 3 * 1 ) / ( 2 + 3 ) = 0.8 (M)
Đúng 0
Bình luận (0)