Cho 20.5g hỗn hợp Cu và Zn vào dung dịch H2SO4 loãng.Sau phản ứng thấy có 2.24l khí không màu thoát ra(ở đktc)
a.Tính khối lượng của kim loại ban đầu trước khi phản ứng
b.chất rắn còn lại sau khi phản ứng với H2SO4
Cho 18.7g hỗn hợp X gồm Mg, Cu, Fe vào dung dịch HCl dư , sau khi phản ứng xảy ra hoàn toàn thì được dung dịch Y, còn lại 0.3g chất rắn không tan và thấy thoát ra 11.2 lít khí.
a) TÍnh khối lượng mỗi kim loại trong hỗn hợp X ban đầu?
b) Đem 0.3g chất rắn không tan sau phản ứng cho tác dụng với H2SO4 đặc nóng (vừa đủ) thì thoát ra V lít khí. Tính V?
a) Theo đề bài: \(m_{Cu}=0,3\left(g\right)\)
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
a______2a______a_____a (mol)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
b_____2b______b____b (mol)
Ta lập được hệ phươn trình: \(\left\{{}\begin{matrix}24a+56b=18,7-0,3=18,4\\a+b=\dfrac{11,2}{22,4}=0,5\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,3\\b=0,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,3\cdot24=7,2\left(g\right)\\m_{Fe}=0,2\cdot56=11,2\left(g\right)\end{matrix}\right.\)
b) PTHH: \(Cu+2H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}CuSO_4+SO_2+2H_2O\)
Ta có: \(n_{Cu}=\dfrac{0,3}{64}=\dfrac{3}{640}\left(mol\right)=n_{SO_2}\) \(\Rightarrow V_{SO_2}=\dfrac{3}{640}\cdot22,4=0,105\left(l\right)\)
a)
Gọi $n_{Mg} = a(mol) ; n_{Fe} = b(mol)$
$Mg + 2HCl \to MgCl_2 + H_2$
$Fe + 2HCl \to FeCl_2 + H_2$
$n_{H_2} = a + b = \dfrac{11,2}{22,4} = 0,5(mol)$
$m_X = 24a + 56b = 0,3 = 18,7(gam)$
Suy ra a = 0,3 ; b = 0,2
$m_{Mg} = 0,3.24 = 7,2(gam)$
$m_{Fe} = 0,2.56 = 11,2(gam)$
b)
$Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + H_2O$
$n_{SO_2} = n_{Cu} = \dfrac{0,3}{64}$
$V = \dfrac{0,3}{64}.22,4 = 0,105(lít)$
Cho 25 (gam) hỗn hợp gồm Nhôm và Đồng vào dung dịch H2SO4 loãng dư, sau phản ứng thấy thoát ra 5,6 (lít) khí H2 (ở đktc). Tính khối lượng mỗi kim loại có trong hỗn hợp ban đầu.
nH2 = 5.6/22.4 = 0.25 (mol)
2Al + 3H2SO4 => Al2(SO4)3 + 3H2
1/6............................................0.25
mAl = 1/6 * 27 = 4.5 (g)
mCu = 25 - 4.5 = 20.5 (g)
Cho hỗn hợp X gồm 3 kim loại: Fe; Zn và Cu.
+ TN1: Cho 4,74 gam X phản ứng hoàn toàn trong H 2 S O 4 loãng thấy thoát ra 1,568 lít khí ở đktc.
+ TN2: Cho 0,16 mol X phản ứng với H 2 S O 4 đặc, nóng, dư thấy thoát ra 4,704 lít khí S O 2 là sản phẩm khử duy nhất ở đktc.
Xác định % khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Cho 10,5g hỗn hợp 2 kim loại Cu; Zn vào dung dịch H2SO4 20%; người ta thu được 2,24l khí (đktc).
a. Viết PTHH.
b. Tính khối lượng chất rắn còn lại sau phản ứng.
c, Tính khối lượng dung dịch H2SO4 thu được sau phản ứng.
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
a. PTHH:
\(Zn+H_2SO_4--->ZnSO_4+H_2\)
\(Cu+H_2SO_4--\times-->\)
b. Theo PT: \(n_{Zn}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,1.65=6,5\left(g\right)\)
\(\Rightarrow m_{chất.rắn.còn.lại.sau.PỨ}=m_{Cu}=10,5-6,5=4\left(g\right)\)
c. Theo PT: \(n_{H_2SO_4}=n_{Zn}=0,1\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,1.98=9,8\left(g\right)\)
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{9,8}{m_{dd_{H_2SO_4}}}.100\%=20\%\)
\(\Leftrightarrow m_{dd_{H_2SO_4}}=49\left(g\right)\)
\(a,PTHH:Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ b,m_{\text{chất rắn sau p/ứ}}=m_{Cu}\\ n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ \Rightarrow n_{Zn}=0,1\left(mol\right)\\ \Rightarrow m_{Zn}=0,1\cdot65=6,5\left(g\right)\\ \Rightarrow m_{Cu}=10,5-6,5=4\left(g\right)\\ c,n_{H_2SO_4}=0,1\left(mol\right)\\ \Rightarrow m_{CT_{H_2SO_4}}=0,1\cdot98=9,8\left(g\right)\\ \Rightarrow m_{dd_{H_2SO_4}}=\dfrac{9,8\cdot100\%}{20\%}=49\left(g\right)\)
Cho 8,64 gam Mg vào dung dịch hỗn hợp NaNO3 và H2SO4, đun nhẹ hỗn hợp phản ứng, lúc đầu tạo ra sản phẩm khử là khí NO, sau đó thấy thoát ra khí không màu X. Sau khi các phản ứng kết thúc thấy còn lại 4,08 gam chất rắn không tan. Biết rằng tổng thể tích của hai khí NO và X là 1,792 lít (đktc) và tổng khối lượng là 1,84 gam. Cô cạn cẩn thận dung dịch sau phản ứng thu được m gam chất muối khan. Giá trị nào sau đây gần với m nhất?
A. 29,60 gam
B. 36,25 gam
C. 28,70 gam
D. 31,52 gam
Đáp án A
mMg pư = 8,64 – 4,08 = 4,56 (g) => nMg pư = 0,19 (mol) => ne (Mg nhường) = 0,38 (mol)
nX = 0,08 (mol) => MX = 1,84: 0,08 = 23(g/mol) => khí X là H2
Gọi nNO = a (mol); nH2 = b (mol)
∑ nX = a + b = 0,08 (1)
∑ mX = 30a + 2b = 1,84 (2)
Từ (1) và (2) => a = 0,06 ; b = 0,02
=> ∑ ne (nhận) = 3nNO + 2nH2 = 0,06.3 + 0,02.2 = 0,22 < ne (Mg nhường) = 0,38
=> tạo muối NH4+
Bảo toàn electron => 2nMg pư = 3nNO + 2nH2 + 8nNH4+
=> nNH4+ = (2nMg pư - 3nNO - 2nH2)/8 = 0,02 (mol)
BTNT N => nNO3- = nNO + nNH4+ = 0,06 + 0,02 = 0,08 (mol) => nNa+ = 0,08 (mol)
=> mmuối = mMgSO4 + m(NH4)2SO4 + mNa2SO4
= 0,19. 120 + 132. 0,01 + 0,04. 142
= 29,8 (g) ≈ 29,6 (g)
Nung nóng 3,72g hỗn hợp bột các kim loại Zn và Fe trong bột S dư. Chất rắn thu được sau phản ứng được hòa tan hoàn toàn bằng dung dịch H2SO4 loãng, nhận thấy có 1,344 lít khí (đktc) thoát ra. Xác định khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Đặt nZn = x mol; nFe = y mol.
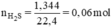
Ta có hệ phương trình: 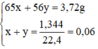
Giải hệ phương trình trên ta được:
x = 0,04 mol, y = 0,02 mol.
mZn = 65 × 0,04 = 2,6g
mFe = 56 × 0,02 = 1,12g
Hòa tan hỗn hợp X gồm Cu và Fe2O3 trong 400 ml dung dịch HCl a (M) thu được dung dịch Y và còn lại 1,0 gam Cu không tan. Nhúng thanh Mg vào dung dịch Y, sau khi phản ứng hoàn toàn nhấc thanh Mg ra thấy khối lượng tăng thêm 4,0 gam so với khối lượng thanh Mg ban đầu và có 1,12 lít khí H2 (đo ở đktc) thoát ra (giả thiết toàn bộ lượng kim loại thoát ra đều bám hết vào thanh Mg). Khối lượng Cu va a?
Vì còn Cu nên chứng tỏ Fe+3 đã bị chuyển hết thành Fe+2 rồi.
gọi x là số mol Cu+2 và 2x là số mol Fe+2
Ta dùng phương pháp tăng giảm KL
64x + 56.2x - 24.3x = m tăng
m tăng = 4 + 0,05.24 ( một phần bị axit hòa tan ) suy ra x = 0,05
Vậy khối lượng Cu ban đầu là
1 + 0,05 .64 = 4,2 g
Số Mol axit bằng
3x.2 + 2.nH2 = 0,4 mol
Cho 10,5g hỗn hợp 2 kim loại Cu, Zn vào dung dịch H2SO4 loãng dư, người ta thu được 2,24 lít khí (đktc). Tính khối lượng chất rắn còn lại sau phản ứng.
A. 3g
B. 4g
C. 5g
D. 6g
Z n + H 2 S O 4 → Z n S O 4 + H 2
Cu không tác dụng với axit Sunfuric.
⇒ n Z n = n H 2 = 2,24/22,4 = 0,1 mol
⇒ m Z n = 0,1.65 = 6,5g
⇒ m C u = m r a n c o n l a i = 10,5 - 6,5 =4g
⇒ Chọn B.
Hoà tan hỗn hợp X gồm Cu và Fe2O3 trong 400 ml dung dịch HCl a mol/lít được dung dịch Y và còn lại 1 gam đồng không tan. Nhúng thanh Mg vào dung dịch Y, sau khi phản ứng xong, nhấc thanh Mg ra thấy khối lượng tăng 4 gam so với ban đầu và có 1,12 lít khí H2 (đktc) bay ra.(Giả thiết toàn bộ lượng kim loại thoát ra đều bám vào thanh Mg). Khối lượng của Cu trong X và giá trị của a là:
A. 4,2g và a = 1M.
B. 4,8g và 2M.
C. 1,0g và a = 1M
D. 3,2g và 2M.