Cho 10,6 g hỗn hợp hai kim loại kiềm thuộc hai chu kì liên tiếp tác dụng với clo dư thu được 31,9 g hỗn hợp muối . Hai kim loại đó là

Những câu hỏi liên quan
Cho 5,4 g hỗn hợp hai kim loại kiềm thuộc hai chu kì liên tiếp tác dụng với clo dư thu được 15,95 g hỗn hợp muối . Hai kim loại đó là
Gọi nguyên tử khối trung bình của 2 kim loại kiềm thuộc 2 chu kì liên tiếp đó là R
\(BTNT\left(R\right):n_R=n_{RCl}\\ \Rightarrow\dfrac{5,4}{R}=\dfrac{15,95}{R+35,5}\\ \Rightarrow R=18,17\)
=> 2 kim loại cần tìm là Li và Na
Đúng 1
Bình luận (0)
Một hỗn hợp gồm hai kim loại kiềm thuộc hai chu kì liên tiếp nhau. Cho 12g hỗn hợp này tác dụng với nước dư thu được 4,48 lít khí H2 ở đktC. Hai kim loại đó là: A. Li, NA. B. Na, K. C. K, RB. D. Rb, Cs.
Đọc tiếp
Một hỗn hợp gồm hai kim loại kiềm thuộc hai chu kì liên tiếp nhau. Cho 12g hỗn hợp này tác dụng với nước dư thu được 4,48 lít khí H2 ở đktC. Hai kim loại đó là:
A. Li, NA.
B. Na, K.
C. K, RB.
D. Rb, Cs.
Gọi kí hiệu chung của hai kim loại kiềm là R ; nH2 = 4,48/22,4 = 0,2 mol
R + H2O → R OH + 1 2 H2
Đúng 0
Bình luận (0)
Một hỗn hợp gồm hai kim loại kiềm thuộc hai chu kì liên tiếp nhau. Cho 12g hỗn hợp này tác dụng với nước dư thu được 4,48 lít khí H2 ở đktC. Hai kim loại đó là: A. Li, Na B. Na, K C. K, Rb D. Rb, Cs
Đọc tiếp
Một hỗn hợp gồm hai kim loại kiềm thuộc hai chu kì liên tiếp nhau. Cho 12g hỗn hợp này tác dụng với nước dư thu được 4,48 lít khí H2 ở đktC. Hai kim loại đó là:
A. Li, Na
B. Na, K
C. K, Rb
D. Rb, Cs
Cho 9,1 gam hỗn hợp hai muối cacbonat của hai kim loại kiềm ở hai chu kì liên tiếp tác dụng hết với dung dịch HCl dư thu được 2,24 lít CO2 (đktc). Hai kim loại đó là A. Li, Na. B. Na, K. C. K, Rb. D. Rb, Cs.
Đọc tiếp
Cho 9,1 gam hỗn hợp hai muối cacbonat của hai kim loại kiềm ở hai chu kì liên tiếp tác dụng hết với dung dịch HCl dư thu được 2,24 lít CO2 (đktc). Hai kim loại đó là
A. Li, Na.
B. Na, K.
C. K, Rb.
D. Rb, Cs.
Đáp án A
Phân tử khối trung bình: 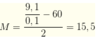
Vậy, 2 kim loại là Li và Na
Đúng 0
Bình luận (0)
Hỗn hợp 2 kim loại kiềm X,Y thuộc 2 chu kì liên tiếp và Zx>Zy.cho 10,6 (g) hỗn hợp tác dụng với Cl2 dư được 31,9 (g) hỗn hợp muối . tính khối lượng mỗi kim loại trong hỗn hợp
Ta có
mCl2=31,9-10,5=21,3(g)
---->n\(_{NaCl}=0,6\left(mol\right)\)
Mtb=\(\frac{10,6}{0,6}=\frac{53}{3}mol\)
Suy ra 2 KL đó là Li và Na , n\(_{Li}=0,2;n_{Na}=0,4\left(mol\right)\)
==> m\(_{Li}=1,4\left(g\right)\)
m\(_{Na}=9,2\left(g\right)\)
quy 2 kim loại kiềm cần tìm về ct chung là R
PTPU
2R+ Cl2\(\rightarrow\) 2RCl
adđlbtkl có
mkim loại+ mCl2= mmuối
\(\Rightarrow\) mCl2= 21,3( g)
\(\Rightarrow\) nR= 2nCl2= 0,6( mol)
\(\Rightarrow\) MR= 17,67( g/ mol)
\(\Rightarrow\) X là Na, Y là Li
gọi a; b lần lượt là số mol Na và Li trong hỗn hợp
ta có hpt: \(\left\{{}\begin{matrix}23a+7b=10,6\\58,5a+42,5b=31,9\end{matrix}\right.\)
\(\Rightarrow\) a= 0,4
b= 0,2
\(\Rightarrow\) mNa= 9,2( g)
mLi= 1,4( g)
\(mCl2=\text{31,9 - 10,6= 21,3g}\)
\(\Rightarrow nCl2=0,3\left(mol\right)\)
\(M+\frac{1}{2}Cl2\rightarrow MCl\)
\(\Rightarrow\text{Số mol KL= 0,6 mol}\)
\(\Rightarrow\text{Mtb(Kl)= 10,6÷ 0,6 = 17,6g/mol}\)
=>2 KL X, Y lần lượt là Na, Li
Số mol Na, Li lần lượt là x,y
Ta có hệ:
\(\Rightarrow\left\{{}\begin{matrix}\text{x + y =0,6}\\\text{23x + 7y = 10,6}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,4\\y=0,2\end{matrix}\right.\)
\(\)\(\Rightarrow\left\{{}\begin{matrix}mNa=9,2\\mLi=1,4\end{matrix}\right.\)
Cho 6,4 g hỗn hợp hai kim loại nhóm IIA, thuộc hai chu kì liên tiếp, tác dụng hết với dung dịch HCl dư thu được 4,48 lít khí hiđro (đktc). Các kim loại đó là
A. Be và Mg
B. Mg và Ca
C. Ca và Sr
D. Sr và Ba
Đáp án B
Áp dụng phương pháp khối lượng mol trung bình, ta có
M = ![]() = 32
= 32
24 = M1 < 32 < M2 = 40
Đúng 0
Bình luận (0)
Cho 6,4 g hỗn hợp hai kim loại nhóm IIA, thuộc hai chu kì liên tiếp, tác dụng hết với dung dịch HCl dư thu được 4,48 lít khí hiđro (đktc). Các kim loại đó là
A. Be và Mg
B. Mg và Ca
C. Ca và Sr
D. Sr và Ba
Đáp án B
Hướng dẫn Áp dụng phương pháp khối lượng mol trung bình, ta có
![]()
→ 24= M1 < 32 <M2 = 40
Đúng 0
Bình luận (0)
Hòa tan hòa toàn 6,645g hỗn hợp muối clorua của hai kim loại kiềm thuộc hai chu kì liên tiếp nhau vào nước được dd X. Cho toàn bộ dd X tác dụng hoàn toàn với dd AgNO3 (dư), thu được 18,655g kết tủa. Hai kim loại kiềm trên là A. Na, K B. Rb, Cs C. Li , Na D. K , Rb
Đọc tiếp
Hòa tan hòa toàn 6,645g hỗn hợp muối clorua của hai kim loại kiềm thuộc hai chu kì liên tiếp nhau vào nước được dd X. Cho toàn bộ dd X tác dụng hoàn toàn với dd AgNO3 (dư), thu được 18,655g kết tủa. Hai kim loại kiềm trên là
A. Na, K
B. Rb, Cs
C. Li , Na
D. K , Rb
Đáp án C
![]()
nAgCl = 18,655/143,5 = 0,13
⇒ M= 6,645/ 0,13 - 35,5 = 15,61
⇒ M1 = 9 (Li) < 15,61 < M2 = 23(Na)
Đúng 0
Bình luận (0)
Cho 7,83 gam một hỗn hợp gồm hai kim loại kiềm ở hai chu kì liên tiếp tác dụng với nước dư thu được 2,8 lít khí H2 (ở đktc). Hai kim loại đó là
Gọi A là công thức cung của 2 KL
\(n_{H_2}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\)
PTHH: 2A + 2H2O --> 2AOH + H2
_____0,25<----------------------0,125_____(mol)
=> \(M_A=\dfrac{7,83}{0,25}=31,32\left(g/mol\right)\)
Mà 2 KL ở 2 chu kì liên tiếp
=> 2 kim loại đó là Na(23) và K(39)
Đúng 2
Bình luận (0)
















