Cho 9,8 g hh mg zn vào 1 cốc chứa 430 ml dd h2so4 1M. Sau khi p/ứ hoàn toàn thêm tiếp vào cốc 1 lít dd Ba(oh)2 0,48 M, khuấy đều cho p/ứ hoàn toàn, lọc kết tủa nung đến m ko đổi thu đc 112,29 g chất rắn. Tính m kim loại trg hh ban đầu

Những câu hỏi liên quan
Cho 9,86 gam hỗn hợp gồm Mg và Zn vào một cốc chứa 430 ml dung dịch H2SO4 1M . Sau khi phảnứng hoàn toàn , thêm tiếp vào cốc 1 lít dung dịch Ba(OH)2 0,48M , khuấy đều cho phản ứng hoàn toàn ,lọc lấy kết tủa và nung đến khối lượng không đổi thì thu được 112,29 gam chất rắn . Viết các phươngtrình phản ứng xảy ra và tính khối lượng mỗi kim loại trong hỗn hợp ban đầu .
Đọc tiếp
Cho 9,86 gam hỗn hợp gồm Mg và Zn vào một cốc chứa 430 ml dung dịch H2SO4 1M . Sau khi phảnứng hoàn toàn , thêm tiếp vào cốc 1 lít dung dịch Ba(OH)2 0,48M , khuấy đều cho phản ứng hoàn toàn ,lọc lấy kết tủa và nung đến khối lượng không đổi thì thu được 112,29 gam chất rắn . Viết các phươngtrình phản ứng xảy ra và tính khối lượng mỗi kim loại trong hỗn hợp ban đầu .
tham khảo link bài làm
https://moon.vn/hoi-dap/cho-986-gam-hon-hop-gom-mg-va-zn-vao-mot-coc-chua-430-ml-dung-dich-h2so4-1m-sau-khi--330887
Đúng 0
Bình luận (2)
cho 8,4 gam hh a gồm al, mg vào cốc chứa 550 ml dd h2so4 1 m, sp thêm tiếp 500 ml dd B chứa ba(oh)2 0,4 m, naoh 1,6 m vào cốc. lọc kết tủa nung đến m ko đổi đc 57 gam cr khan. bt p/ứ xảy ra hoàn toàn. tính khối lượng mỗi chất
bạn đã có đáp án bài này chưa, nếu có cho mk xin vs
Đúng 0
Bình luận (0)
Cho 14,4g hỗ hợp gồm Mg và Fe vào 1 cốc chứa 430ml dung dịch H2SO4 1,5M loãng. Sau khi phản ứng hoàn toàn, thêm tiếp vào cốc 2 lít dung dịch hỗn hợp gồm Ba(OH)2 0,3225M khuấy đều cho phản ứng hoàn toàn, rồi lọc lấy kết tủa và nung nóng đến khối lượng không đổi thì thu được 167,625g chất rắn. Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu
Hh A gồm Zn và Fe. Cho 42,8g A vào 300g dd HCl 18,25% thu đc dd B và H2 . Cho tiếp 800ml dd KOH 2M vào B khuấy đều cho p/ứ hoàn toàn, lọc lấy kết tủa, đem nung ngoài không khí đến khối lượng k đổi thu đc 48,3g rắn C . Tính % khối lg các kim loại trong A . ai giải được có thể giải thích cho em biết tại sao hcl và koh lại dư được không ạ
Xem chi tiết
Biết chất dư, không dư thì cứ xét trường hợp. Ví dụ giả sử rồi tính mol theo giả sử, mol âm hoặc sai khác với ban đầu. Tìm hiểu trên mạng về cách biết chất dư, không dư nha.

Đúng 3
Bình luận (1)
Dung dịch X chứa H2SO4 0,4M với HCl 0,5M. Cho 6,85g hỗn hợp A gồm Mg và Zn vào 500ml dd X khuấy đều cho các phản ứng xảy ra hoàn toàn. Thêm tiếp dd Ba(OH)2 dư vào thu được kết tủa B, lọc lấy kết tủa B đem nung ở nhiệt độ cao đến khối lượng không đổi thu được 52,6g chất rắn. Biết rằng BaSO4 không bị nhiệt phân.
a. Viết phương trình phản ứng xảy ra.
b. Tính khối lượng các kim loại trong hỗn hợp A.
Đọc tiếp
Dung dịch X chứa H2SO4 0,4M với HCl 0,5M. Cho 6,85g hỗn hợp A gồm Mg và Zn vào 500ml dd X khuấy đều cho các phản ứng xảy ra hoàn toàn. Thêm tiếp dd Ba(OH)2 dư vào thu được kết tủa B, lọc lấy kết tủa B đem nung ở nhiệt độ cao đến khối lượng không đổi thu được 52,6g chất rắn. Biết rằng BaSO4 không bị nhiệt phân. a. Viết phương trình phản ứng xảy ra. b. Tính khối lượng các kim loại trong hỗn hợp A.
Ba(OH)2 dư => Zn(OH)2 tan hết , kết tủa chỉ là Mg(OH)2.
\(n_{Mg}=n_{MgO}=\dfrac{52.6}{40}=1.315\left(g\right)\)
\(m_{Mg}=1.315\cdot24=31.56\left(g\right)>m_{hh}\)
Đề sai !
Đúng 1
Bình luận (0)
a)H2SO4 + Zn --> ZnSO4 + H2
HCl + Zn --> ZnCl2 + H2
H2SO4 + Mg --> MgSO4 + H2
HCl + Mg --> MgCl2 + H2
Zn + H2O --> Zn(OH)2+ H2
Mg + H2O --> Mg(OH)2 + H2
Zn(OH)2 + Mg(OH)2 --> MgZnO2 + H2O
Đúng 1
Bình luận (0)
hòa tan hoàn toàn 19,56 g hỗn hợp gồm ba và kim loại R hóa trị 1 tác dụng đc vs nước thu đc dd A và 3,584 l h2
- cho 50 ml dung dịch na2so4 0,2 M vào cốc chứa 1/10 dd A thấy vẫn dư ba(oh)2 . thêm tiếp 15 ml dd na2so4 0,2 M vào cốc thì lại dư na2so4
xác định kim loại R??
(giúp mk vs , please !!!!)
Thêm 240 ml dung dịch NaOH 1M vào một cốc thuỷ tinh đựng 100 ml dung dịch
AlCl
3
nồng độ x mol/lít, khuấy đều đến phản ứng hoàn toàn, thấy trong cốc có 0,08 mol chất kết tủa. Thêm tiếp 100 ml dung dịch NaOH 1M vào cốc, khuấy đều đến phản ứng hoàn toàn thấy trong cốc có 0,06 mol chất kết tủa. Giá trị của x là : A. 0,75M B. 1M C. 0,5M D. 0,8M
Đọc tiếp
Thêm 240 ml dung dịch NaOH 1M vào một cốc thuỷ tinh đựng 100 ml dung dịch AlCl 3 nồng độ x mol/lít, khuấy đều đến phản ứng hoàn toàn, thấy trong cốc có 0,08 mol chất kết tủa. Thêm tiếp 100 ml dung dịch NaOH 1M vào cốc, khuấy đều đến phản ứng hoàn toàn thấy trong cốc có 0,06 mol chất kết tủa. Giá trị của x là :
A. 0,75M
B. 1M
C. 0,5M
D. 0,8M
Đáp án B
Bản chất phản ứng là : Cho 340 ml dung dịch NaOH 1M vào cốc thủy tinh đựng 100 ml dung dịch AlCl 3 nồng độ x mol/lít, tạo ra 0,06 mol kết tủa. Ta có :
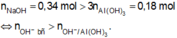
Suy ra đã có hiện tượng hòa tan kết tủa. Như vậy dung dịch sau phản ứng có chứa các ion Na + , Cl - và Al OH 4 - . Theo bảo toàn nguyên tố Cl, Al và bảo toàn điện tích, ta có :
![]()
![]()
Đúng 0
Bình luận (0)
1. Đốt cháy hoàn toàn m gam cacbon trong V lít khí oxi (đktc) thu được hỗn hợp khí A có tỉ khối đối với oxi là 1,25. Dẫn hh A vào bình chứa dd Ca(OH)2 dư tạo thành 6 gam kết tủa. Tính m và V.2. Cho m gam bột Cu vào 160ml dd AgNO3 1M, sau một thời gian thu được 9,73 gam hh chất rắn X và dd Y. Thêm 6,5 gam Zn vào dd Y đến khi phản ứng hoàn toàn thu được 14,02 g chất rắn Z. Tính m?
Đọc tiếp
1. Đốt cháy hoàn toàn m gam cacbon trong V lít khí oxi (đktc) thu được hỗn hợp khí A có tỉ khối đối với oxi là 1,25. Dẫn hh A vào bình chứa dd Ca(OH)2 dư tạo thành 6 gam kết tủa. Tính m và V.
2. Cho m gam bột Cu vào 160ml dd AgNO3 1M, sau một thời gian thu được 9,73 gam hh chất rắn X và dd Y. Thêm 6,5 gam Zn vào dd Y đến khi phản ứng hoàn toàn thu được 14,02 g chất rắn Z. Tính m?
Câu 1/
\(2C\left(\dfrac{m}{12}\right)+O_2\left(\dfrac{m}{24}\right)\rightarrow2CO_2\left(\dfrac{m}{12}\right)\)
\(CO_2\left(\dfrac{m}{12}\right)+Ca\left(OH\right)_2\rightarrow CaCO_3\left(\dfrac{m}{12}\right)+H_2O\)
Nếu như O2 thì tỷ khối của hỗn hợp so với O2 phải là: \(\dfrac{44}{32}=1,375>1,25\) vậy trong hỗn hợp khí phải có O2
\(n_C=\dfrac{m}{12}\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{V}{22,4}-\dfrac{m}{12}\left(mol\right)\)
\(\Rightarrow\dfrac{44.\dfrac{m}{12}+32.\left(\dfrac{V}{22,4}-\dfrac{m}{24}\right)}{\dfrac{m}{12}+\dfrac{V}{22,4}-\dfrac{m}{24}}=1,25.32=40\)
\(\Leftrightarrow15V-28m=0\left(1\right)\)
Ta lại có: \(n_{CaCO_3}=\dfrac{6}{100}=0,06\left(mol\right)\)
\(\Rightarrow\dfrac{m}{12}=0,06\Leftrightarrow m=0,72\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{{}\begin{matrix}15V-28m=0\\m=0,72\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}m=0,72\left(g\right)\\V=1,344\left(l\right)\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Thêm 240 ml dung dịch NaOH 1M vào một cốc thủy tinh đựng 100 ml dung dịch AlCl3 xM, khuấy đều đến khi phản ứng hoàn toàn thấy trong cốc có 0,08 mol chất kết tủa. Thêm tiếp 100 ml dung dịch NaOH 1M vào cốc, khuấy đều đến phản ứng hoàn toàn thấy trong cốc có 0,06 mol chất kết tủa. Nồng độ x là A. 0,75M. B. 1M. C. 0,5M. D. 0,8M.
Đọc tiếp
Thêm 240 ml dung dịch NaOH 1M vào một cốc thủy tinh đựng 100 ml dung dịch AlCl3 xM, khuấy đều đến khi phản ứng hoàn toàn thấy trong cốc có 0,08 mol chất kết tủa. Thêm tiếp 100 ml dung dịch NaOH 1M vào cốc, khuấy đều đến phản ứng hoàn toàn thấy trong cốc có 0,06 mol chất kết tủa. Nồng độ x là
A. 0,75M.
B. 1M.
C. 0,5M.
D. 0,8M.




















