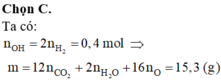Câu 1: Cho 0,557 gam (natri) Na tác dụng với H2O dư, thoát ra V lít khí, tính V.

Những câu hỏi liên quan
Cho m gam Fe tác dụng với dung dịch H2SO4 loãng tạo 1,792 lít khí.Cũng cho m gam Fe tác dụng với lượng dư HNO3 loãng thì thoát ra V lít khí (đktc) khí NO.Giá trị V là
\(\text{Fe+H2SO4=FeSO4+H2}\)
Ta có :
\(\text{nH2=1,792/22,4=0,08mol}\)
\(\text{=>nFe=0,08mol}\)
Khi cho 0,08mol Fe td với HNO3:
Quá trình nhường e: Fe=Fe+3 +3e
=> n e nhường=0,24mol
Theo ĐLBTe, ta có n e cho=n e nhận.
Quá trình nhận e: \(\text{N+5 +3e=>N+2}\)
\(\text{=> nN+2=0,24/3=0,08mol}\)
\(\text{=>nNO=0,08mol =>V NO=0,08.22,4=1,792l}\)
Fe+H2SO4--->FeSO4+H2
Fe+4HNO3---->Fe(NO3)3+NO+2H2O
n H2=0,08(mol)
Theo pthh1
n Fe =n H2 =0,08(mol)
m Fe=0,08.56=4,48(g)=m
Theo pthh2
n NO=n Fe=0,08(mol)
V NO= V=0,08.22,4=1,792(l)
PTHH:Fe+H2SO4->FeSO4+H2
mol:....1......1..............1..........1
mol:...0,08.....0,08.....0,08......0,08
nH2=1,792:22,4=0,08(mol)
m=0,08.56=4,48(g)
PTHH:Fe+4HNO3->2H2O+NO+Fe(NO3)3
mol:1...........4.............2........1..........1
mol:0,08......0,32......0,16.....0,08.....0,08
V\(_{NO}\)=0,08.22,4=1,792(l)
Xem thêm câu trả lời
Cho 3,36g kim loại X hóa trị(II) vào 250ml dung dịch H2SO4 loãng 0,3M, X tan hết và có 1,344 lít khí thoát ra ở đktc.
A) Tính số mol Axit dư
B) Xác định tên kim loại X
C) Cũng lượng kim loại X như trên, cho tác dụng với H2SO4 đặc nóng thu được chất khí có mùi xốc. Tính V t khí thoát ra ở đktc . Giúp em vs ạ!!!!
\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\) \(n_{H_2SO_4}=0,3.0,25=0,075\left(mol\right)\)
\(X+H_2SO_{4\left(l\right)}\rightarrow XSO_4+H_2\uparrow\)
0,06 0,06 0,06 0,06 (mol)
dư:0 0,015 0 0 (mol)
b/
m\(M_X=\dfrac{3,36}{0,06}=56\left(g\right)\)
\(\rightarrow Fe\)
c/
\(2Fe+6H_2SO_{4\left(đn\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
0,06 0,09 (mol)
V\(_{SO_2}=0,09.22,4=2,016\left(l\right)\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai ancol, thu được 13,44 lít CO2 (đktc) và 15,3 gam H2O. Mặt khác, cho m gam X tác dụng với Na (dư), thu được 4,48 lít khí H2 (đktc). Giá trị của m là A. 15,7 B. 12,9 C. 15,3. D. 12,3
Đọc tiếp
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai ancol, thu được 13,44 lít CO2 (đktc) và 15,3 gam H2O. Mặt khác, cho m gam X tác dụng với Na (dư), thu được 4,48 lít khí H2 (đktc). Giá trị của m là
A. 15,7
B. 12,9
C. 15,3.
D. 12,3
Hỗn hợp A gồm các kim loại Mg, Al, Fe.Lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch NaOH dư, sinh ra 3,36 lít khí (đktc). Mặt khác cũng lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch HCl dư, sinh ra 10,08 lít khí (đktc) và dung dịch B. Cho dung dịch B tác dụng với dung dịch NaOH dư, lọc kết tủa tạo thành và nung nóng trong không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m và tính % theo khối lượng của mỗi kim loại tron...
Đọc tiếp
Hỗn hợp A gồm các kim loại Mg, Al, Fe.
Lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch NaOH dư, sinh ra 3,36 lít khí (đktc). Mặt khác cũng lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch HCl dư, sinh ra 10,08 lít khí (đktc) và dung dịch B. Cho dung dịch B tác dụng với dung dịch NaOH dư, lọc kết tủa tạo thành và nung nóng trong không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m và tính % theo khối lượng của mỗi kim loại trong hỗn hợp A.Cho hỗn hợp A tác dụng với dung dịch CuSO4 dư, sau khi phản ứng kết thúc, lọc lấy chất rắn đem hòa tan hết chất rắn trong dung dịch HNO3 loãng dư, thu được 26,88 lít khí NO (đktc). Tính khối lượng hỗn hợp A.1.1. Al + NaOH + H2O ==> NaAlO2 + 3/2H2
nH2(1)=3,36/22,4=0.15(mol)
=> nAl(1)= nH2(1):3/2= 0.15:3/2= 0.1(mol)
2.Mg + 2HCl ==> MgCl2 + H2
3.2Al + 6HCl ==> 2AlCl3 + 3H2
4.Fe + 2HCl ==> FeCl2 + H2
=> \(n_{H_2\left(2,3,4\right)}=\) 10.08/22.4= 0.45(mol)
=> nH2(3)=0.1*3/2=0.15(mol)
MgCl2 + 2NaOH ==> Mg(OH)2 + 2NaCl
AlCl3 + 3NaOH ==> Al(OH)3 + 3NaCl
FeCl2 + 2NaOH ==> Fe(OH)2 + 2NaCl
Đúng 0
Bình luận (0)
Hỗn hợp A gồm các kim loại Mg, Al, Fe.
Lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch NaOH dư, sinh ra 3,36 lít khí (đktc). Mặt khác cũng lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch HCl dư, sinh ra 10,08 lít khí (đktc) và dung dịch B. Cho dung dịch B tác dụng với dung dịch NaOH dư, lọc kết tủa tạo thành và nung nóng trong không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m và tính % theo khối lượng của mỗi kim loại...
Đọc tiếp
Hỗn hợp A gồm các kim loại Mg, Al, Fe.
Lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch NaOH dư, sinh ra 3,36 lít khí (đktc). Mặt khác cũng lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch HCl dư, sinh ra 10,08 lít khí (đktc) và dung dịch B. Cho dung dịch B tác dụng với dung dịch NaOH dư, lọc kết tủa tạo thành và nung nóng trong không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m và tính % theo khối lượng của mỗi kim loại trong hỗn hợp A. Cho hỗn hợp A tác dụng với dung dịch CuSO4 dư, sau khi phản ứng kết thúc, lọc lấy chất rắn đem hòa tan hết chất rắn trong dung dịch HNO3 loãng dư, thu được 26,88 lít khí NO (đktc). Tính khối lượng hỗn hợp A.Tham khảo
Cho hỗn hợp X vào dung dịch HCl lấy dư:
PTHH: Al2O3 + 6HCl → 2AlCl3 + 3H2O
MgO + 2HCl → MgCl2 + H2O
Fe + 2HCl → FeCl2 + H2
Dung dịch Y gồm: AlCl3, MgCl2, FeCl2, HCl dư
Khí Z là H2
Chất rắn A là Cu
Cho A tác dụng với H2SO4 đặc nóng.
PTHH: Cu + 2H2SO4(đặc, nóng) → CuSO4 + SO2 + 2H2O
Khí B là SO2
Cho B vào nước vôi trong lấy dư
PTHH: SO2 + Ca(OH)2 → CaSO3 + H2O
Kết tủa D là CaSO3
Cho dung dịch NaOH vào Y tới khi kết tủa lớn nhất thì dừng lại.
PTHH: NaOH + HCl → NaCl + H2O
3NaOH + AlCl3 → Al(OH)3 + 3NaCl
2NaOH + MgCl2 → Mg(OH)2 + 2NaCl
2NaOH + FeCl2 → Fe(OH)2 + 2NaCl
Chất rắn E là: Al(OH)3, Mg(OH)2, Fe(OH)2
Nung E trong không khí
Chất rắn G là Al2O3, MgO, Fe2O3
Đúng 0
Bình luận (0)
Cho 7,4 gam hợp chất A tác dụng với 5,6 gam oxi thu được 3.36 lít khí CO2 và H2O
biết PTK của hợp chất A là 74 đvc
a) Xác định CTHH của A
b) Tính thể tích của CO2 và H2O khi cho 22.2 gam hợp chất A tác dụng với 10.08 lít khí oxi
Cho 0,84g Mg tác dụng với dung dịch HCl dư tạo ra Thể tích lít khí .Tính thể tích khí
giúp em với ạ
nMg= 0.84/24=0.035 mol
PTHH: Mg +2HCl ----> MgCl2 + H2
0.035..................................0.035
VH2= 0.035*22.4=0.784 l
Đúng 0
Bình luận (0)
Cho 18,30 gam hỗn hợp M gồm etanol và propan 1-ol tác dụng với natri dư thu được 4,2 lít khí (đktc) . Tính thành phần phần trăm khối lượng của mỗi chất trong M
\(2C_2H_5OH+2Na\rightarrow2C_2H_5Na+H_2\)
\(2C_3H_7OH+2Na\rightarrow2C_3H_7Na+H_2\)
Ta có:
\(n_{H2}=\frac{4,2}{22,4}=0,1875\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{C2H5OH}:a\left(mol\right)\\n_{C3H7OH}:b\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}0,5a+0,5b=0,1875\\46a+60b=18,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,03\\b=0,075\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{C2H5OH}=\frac{0,3.46}{18,3}.100\%=75,41\%\\\%m_{C3H7OH}=100\%-75,41\%=24,59\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Đem 17,8 gam hỗn hợp hai kim loại Mg và Zn chia làm 2 phần bằng nhau: ▪ Phần 1: Cho tác dụng với 0,2 lít dung dịch H2SO4 aM thoát ra 0,15 mol H2 ▪ Phần 2: Cho tác dụng với 0,3 lít dung dịch H2SO4 aM thoát ra 0,2 mol H2
Tất cả phản ứng xảy ra hoàn toàn.
a. Tính aM.
b. Tính khối lượng từng kim loại trong hỗn hợp ban đầu.
Chia làm hai phần bằng nhau mỗi phần co 8,9g hỗn hợp.
Phần 1:
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
x x x
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
y y y
\(\left\{{}\begin{matrix}24x+65y=8,9\\x+y=0,15\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{17}{820}\\y=\dfrac{53}{410}\end{matrix}\right.\)
\(\Rightarrow n_{H_2SO_4}=\dfrac{17}{820}+\dfrac{53}{410}=0,15mol\)
\(a=C_{M_{H_2SO_4}}=\dfrac{0,15}{0,2}=0,75M\)
\(m_{Mg}=2\cdot\dfrac{17}{820}\cdot24=1g\)
\(\Rightarrow m_{Zn}=17,8-1=16,8g\)
Đúng 4
Bình luận (0)