Chất X là muối photphat của kim loại R. Phân tử khối của X là 310 đvC. Tìm tên kim loại R?

Những câu hỏi liên quan
Kim loại R có hóa trị 3. Hợp chất tạo bởi R và nhóm SO4 có phân tử khối là 400 đvC. Hãy xác định nguyên tử khối của R
Đặt CTPT của chất là Rx(SO4)y (x, y nguyên dương)
Theo quy tắc hóa trị, ta có: x.III = y.II
=> \(\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTHH của chất lả R2(SO4)3
=> 2.R + (32 + 16.4).3 = 400
=> R = 56 (đvC)
Đúng 4
Bình luận (1)
áp dụng quy tắc hóa trị thì công thức hóa học đơn giản là
R2(SO4)3
theo đề bài ta có
PTK[R2(SO4)3]=400(dvC)
=>PTK(R2)=400-(32+16*4)*3=112(dvC)
=>NTK(R)=112:2=56(dvC)
=> R là sắt (Fe)
Đúng 3
Bình luận (1)
Muối Sunfat có dạng RSO4 có khối lượng phân tử là 160 đvC. Hỏi R là kim loại nào?
Có: MRSO4 = 1.MR + 32.1 + 16.4 = 160
=> MR = 64(g/mol)
=> R là Cu
Đúng 0
Bình luận (0)
Ta có: R + 32 + 16 . 4 =160
<=> R = 64
Vậy R là kim loại đồng
Đúng 0
Bình luận (0)
Ta có:
\(NTK\left(R\right)+32+16.4=160\\ \Rightarrow NTK\left(R\right)+96=160\\ \Rightarrow NTK\left(R\right)=64\)
\(\Rightarrow R\) là đồng
Đúng 0
Bình luận (0)
muối cacbonat có dạng RCO3 có khối lượng phân tử là 100 đvC Hỏi R là kim loại nào ❓
Khối lượng phân tử của RCO3 = MR + MC + 3. MO= MR + 12 + 3.16=100
=> MR = 40
Vậy R là Canxi (Ca)
Đúng 1
Bình luận (0)
1.Oxit cao nhất của 1 nguyên tố R có dạng R2Ox. Phân tử khối của oxit là 102 đvC. Xác định R.
2. Cho biết phân tử khối của một oxit kim loại là 160, phần trăm khối lượng của kim loại trong
oxit là 70%. Lập công thức oxit đó.
1)
PTKR2Ox = 2.NTKR + 16x = 102 (đvC)
| x | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| NTKR | 43(Loại) | 35(Loại) | 27(Al) | 19(Loại) | 11(Loại) | 3(Loại) | Loại | Loại |
=> R là Al
2)
CTHH: RxOy
\(\%R=\dfrac{x.NTK_R}{160}.100\%=70\%\)
=> \(NTK_R=\dfrac{112}{x}\left(đvC\right)\)
Chỉ có x = 2 thỏa mãn \(NTK_R=\dfrac{112}{2}=56\left(đvC\right)\)
=> R là Fe
PTKFe2Oy = 160 (đvC)
=> y = 3
CTHH: Fe2O3
Đúng 2
Bình luận (0)
Nguyên tố R tạo một oxit RO2 (chất D) và một hợp chất RHn (chất E). Cho biết khối lượng riêng hơi của E ở dktc là 1,5179g/ml và phân tử khối của D là 32/17 phân tử khối của E.a) Tìm nguyên tố Rb) M là kim loại hóa trị I, tạo được muối X có công thức M2RO3. Hòa tan 12,6g X trong 100ml dd HCl lấy dư có D 1,2g/ml. Sau phản ứng thu được 126,2g dd. Tìm kim loại M
Đọc tiếp
Nguyên tố R tạo một oxit RO2 (chất D) và một hợp chất RHn (chất E). Cho biết khối lượng riêng hơi của E ở dktc là 1,5179g/ml và phân tử khối của D là 32/17 phân tử khối của E.
a) Tìm nguyên tố R
b) M là kim loại hóa trị I, tạo được muối X có công thức M2RO3. Hòa tan 12,6g X trong 100ml dd HCl lấy dư có D = 1,2g/ml. Sau phản ứng thu được 126,2g dd. Tìm kim loại M
a) MD = R + 32 (g/mol)
ME = R + n (g/mol)
Theo đề bài \(\dfrac{M_D}{M_E}\)= \(\dfrac{R+32}{R+n}\)= \(\dfrac{32}{17}\) => \(\left\{{}\begin{matrix}n=2\\R=32\end{matrix}\right.\) là giá trị thỏa mãn
Vậy R là lưu huỳnh (S)
b) m 100ml dung dịch HCl = 1,2.100 = 120 gam
M2SO3 + 2HCl → 2MCl + SO2↑ + H2O
m dung dịch sau phản ứng = m M2SO3 + m dung dịch HCl - m SO2 = 126,2 gam
=> 12,6 + 120 - 126,2 = mSO2
<=> mSO2 = 6,4 gam , nSO2 = 6,4 : 64 = 0,1 mol
Theo phương trình phản ứng , nM2SO3 = nSO2 = 0,1 mol
=> MM2SO3 = \(\dfrac{12,6}{0,1}\)= 126 (g/mol)
=> MM = (126 - 32 - 16.3) : 2 = 23 g/mol
Vậy M là natri (Na)
Đúng 3
Bình luận (2)
Nguyên tố R là một phi kim, tỉ lệ phần trăm khối lượng của R trong hợp chất khí với hidro bằng 0,5955. Cho 4,05 gam một kim loại M chưa rõ hóa trị tác dụng hết với đơn chất R thì được 40,05 gam muối. Phân tử khối của muối tạo ra là A. 267 B. 169 C. 89 D. 107
Đọc tiếp
Nguyên tố R là một phi kim, tỉ lệ phần trăm khối lượng của R trong hợp chất khí với hidro bằng 0,5955. Cho 4,05 gam một kim loại M chưa rõ hóa trị tác dụng hết với đơn chất R thì được 40,05 gam muối. Phân tử khối của muối tạo ra là
A. 267
B. 169
C. 89
D. 107
Đáp án A
* Xác định nguyên tố phi kim R:
+) Nếu hóa trị của R trong oxit cao nhất là chẵn thì ta có công thức của oxit cao nhất là ROn.
Khi đó công thức của hợp chất khí với hidro của R là RH8-2n. Theo giả thiết đề bài ta có:

| n |
1 |
2 |
3 |
| R |
8,72 |
37,22 |
65,72 |
Do đó trường hợp này có kết quả thỏa mãn.
+) Nếu hóa trị của R trong oxit cao nhất là lẻ thì ta có công thức oxit cao nhất là R2On.
Khi đó công thức của hợp chất khí với hidro của R là RH8-n. Theo giả thiết đề bài ta có:
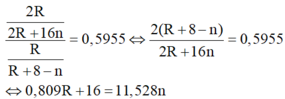
| n |
1 |
3 |
5 |
7 |
| R |
âm |
22,97 |
51,47 |
80 |
Do đó có n = 7 và R = 80 thỏa mãn.
Suy ra R là Br.
* Xác định kim loại M.
Vì Br trong hợp chất muối với kim loại có hóa trị I
Nên gọi công thức của muối thu được là MBrx với x là hóa trị của M. Theo định luật bảo toàn khối lượng ta có:
![]() (gam)
(gam)
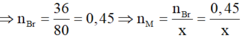
Mà 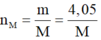 nên
nên 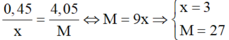 là Al.
là Al.
Do đó muối thu được là AlBr3.
Vậy phân tử khối của muối tạo ra là 27 + 80.3 = 267
Đúng 0
Bình luận (0)
Nguyên tố R là một phi kim, tỉ lệ phần trăm khối lượng của R trong hợp chất khí với hidro bằng 0,5955. Cho 4,05 gam một kim loại M chưa rõ hóa trị tác dụng hết với đơn chất R thì được 40,05 gam muối. Phân tử khối của muối tạo ra là A. 267 B. 169 C. 89 D. 107
Đọc tiếp
Nguyên tố R là một phi kim, tỉ lệ phần trăm khối lượng của R trong hợp chất khí với hidro bằng 0,5955. Cho 4,05 gam một kim loại M chưa rõ hóa trị tác dụng hết với đơn chất R thì được 40,05 gam muối. Phân tử khối của muối tạo ra là
A. 267
B. 169
C. 89
D. 107
Đáp án A
* Xác định nguyên tố phi kim R:
+) Nếu hóa trị của R trong oxit cao nhất là chẵn thì ta có công thức của oxit cao nhất là ROn.
Khi đó công thức của hợp chất khí với hidro của R là RH8-2n. Theo giả thiết đề bài ta có:

Do đó trường hợp này có kết quả thỏa mãn.
+) Nếu hóa trị của R trong oxit cao nhất là lẻ thì ta có công thức oxit cao nhất là R2On.
Khi đó công thức của hợp chất khí với hidro của R là RH8-n. Theo giả thiết đề bài ta có:

Do đó có n = 7 và R = 80 thỏa mãn.
Suy ra R là Br.
* Xác định kim loại M.
Vì Br trong hợp chất muối với kim loại có hóa trị I
Nên gọi công thức của muối thu được là MBrx với x là hóa trị của M. Theo định luật bảo toàn khối lượng ta có:
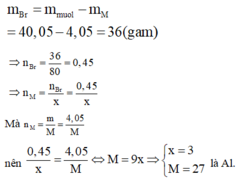
Do đó muối thu được là AlBr3.
Vậy phân tử khối của muối tạo ra là 27 + 80.3 = 267
Đúng 0
Bình luận (0)
R là nguyên tố kim loại có hóa trị không đổi 1 hợp chất của R với nhóm cacbonat trong đó nguyên tố R chiếm 40% theo khối lượng không cần xác định nguyên tố R em Hãy tính phần trăm khối lượng của nguyên tố R trong hợp chất muối photphat
CTHH muối cacbonat: R2(CO3)n
CTHH muối photphat: R3(PO4)n
Xét R2(CO3)n
\(\%R=\dfrac{2.M_R}{2.M_R+60n}.100\%=40\%\)
=> 2.MR = 0,8.MR + 24n
=> 1,2.MR = 24n
=> \(M_R=20n\) (g/mol)
Xét R3(PO4)n
\(\%R=\dfrac{3.M_R}{3.M_R+95n}.100\%=\dfrac{3.20n}{3.20n+95n}.100\%=38,71\%\)
Đúng 2
Bình luận (0)
một khim loại X có hóa trị n. Nếu % khối lượng của kim loại đó trong muối cacbonat là 40% thì % khối lượng của kim loại đó trong muối photphat là bao nhiêu? Điều đó có đúng với mọi kim loại không? Vì sao?
\(CTTQ:X_2\left(CO_3\right)_n\\ Vì:\%m_X=40\%\\ \Leftrightarrow\dfrac{2M_X}{2M_X+60n}.100\%=40\%\\ \Leftrightarrow60n=60\%M_{hc}\\ \Leftrightarrow M_{hc}=100n\)
Xét các TH n=1; n=2; n=3 ; n=8/3
=>Chọn n=2 => CTTQ: XCO3 => X: Canxi (Ca)
Đúng 1
Bình luận (4)
$CTHH:X_2(CO_3)_n$ và $X_3(PO_4)_n$
\(\%m_{X(CO_3^{2-})}=\dfrac{2X}{2X+60n}.100\%=40\%\\ \Rightarrow \dfrac{X}{X+30n}=0,4\\ \Rightarrow X=12n+0,4X\\ \Rightarrow X=20n\\ \%m_{X(PO_4^{3-})}=\dfrac{3X}{3X+95n}.100\% =\dfrac{60n}{60n+95n}.100\%\approx 38,71\%\)
Điều này không đúng với mọi KL vì mỗi KL có NTK khác nhau và có hóa trị khác nhau
Đúng 0
Bình luận (0)





















