Nguyên tử R có tổng số hạt là 40, trong đó số n nhiều hơn số p là 1 hạt. R là nguyên tử nguyên tố nào?

Những câu hỏi liên quan
Nguyên tử của nguyên tố R có tổng số hạt bằng 40, trong đó số hạt n nhiều hơn số hạt p là 1 hạt. Xác định tên, KHHH của nguyên tử R.
Tổng số hạt bằng 40
\(2p+n=40\left(1\right)\)
Số hạt n nhiều hơn số hạt p là 1 hạt
\(-p+n=1\left(2\right)\)
\(\left(1\right),\left(2\right):p=e=13,n=14\)
\(R:Al\)
Đúng 2
Bình luận (0)
Gọi số hạt proton = số hạt electron = p
Gọi số hạt notron = n
Ta có :
$2p + n = 40$
$n - p = 1$
Suy ra p = 13 ; n = 14
Vậy R là nguyên tố Nhôm, KHHH : Al
Đúng 3
Bình luận (0)
Theo đề ta cps: p + n + e = 40 (1)
n - p = 1 => n = 1 + p (2)
Từ (1) và (2) => p + 1 + p + e = 40
=> 2p + e = 39
Mà p = e
=> p = e = 39/3 = 13
=> ĐÓ Là nhôm (Al)
Đúng 2
Bình luận (0)
Xem thêm câu trả lời
Câu 4: Tìm số E, P. N trong các trường hợp sau:a. Nguyên tử nhôm có tổng số hạt là 40, trong hạt nhân số hạt không mang điện nhiều hơn số hạt mang điện là 1. b. Nguyên tử một nguyên tố R có tổng các hạt 21, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 7.c. Hạt nhân nguyên tử một nguyên tố X có tổng các hạt 16, tỉ lệ giữa số hạt mang điện và số hạt không mang điện là 1:1.
Đọc tiếp
Câu 4: Tìm số E, P. N trong các trường hợp sau:
a. Nguyên tử nhôm có tổng số hạt là 40, trong hạt nhân số hạt không mang điện nhiều hơn số hạt mang điện là 1.
b. Nguyên tử một nguyên tố R có tổng các hạt 21, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 7.
c. Hạt nhân nguyên tử một nguyên tố X có tổng các hạt 16, tỉ lệ giữa số hạt mang điện và số hạt không mang điện là 1:1.
a,
Ta có: \(\left\{{}\begin{matrix}p+e+n=40\\p=e\\n-p=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}3p=39\\n=p+1\\p=e\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=13\\n=14\end{matrix}\right.\)
b,
Ta có: \(\left\{{}\begin{matrix}p+e+n=21\\p=e\\p+e-n=7\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2n=14\\p=e\\p+e+n=21\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=7\\n=7\end{matrix}\right.\)
c,
Ta có: \(\left\{{}\begin{matrix}p+n=16\\p=e\\\dfrac{p}{n}=\dfrac{1}{1}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2p=16\\p=e\\p=n\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=8\\n=8\end{matrix}\right.\)
Đúng 2
Bình luận (1)
Nguyên tử của một nguyên tố R có tổng số các loại hạt bằng 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22 hạt. Số hiệu nguyên tử của R là:
A. 56
B. 30
C. 26
D. 24
Chọn C
Gọi số proton, nơtron và electron của R lần lượt là p, n và e trong đó p = e.
Theo bài ra ta có: 2p + n = 82 và 2p – n = 22.
Giải hệ phương trình được p = 26 và n = 30.
Số hiệu nguyên tử của R là 26.
Đúng 0
Bình luận (0)
Câu 2: Tổng hạt proton, nơtron và electron trong nguyên tử của nguyên tố R là 40.
a) Xác định số hiệu nguyên tử và số khối của R? Biết trong nguyên tử R số hạt mang điện nhiều hơn số hạt không mang điện là 12.
b) Viết cấu hình electron nguyên tử của nguyên tố đó. Biểu diễn sự phân bố các electron trên các obitan của R?
Nguyên tố X có tổng số hạt trong nguyên tử là 40, trong đó số hạt mang điện nhiều hơn hạt không mang điện là 12. Nguyên tố Y có tổng số hạt nguyên tử là 52. Số hạt mang điện nhiều hơn hạt mang điện trong X là 8. xác định Ct hợp chất gồm hai nguyên tố x và y
Do nguyên tử X có tổng số hạt trong nguyên tử là 40
=> 2pX + nX = 40 (1)
Do nguyên tử X có số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt
=> 2pX - nX = 12 (2)
(1)(2) => \(\left\{{}\begin{matrix}e_X=p_X=13\\n_X=14\end{matrix}\right.\) => X là Al
Nguyên tử X có số hạt mang điện là 13 + 13 = 26 (hạt)
=> Nguyên tử Y có số hạt mang điện là 26 + 8 = 34 (hạt)
=> eY = pY = 17 (hạt)
=> Y là Cl
CTHH hợp chất 2 nguyên tố X, Y có dạng AlxCly
Có: \(Al^{III}_xCl^I_y\)
=> Theo quy tắc hóa trị, ta có: x.III = y.I
=> \(\dfrac{x}{y}=\dfrac{I}{III}=\dfrac{1}{3}\)
=> CTHH: AlCl3
Đúng 8
Bình luận (0)
ta có : số hạt mạng điện tích ở X nhiều hơn số hạt ko mạng điện tích là 12
=> p+e-n = 12
<=> 2p-n=12 (p=e)
<=> n = 2p - 12 (1)
mà tổng số hạt ở X là 40
=> 2p+n=40 (2)
thay (1)vào (2) ta đc
2p+2p-12 = 40
<=> 4p = 52
<=> p = 13
=> X là nhôm : Al
Đúng 2
Bình luận (0)
Tổng số hạt trong nguyên tử R là 76, số hạt mang điện nhiều hơn số hạt không mang điện là 20.
a/ Cho biết R là nguyên tử của nguyên tố nào. Vẽ sơ đồ cấu tạo nguyên tử R?
b/ Tính khối lượng bằng gam của 2 nguyên tử R
a)
Gọi số hạt proton = số hạt elctron = p
Gọi số hạt notron = n
Ta có :
$2p+ n = 76$
$2p -n = 20$
Suy ra p = 24 ; n = 28
Vậy R là nguyên tử nguyên tố Crom
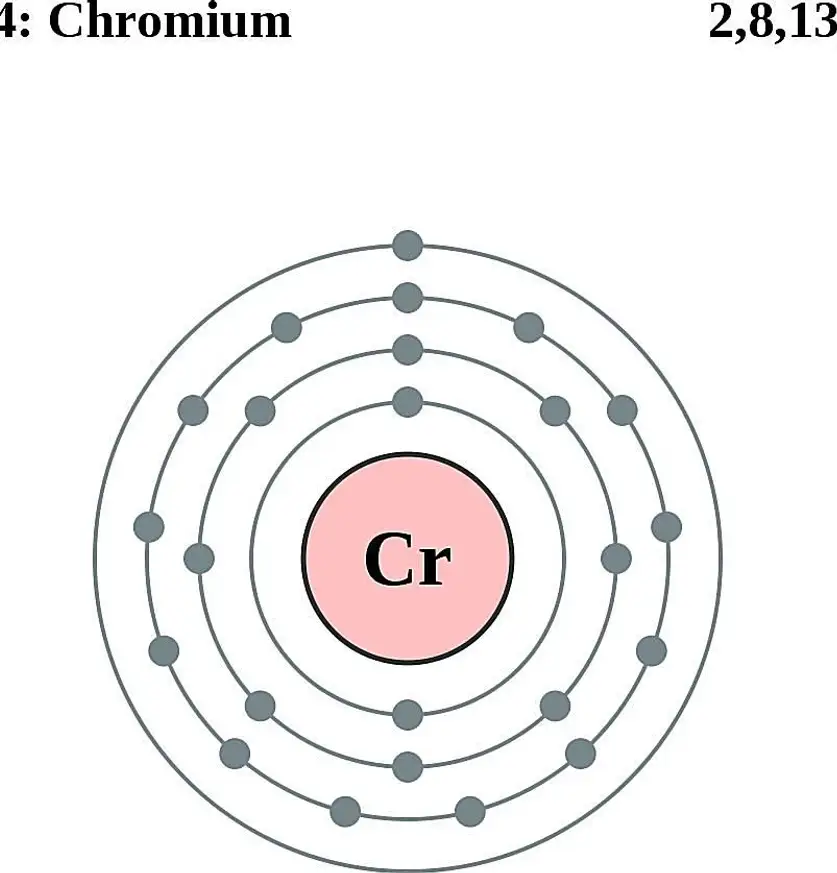
b)
$m_{2\ nguyên\ tử\ Crom} = 2.52.0,166.10^{-24} = 2,7364.10^{-23}(kg)$
Đúng 1
Bình luận (2)
Bài 1: Nguyên tử R có tổng số hạt là 62, trong đó số khối của R nhỏ hơn 43. Tính N, P
Bài 2: 2 nguyên tử A và B có tổng số các hạt là 142 trong đó số hạt mang điện nhiều hơn hạt ko mang điện là 42. Số hạt mang điện của B nhiều hơn của A là 12.
Tìm P của A
Tìm P của B
mik cần gấp mọi người giúp mik với nha, mik cảm ơn rất nhiều ![]()
Đúng 0
Bình luận (0)
Bài 1: Nguyên tử của 1 nguyên tố X có tổng số hạt là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt. Tính số hạt từng loạiBài 2: Nguyên tử của 1 nguyên tố Y có tổng số hạt là 58. Trong đó số hạt proton ít hơn số hạt notron là 1 hạt. Tính số hạt từng loạiBài 3: Nguyên tử của một nguyên tố A có tổng số hạt proton, nơtron, electron là 48, trong đó số hạt mang điện gấp hai lần số hạt không mang điện. Tính số hạt mỗi loại.
Đọc tiếp
Bài 1: Nguyên tử của 1 nguyên tố X có tổng số hạt là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt. Tính số hạt từng loại
Bài 2: Nguyên tử của 1 nguyên tố Y có tổng số hạt là 58. Trong đó số hạt proton ít hơn số hạt notron là 1 hạt. Tính số hạt từng loại
Bài 3: Nguyên tử của một nguyên tố A có tổng số hạt proton, nơtron, electron là 48, trong đó số hạt mang điện gấp hai lần số hạt không mang điện. Tính số hạt mỗi loại.
Gọi số hạt proton = Số hạt electron = p
Gọi số hạt notron = n
Hạt mang điện là proton, electron
Hạt không mang điện là notron
Bài 1 :
Ta có :
$2p + n = 40$ và $2p - n = 12$
Suy ra p = 13 ; n = 14
Bài 2 :
Ta có :
$2p + n = 58$ và $n - p = 1$
Suy ra p = 19 ; n = 20
Bài 3 :
Ta có :
$2p + n = 48$ và $2p = 2n$
Suy ra p = n = 16
Đúng 1
Bình luận (0)
1:Tổng số hạt cơ bản của nguyên tử nguyên tố X là 36.Trong đó số hạt mang điện gấp đôi số hạt không mang điện.Xác định số hiệu nguyên tử và số khối của nguyên tử X?2:Tổng số hạt trong nguyên tử là Y là 54 hạt,trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 14.a)Xác định các loại hạt trong Y b)Xác định đơn vị điện tích hạt nhân của Y c)Viết kí hiệu nguyên tử Y 3:Nguyên tử R có tổng số hạt là 115.Số hạt mang điện nhiều hơn số hạt không mang điện là 25.Xác định ngu...
Đọc tiếp
1:Tổng số hạt cơ bản của nguyên tử nguyên tố X là 36.Trong đó số hạt mang điện gấp đôi số hạt không mang điện.Xác định số hiệu nguyên tử và số khối của nguyên tử X?
2:Tổng số hạt trong nguyên tử là Y là 54 hạt,trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 14.
a)Xác định các loại hạt trong Y b)Xác định đơn vị điện tích hạt nhân của Y c)Viết kí hiệu nguyên tử Y
3:Nguyên tử R có tổng số hạt là 115.Số hạt mang điện nhiều hơn số hạt không mang điện là 25.Xác định nguyên tử R từ đó suy ra STT của R?
-Mình cần rất gấp,các bạn giúp mình với!-
1. Ta có tổng số hạt cơ bản của nguyên tố X là 36 , suy ra
p + e + n = 36 => 2p + n = 36
Số hạt mang điện gấp đôi số hạt không mang điện : 2p = 2n => p = n
Vậy : 3p = 36 => p = 12 => số p = số e = số z = 12
Số khối : A = p + n = 12 + 12 = 24
Đúng 2
Bình luận (3)
2.
a, Ta có tổng số hạt cơ bản là 54 hạt.
=> p+e+n=54 => 2p+n=54(1)
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 14
=> 2p-n=14(2)
Từ (1) và (2) ta có hệ pt:
2p-n=14
2p+n=54
<=> p=17
n=20
Vậy e=17, p=17, n=20
b, số hiệu nguyên tử Z=17
c, kí hiệu: Cl
Đúng 2
Bình luận (1)
3.
Ntử R có tổng số hạt cơ bản là 115
=> p+e+n=115
=>2p+n=115(1)
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 25
=> 2p-n=25(2)
Từ (1)&(2) => ta có hệ phương trình
=>2p+n=115
2p-n=25
<=>p=35
n=45
=> e=35, p=35, n=45
=> R là Br
STT của Br là 35
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Hợp chất X tạo bởi 2 nguyên tử của nguyên tố R với 1 nguyên tử của nguyên tố Y. Trong X tổng số hạt mang điện và không mang điện là 92 ; tổng số hạt không mang điện nhiều hơn tổng số hạt mang điện dương là 2; số hạt mang điện dương của R nhiều hơn số hạt mang điện dương của Y là 14.
Xác định R, Y thuộc nguyên tố nào? Lập công thức phân tử của X.
Tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong X.
Không cần tính toán, hãy suy luận để sắp xếp các chất sau theo thứ tự tăng dầ...
Đọc tiếp
Hợp chất X tạo bởi 2 nguyên tử của nguyên tố R với 1 nguyên tử của nguyên tố Y. Trong X tổng số hạt mang điện và không mang điện là 92 ; tổng số hạt không mang điện nhiều hơn tổng số hạt mang điện dương là 2; số hạt mang điện dương của R nhiều hơn số hạt mang điện dương của Y là 14.
Xác định R, Y thuộc nguyên tố nào? Lập công thức phân tử của X. Tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong X.Không cần tính toán, hãy suy luận để sắp xếp các chất sau theo thứ tự tăng dần hàm lượng oxi: Na2O, CaO, CuO, PbO, Fe2O3.























