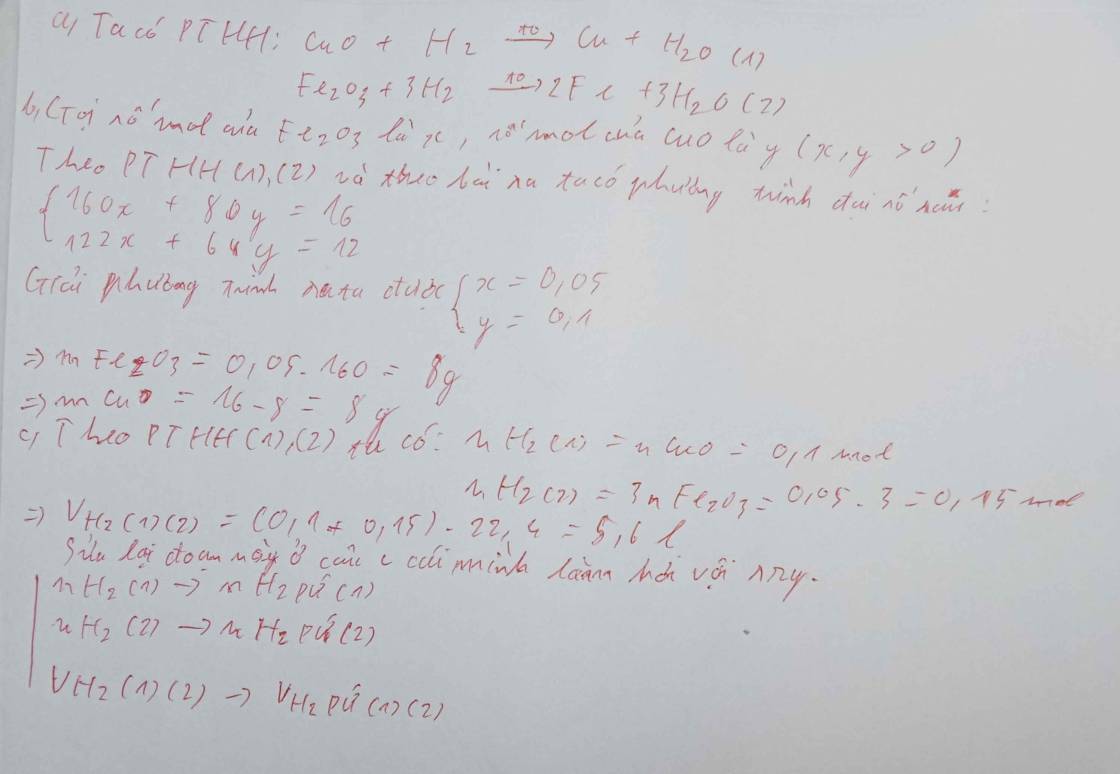cho dòng khí CO dư qua hỗn hợp 2 Oxit : CuO , Fe2O3 . Nung nóng thu được 29,6 g hỗn hợp 2 kim loại sắt trong đó Fe nhiều hơn Cu là 4g . Tính VCO cần dùng

Những câu hỏi liên quan
cho dòng khí co dư qua hỗn hợp 2 oxit cuo và fe3o4 nung nóng thu được 29,6 hỗn hợp 2 kim loại trong đó sắt nhiều hơn đồng là 4g. tính thể tích khí co cần dùng
Ta có: \(m_{Fe}\) + \(m_{Cu}\) = 29,6
hay\(m_{Cu}\) +4 + \(m_{Cu}\) = 29,6
2\(m_{Cu}\) = 25,6
\(m_{Cu}\) =12,8(g)
=> \(m_{Fe}\) = 16,8(g)
Số mol của 12,8 g Cu:
\(\frac{12,8}{64}\)= 0,2(mol)
Số mol của 16,8g Fe:
\(\frac{16,8}{56}\)=0,3(mol)
CO + CuO \(\rightarrow\) Cu + C\(O_2\)
1(mol) 1(mol)
0,2(mol) 0,2(mol)
4CO + \(Fe_3\)\(O_4\) \(\rightarrow\) 3Fe + 4C \(O_2\)
4(mol) 3(mol)
0,4(mol) 0,3(mol)
Thể tích CO cần dùng:
(0,2+0,4).22,4= 13,44(l)
Đúng 0
Bình luận (0)
PTHH: Fe3O4+4Co->3Fe+4Co2 (1)
CuO+Co->Cu+Co2 (2)
Lại có: mFe+mCu=29,6
mFe-mCu=4
=>mFe=16,8=> nFe=0.3mol
mCu=12,8g=>nCu=0.2mol
Theo PTHH(1)
nFe:nCo= 3:4=> nCo=0,3.4/3=0,4mol
nCu:nCo= 1:1 => nCo= 0,2mol
=> nCo=0,6mol=13,44(l)
Đúng 0
Bình luận (0)
bạn ơi mk cx muốn hỏi câu này
ban trả lời giúp mk đc ko
Đúng 0
Bình luận (0)
Cho dòng khí CO qua hỗn hợp 2 oxit CuO và F e 3 O 4 nung nóng thu được 29,6g hỗn hợp 2 kim loại trong đó sắt nhiều hơn đồng là 4g.
Tính thể tích khí CO cần dùng (đktc).
PTHH của các phản ứng:
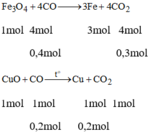
Gọi x là khối lượng của Cu sau phản ứng
→ Khối lượng của sắt sau phản ứng là x+4
Theo đề bài ta có: x + x + 4 = 29,6 → x = 12,8(g)
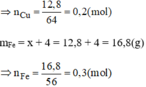
Theo pt: 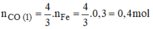
n C O ( 2 ) = n C u = 0 , 2 m o l
n C O = (0,4 + 0,2).22,4 = 13,44(l)
Đúng 0
Bình luận (0)
1.Đốt cháy hỗn hợp bột Fe và Mg trong đó khối lượng Mg là 0,48g cần dùng hết 672ml oxi ở đktc.a)Tính khối lượng hỗn hợp ban đầub)Tính thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp2.Cho dòng khí CO dư đi qua hỗn hợp 2 oxit CuO và Fe2O3 nung nóng thu được 29,6g hỗn hợp 2 kim loại trong đó Fe nhiều hơn Cu 4g.Tính thể tích khí CO cần dùng ở đktc
Đọc tiếp
1.Đốt cháy hỗn hợp bột Fe và Mg trong đó khối lượng Mg là 0,48g cần dùng hết 672ml oxi ở đktc.
a)Tính khối lượng hỗn hợp ban đầu
b)Tính thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp
2.Cho dòng khí CO dư đi qua hỗn hợp 2 oxit CuO và Fe2O3 nung nóng thu được 29,6g hỗn hợp 2 kim loại trong đó Fe nhiều hơn Cu 4g.
Tính thể tích khí CO cần dùng ở đktc
Dẫn luồng khí H2 dư đi qua 16g hoá hợp A chứa hai oxit CuO và Fe2O3 nung nóng sau khi hỗn hợp kết thúc thu được 12g hỗn hợp B chứa 2 kim loại Đồng và Sắt a, Viết pthhb,Tính khối lượng mỗi oxit trong hoá hợp A c,Tính thể tích H2 đã dùng ở đktc
Đọc tiếp
Dẫn luồng khí H2 dư đi qua 16g hoá hợp A chứa hai oxit CuO và Fe2O3 nung nóng sau khi hỗn hợp kết thúc thu được 12g hỗn hợp B chứa 2 kim loại Đồng và Sắt
a, Viết pthh
b,Tính khối lượng mỗi oxit trong hoá hợp A
c,Tính thể tích H2 đã dùng ở đktc
Dẫn khí CO dư qua hỗn hợp bột gồm MgO, CuO, FeO, Fe2O3 nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn X. Oxit kim loại trong X là A. MgO. B. CuO. C. FeO. D. Fe2O3
Đọc tiếp
Dẫn khí CO dư qua hỗn hợp bột gồm MgO, CuO, FeO, Fe2O3 nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn X. Oxit kim loại trong X là
A. MgO.
B. CuO.
C. FeO.
D. Fe2O3
Chọn A
vì CO khử oxit của kim loại đứng sau Al
Đúng 0
Bình luận (0)
Cho hỗn hợp gồm CuO và Fe3O4 tác dụng với H2 dư ở nhiệt độ cao hỏi nếu thu được 29,26g kim loại trong đó Fe nhiều hơn Cu là 4g thì VH2 cần dùng là bnhieu
Gọi a, b là khối lượng của Fe và Cu.
Ta có: a + b = 29,26 và a - b = 4
Suy ra: a = 16,63 gam và b = 12,63 gam.
Số mol H2 = số mol H2O = số mol O trong hh = 4.16,63/3.56 + 12,63/64 = 0,59 mol.
Hay V = 13,216 lít.
Đúng 1
Bình luận (1)
Gọi mFe =a(g) và mCu=b(g)
Ta có:a+b=29,26 và a-b=4
=>a=16,63g va b=12,63g
Ta có:nH2=nH2O=nO trong hỗn hợp=\(\frac{4.16,63}{3,56}\)+\(\frac{12,63}{64}\)=0,59 mol
=>VH2O=13,216 lít
Đúng 0
Bình luận (0)
11/ Dẫn dòng khí H2 dư qua hỗn hợp gồm 1,6g Fe2O3 và 4g CuO ở nhiệt độ cao
a/ Viết phương trình hóa học của các phản ứng? b/ Tính khối lượng kim loại Cu và Fe thu được spư.
c/ tính số mol H2 đã tham gia các pư.
12/ Dùng 3,36 lit khí hidrro khử hoàn toàn 8 gam một oxit sắt. Tìm CTHH của oxit sắt
Bài 11:
\(a,n_{Fe_2O_3}=\dfrac{1,6}{160}=0,01\left(mol\right)\\ n_{Cu}=\dfrac{4}{80}=0,05\left(mol\right)\\ PTHH:\\ Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
0,01 -----> 0,03 ---> 0,02
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,05 ---> 0,05 -> 0,05
\(b,m_{Fe}=0,02.56=1,12\left(g\right)\\ m_{Cu}=0,05.64=3,2\left(g\right)\\ V_{H_2}=\left(0,03+0,05\right).22,4=1,792\left(l\right)\)
Bài 12:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ n_{O\left(trong.oxit\right)}=n_{H_2}=0,15\left(mol\right)\\ n_{Fe\left(trong.oxit\right)}=\dfrac{8-0,15,16}{56}=0,1\left(mol\right)\\ CTHH:Fe_xO_y\\ \Rightarrow x:y=0,1:0,15=2:3\\ CTHH:Fe_2O_3\)
Đúng 0
Bình luận (0)
Dẫn khí CO dư qua hỗn hợp bột gồm MgO, CuO, FeO,
F
e
2
S
O
3
nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn X. Oxit kim loại trong X là A. MgO. B. CuO. C. FeO. D.
F
e
2
O
3
Đọc tiếp
Dẫn khí CO dư qua hỗn hợp bột gồm MgO, CuO, FeO, F e 2 S O 3 nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn X. Oxit kim loại trong X là
A. MgO.
B. CuO.
C. FeO.
D. F e 2 O 3
Đáp án A
Chọn A vì CO khử oxit của kim loại đứng sau Al.
Đúng 0
Bình luận (0)
Cho CO đi qua 70,25 gam hỗn hợp X gồm Fe2O3 và một oxit của kim loại R (R có hóa trị không đổi) nung nóng thu được 3,36(l) khí CO2 và hỗn hợp Y gồm Fe, Fe2O3, FeO, Fe3O4, oxit của kim loại R. Hỗn hợp Y phản ứng vừa đủ với 750ml H2SO4 1M thu được 1,12 lít khí H2và hỗn hợp Z.Thêm tiếp dung dịch NaOH từ từ cho tới dư vào hh Z, sau phản ứng hòan toàn thu được kết tủa T. Lọc T để ngoài không khí đến khối lượng không đổi thu được 101,05 gam chất rắn. Xác định CT của oxit kim loại R
Đọc tiếp
Cho CO đi qua 70,25 gam hỗn hợp X gồm Fe2O3 và một oxit của kim loại R (R có hóa trị không đổi) nung nóng thu được 3,36(l) khí CO2 và hỗn hợp Y gồm Fe, Fe2O3, FeO, Fe3O4, oxit của kim loại R. Hỗn hợp Y phản ứng vừa đủ với 750ml H2SO4 1M thu được 1,12 lít khí H2và hỗn hợp Z.Thêm tiếp dung dịch NaOH từ từ cho tới dư vào hh Z, sau phản ứng hòan toàn thu được kết tủa T. Lọc T để ngoài không khí đến khối lượng không đổi thu được 101,05 gam chất rắn. Xác định CT của oxit kim loại R

Chào bạn tuy không thể giúp bạn nhưng cho mình hỏi bạn có bị mất thanh thông báo tin nhắn như mình không ạ
Đúng 0
Bình luận (3)
Oxit kim loại R : \(R_2O_n\)
\(n_{Fe_2O_3} = a(mol) ; n_{R_2O_n} = b(mol)\\ \Rightarrow 160a + b(2R + 16n) = 70,25(1)\)
\(n_{CO} = n_{CO_2} = 0,15(mol)\)
\(CO + O_{oxit} \to CO_2\)
\(n_{O\ pư} = n_{CO_2} = 0,15(mol)\)
\(2H^+ \to H_2 + 2e\\ 2H^+ + O^{2-} \to H_2O\)
Ta có : \(n_{H^+} =2n_{H_2SO_4} = 2n_{H_2} + 2n_{O(Y)}\)
\(\Rightarrow n_{O(Y)} = 0,7(mol)\)
Bảo toàn nguyên tố với O : 3a + bn = 0,7 + 0,15 = 0,85(2)
Sau phản ứng, không thu được kim loại R,chứng tỏ R không phản ứng với CO
Mà sau khi nung T thu được khối lượng oxit lớn hơn khối lượng X ban đầu. Chứng tỏ muối sunfat của kim loại R không tan trong nước.
Vậy,101,05 gam chất rắn gồm :
\(Fe(OH)_3 : 2a(mol)\\ R_2(SO_4)_n : b(mol)\)
⇒107.2a + b(2R + 96n) = 101,05(3)
Từ (1)(2)(3) suy ra a = 0,2 ; Rb = 17,125 ; bn = 0,25
Suy ra :\(R = \dfrac{17,125}{\dfrac{0,25}{n}} = \dfrac{137}{2}n\)
Với n = 2 thì R = 137(Ba) .Vậy oxit : BaO
Đúng 2
Bình luận (4)