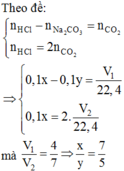rộn V1 ml dung dịch axit clohiđric có nồng độ 0,5M với V2 ml dung dịch axit clohiđric cÓ nồng độ 3M ta thu được 100 ml dung dịch axit clohiđric có nồng độ 2,5M tính V1 và V2

Những câu hỏi liên quan
cho 600 ml dung dịch axit clohiđric 2M vào thể tích nước để thu được dung dịch axit clohiđric có nồng độ 0,75 M .xác định thể tích
\(n_{HCl} = 0,6.2 = 1,2(mol)\\ \Rightarrow V_{dd\ HCl\ 0,75M} = \dfrac{1,2}{0,75} = 1,6(lít) = 1600(ml)\\ \Rightarrow V_{nước} = 1600 -600 = 1000(ml)\)
Đúng 1
Bình luận (0)
Cho 50 ml dd bari hiđroxit 0,5M tác dụng với 150 ml dd axit clohiđric 0,1M.
a) Viết PTPƯ xảy ra?
b) Dung dịch sau phản ứng có tính kiềm, axit hay trung tính?
c) Tính nồng độ mol của các chất có trong dung dịch sau phản ứng?
PTHH: \(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Ba\left(OH\right)_2}=0,05\cdot0,5=0,025\left(mol\right)\\n_{HCl}=0,15\cdot0,1=0,015\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,025}{1}>\dfrac{0,015}{2}\) \(\Rightarrow\) Ba(OH)2 còn dư, dd sau p/ứ có tính kiềm
\(\Rightarrow\left\{{}\begin{matrix}n_{BaCl_2}=0,0075\left(mol\right)\\n_{Ba\left(OH\right)_2\left(dư\right)}=0,0175\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{BaCl_2}}=\dfrac{0,0075}{0,05+0,15}=0,0375\left(M\right)\\C_{M_{Ba\left(OH\right)_2}}=\dfrac{0,0175}{0,2}=0,0875\left(M\right)\end{matrix}\right.\)
Đúng 0
Bình luận (0)
: Cho 36,4 gam sắt vào dung dịch axit clohiđric nồng độ 0,5M.
a. Tính thể tích dung dịch axit clohiđric đã phản ứng?
b. Tính thể tích khí sinh ra (đktc)?
c. Tính nồng độ dung dịch muối thu được (coi thể tích dung dịch không thay đổi)?
\(n_{Fe}=\dfrac{36,4}{56}=0,65\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
0,65->1,3----->0,65--->0,65
=> \(\left\{{}\begin{matrix}a,V_{ddHCl}=\dfrac{1,3}{0,5}=2,6\left(l\right)\\b,V_{H_2}=0,65.22,4=14,56\left(l\right)\end{matrix}\right.\)
c, \(C_{M\left(FeCl_2\right)}=\dfrac{0,65}{2,6}=0,25M\)
Đúng 3
Bình luận (0)
X là dung dịch HCl nồng độ x (M). Y là dung dịch
N
a
2
C
O
3
nồng độ y(M). Nhỏ từ từ 100 ml dung dịch X vào 100 ml dung dịch Y, thu được
V
1
lít
C
O
2
(đktc). Nhỏ từ từ 100 ml dung dịch Y vào 100 ml dung dịch X, thu được
V
2
lít
C
O...
Đọc tiếp
X là dung dịch HCl nồng độ x (M). Y là dung dịch N a 2 C O 3 nồng độ y(M). Nhỏ từ từ 100 ml dung dịch X vào 100 ml dung dịch Y, thu được V 1 lít C O 2 (đktc). Nhỏ từ từ 100 ml dung dịch Y vào 100 ml dung dịch X, thu được V 2 lít C O 2 (đktc), biết tỉ lệ V 1 : V 2 = 3 : 5. Tỉ lệ x : y là
A. 5 :3
B. 10 : 7
C. 7 : 5
D. 7 : 3
X là dung dịch HCl nồng độ xM, Y là dung dịch Na2CO3 nồng độ yM. Nhỏ từ từ 100 ml dung dịch X vào 100 ml dung dịch Y, sau phản ứng thu được V1 lít CO2 (đktc). Nhỏ từ từ 100 ml dung dịch Y vào 100 ml dung dịch X, sau phản ứng thu được V2 lít CO2 (đktc). Biết tỉ lệ V1 : V2 4 : 7. Tỉ lệ x : y bằng A. 5 : 3 B. 10 : 7 C. 7 : 5 D. 7 : 3
Đọc tiếp
X là dung dịch HCl nồng độ xM, Y là dung dịch Na2CO3 nồng độ yM. Nhỏ từ từ 100 ml dung dịch X vào 100 ml dung dịch Y, sau phản ứng thu được V1 lít CO2 (đktc). Nhỏ từ từ 100 ml dung dịch Y vào 100 ml dung dịch X, sau phản ứng thu được V2 lít CO2 (đktc). Biết tỉ lệ V1 : V2 = 4 : 7. Tỉ lệ x : y bằng
A. 5 : 3
B. 10 : 7
C. 7 : 5
D. 7 : 3
X là dung dịch HCl nồng độ xM, Y là dung dịch Na2CO3 nồng độ yM. Nhỏ từ từ 100 ml dung dịch X vào 100 ml dung dịch Y, sau phản ứng thu được V1 lít CO2 (đktc). Nhỏ từ từ 100 ml dung dịch Y vào 100 ml dung dịch X, sau phản ứng thu được V2 lít CO2 (đktc). Biết tỉ lệ V1 : V2 4 : 7. Tỉ lệ x : y bằng A. 5 : 3 B. 10 : 7 C. 7 : 5 D. 7 : 3
Đọc tiếp
X là dung dịch HCl nồng độ xM, Y là dung dịch Na2CO3 nồng độ yM. Nhỏ từ từ 100 ml dung dịch X vào 100 ml dung dịch Y, sau phản ứng thu được V1 lít CO2 (đktc). Nhỏ từ từ 100 ml dung dịch Y vào 100 ml dung dịch X, sau phản ứng thu được V2 lít CO2 (đktc). Biết tỉ lệ V1 : V2 = 4 : 7. Tỉ lệ x : y bằng
A. 5 : 3
B. 10 : 7
C. 7 : 5
D. 7 : 3
Cho 11,2(g) Canxi Oxit tác dụng với 100(ml) dung dịch Axit Clohiđric tạo ra Canxi Clorua và Nước A. Tính nồng độ dung dịch Axit Clohidric cần lấy. B. Tính khối lượng Canxi Clorua tạo ra.
\(n_{CaO}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(CaO+2HCl\rightarrow CaCl_2+H_2O\)
\(0.2..........0.4.........0.2\)
\(C_{M_{HCl}}=\dfrac{0.4}{0.1}=4\left(M\right)\)
\(m_{CaCl_2}=0.2\cdot111=22.2\left(g\right)\)
Đúng 2
Bình luận (0)
Cho 7,2 gam Magie tác dụng vừa đủ với 500 ml dung dịch axit clohiđric. a. Viết PTHH của phản ứng. b.Tính nồng độ mol của dung dịch axit clohiđric đã phản ứng. c. Lượng khí hiđro sinh ra ở phản ứng có đủ để khử 16 gam CuO ở nhiệt độ cao?
\(a,n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,3--->0,6------------------->0,3
\(b,C_{M\left(HCl\right)}=\dfrac{0,6}{0,5}=1,2M\\ c,n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
LTL: 0,2 < 0,3 ---> H2 đủ
Đúng 2
Bình luận (0)
\(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\\ pthh:Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
0,3 0,6 0,3
\(C_{M\left(HCl\right)}=\dfrac{0,6}{0,5}=1,2M\\ n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\\ pthh:CuO+H_2\underrightarrow{t^o}Cu+H_2O\\ LTL:\dfrac{0,2}{1}< \dfrac{0,3}{1}\)
=> H2 có khử hết
Đúng 0
Bình luận (0)
Cho 7,2 gam Magie tác dụng vừa đủ với 500 ml dung dịch axit clohiđric. a. Viết PTHH của phản ứng. b.Tính nồng độ mol của dung dịch axit clohiđric đã phản ứng. c. Lượng khí hiđro sinh ra ở phản ứng có đủ để khử 16 gam CuO ở nhiệt độ cao?
\(\begin{array} {l} a)\\ Mg+2HCl\to MgCl_2+H_2\\ b)\\ n_{Mg}=\dfrac{7,2}{24}=0,3(mol)\\ \text{Theo PT: }n_{HCl}=2n_{Mg}=0,6(mol)\\ 500ml=0,5l\\ \to C_{M\,HCl}=\dfrac{0,6}{0,5}=1,2M\\ c)\\ n_{CuO}=\dfrac{16}{80}=0,2(mol)\\ \text{Theo PT: }n_{H_2}=n_{Mg}=0,3(mol)\\ CuO+H_2\xrightarrow{t^o}Cu+H_2O\\ \text{Vì }n_{CuO}<n_{H_2}\to H_2\text{ dư}\\ \text{Vậy lượng hiđro đủ để khử hết }16g\,CuO\end{array}\)
Đúng 3
Bình luận (0)