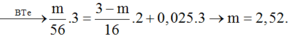Đốt m gam bột sắt trong khí oxi thu được 11,04 gam chất rắn X gồm Fe, Fe3O4, FeO, Fe2O3. Để hòa tan hoàn toàn hỗn hợp cần vừa hết 180 ml dung dịch H2SO4 1M, tạo thành 0,336 lít khí ở đktc. Tính m.

Những câu hỏi liên quan
Đốt m gam bột sắt trong khí oxi thu được 7,36 gam chất rắn X gồm: Fe; FeO; Fe3O4; Fe2O3. Để hoà tan hoàn toàn hỗn hợp X cần vừa hết 120 ml dung dịch H2SO4 1M ( loãng), tạo thành 0,224 l H2 ở đktc.
A.Viết phương trình hoá học xảy ra.
B. Tính m?
Cho Fe = 56, O = 16, Ca = 40, S = 32, C = 12, H = 1
Hỗn hợp gồm Fe,Fe2O3,Fe3O4,FeO (coi hỗn hợp gồm Fe và O )
nFe=0,01 mol
=>nH2SO4 p/ư với Fe =0,01mol
=>nH2SO4 p/ư với oxit=0,11mol
=>n[O]=0,11mol
=> mFe ban đầu =7,36-0,01x16=5,6 g
Khi cho hh Fe,FeO,Fe3O4 vao dd H2SO4 thì thoát ra 0.01 mol H2 nên nFe trong hh =0.01mol
bạn để ý thấy trong oxits sắt thì có bao nhiêu ngtu O thì sẽ có bấy nhiêu gốc SO4 2- kết hợp vs Fe khi cho õit đó vào dd H2SO4 loãng
như vẬY nH2SO4 dùng để hoà tan oxits sắt là 0.12-nH2SO4(hoà tan Fe)=0.12-0.01=0.11
như vậy nO trong ôxuts sắt =nH2SO4 hoà tan ôxits sắt=0.11
nên m=7.36-0,11.16=5.6g
Đúng 0
Bình luận (1)
Đốt m gam bột sắt trong khí oxi thu được 7,36 gam chất rắn X gồm: Fe; FeO; Fe3O4; Fe2O3. Để hoà tan hoàn toàn hỗn hợp X cần vừa hết 120 ml dung dịch H2SO4 1M ( loãng), tạo thành 0,224 l H2 ở đktc.
A.Viết phương trình hoá học xảy ra.
B. Tính m?
Hỗn hợp gồm Fe,Fe2O3,Fe3O4,FeO (coi hỗn hợp gồm Fe và O )
nFe=0,01 mol
=>n H2S04 p/ư với Fe =0,01mol
=>n H2S04 p/ư với oxit=0,11mol
=>n[O]=0,11mol
=> mFe ban đầu =7,36-0,01x16=5,6 g
Đúng 0
Bình luận (1)
Nung m gam bột sắt trong oxi thu được 3,0 gam hỗn hợp chất rắn X gồm Fe, FeO, Fe2O3, Fe3O4. Hòa tan hết hỗn hợp X trong dung dịch HNO3 (dư), thấy thoát ra 0,56 lít khí NO (là sản phẩm khử duy nhất, đo ở đktc). Giá trị của m là A. 2,52. B. 2,10. C. 4,20. D. 2,80.
Đọc tiếp
Nung m gam bột sắt trong oxi thu được 3,0 gam hỗn hợp chất rắn X gồm Fe, FeO, Fe2O3, Fe3O4. Hòa tan hết hỗn hợp X trong dung dịch HNO3 (dư), thấy thoát ra 0,56 lít khí NO (là sản phẩm khử duy nhất, đo ở đktc). Giá trị của m là
A. 2,52.
B. 2,10.
C. 4,20.
D. 2,80.
Nung m gam bột sắt trong oxi thu được 3,0 gam hỗn hợp chất rắn X gồm Fe, FeO, Fe2O3, Fe3O4. Hòa tan hết hỗn hợp X trong dung dịch HNO3 (dư), thấy thoát ra 0,56 lít khí NO (là sản phẩm khử duy nhất, đo ở đktc). Giá trị của m là
A. 2,52.
B. 2,10.
C. 4,20.
D. 2,80.
Hỗn hợp X gồm Al và
Fe
2
O
3
.Nếu cho m gam hỗn hợp X tác dụng với dung dịch HCl dư thu được 2,688 lít khí
H
2
(đktc).Nếu nung nóng m gam hỗn hợp X để thực hiện phản ứng nhiệt nhôm hoàn toàn, thu được chất rắn Y. Hòa tan hết chất rắn Y với dung dịch NaOH dư thu được 0,336 lít
H
2
(đktc).Để hòa tan hết m gam hỗn hợp X cần bao nhiêu...
Đọc tiếp
Hỗn hợp X gồm Al và Fe 2 O 3 .
Nếu cho m gam hỗn hợp X tác dụng với dung dịch HCl dư thu được 2,688 lít khí H 2 (đktc).
Nếu nung nóng m gam hỗn hợp X để thực hiện phản ứng nhiệt nhôm hoàn toàn, thu được chất rắn Y. Hòa tan hết chất rắn Y với dung dịch NaOH dư thu được 0,336 lít H 2 (đktc).
Để hòa tan hết m gam hỗn hợp X cần bao nhiêu ml dung dịch A chứa HCl 1M và H 2 SO 4 0,5M ?
A. 300 ml
B. 225 ml
C. 360 ml
D. 450 ml
Đốt m gam bột sắt trong không khí thu được 6,52 gam chất rắn X gồm Fe, Fe3O4, Fe2O3. Để hoà tan hỗn hợp X cần vừa hết 120ml dung dịch H2SO4 1M, tạo thành 0,224l khí ở đktc. Tính m gam bột sắt ban đầu.
Các PTHH:
X + H2SO4:
Fe + H2SO4 ---> FeSO4 + H2
FeO + H2SO4 ---> FeSO4 + H2O
Fe2O3 + 3H2SO4 ---> Fe2(SO4)3 +3 H2O
Fe3O4 + 4H2SO4 ---> FeSO4 + Fe2(SO4)3 +4 H2O
Ta có: nH2SO4 =1.0,12= 0,12 ( mol)
nH2 =\(\frac{0,224}{22,4}\)= 0,01 (mol)
Hỗn hợp gồm Fe,Fe2O3,Fe3O4,FeO (coi hỗn hợp gồm Fe và O )
nFe=0,01 mol
=>n H2S04 p/ư với Fe =0,01mol
=>n H2S04 p/ư với oxit=0,11mol
=>n[O]=0,11mol
=> mFe ban đầu =6,52-0,01x16=4,92 g
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 17,04 gam hỗn hợp gồm Fe ; FeO ; Fe3O4 và Fe2O3 trong 660 ml dung dịch HCl 1M dư thu được dung dịch A và 1,68 lít H2 (đktc). Cho AgNO3 dư vào A thấy thoát ra 0,336 lít khí NO (sản phẩm khử duy nhất) và tạo thành m gam kết tủa. Giá trị của m là : A. 102,81 gam. B. 94,20 gam. C. 99,06 gam. D. 94,71 gam.
Đọc tiếp
Hòa tan hoàn toàn 17,04 gam hỗn hợp gồm Fe ; FeO ; Fe3O4 và Fe2O3 trong 660 ml dung dịch HCl 1M dư thu được dung dịch A và 1,68 lít H2 (đktc). Cho AgNO3 dư vào A thấy thoát ra 0,336 lít khí NO (sản phẩm khử duy nhất) và tạo thành m gam kết tủa. Giá trị của m là :
A. 102,81 gam.
B. 94,20 gam.
C. 99,06 gam.
D. 94,71 gam.
Chọn đáp án A
4H+ + NO3– + 3e → NO + 2H2O ⇒ nH+ dư = 4nNO = 0,06 mol.
Bảo toàn nguyên tố Hidro: nH2O = (0,66 - 0,06 - 0,075 × 2) ÷ 2 = 0,225 mol.
Quy hỗn hợp ban đầu về Fe và O ⇒ nO = nH2O = 0,225 mol.
⇒ nFe = (17,04 - 0,225 × 16) ÷ 56 = 0,24 mol. Bảo toàn electron cả quá trình:
3nFe = 2nO + 2nH2 + 3nNO + nAg ⇒ nAg = 0,075 mol.
► Kết tủa gồm 0,075 mol Ag và 0,66 mol AgCl
⇒ m = 0,075 × 108 + 0,66 × 143,5 = 102,81(g) ⇒ chọn A
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 17,04 gam hỗn hợp gồm Fe ; FeO ; Fe3O4 và Fe2O3 trong 660 ml dung dịch HCl 1M dư thu được dung dịch A và 1,68 lít H2 (đktc). Cho AgNO3 dư vào A thấy thoát ra 0,336 lít khí NO (sản phẩm khử duy nhất) và tạo thành m gam kết tủa. Giá trị của m là A. 102,81 gam. B. 94,20 gam. C. 99,06 gam. D. 94,71 gam.
Đọc tiếp
Hòa tan hoàn toàn 17,04 gam hỗn hợp gồm Fe ; FeO ; Fe3O4 và Fe2O3 trong 660 ml dung dịch HCl 1M dư thu được dung dịch A và 1,68 lít H2 (đktc). Cho AgNO3 dư vào A thấy thoát ra 0,336 lít khí NO (sản phẩm khử duy nhất) và tạo thành m gam kết tủa. Giá trị của m là
A. 102,81 gam.
B. 94,20 gam.
C. 99,06 gam.
D. 94,71 gam.
+ + NO3– + 3e → NO + 2H2O ⇒ nH+ dư = 4nNO = 0,06 mol.
Bảo toàn nguyên tố Hidro: nH2O = (0,66 - 0,06 - 0,075 × 2) ÷ 2 = 0,225 mol.
Quy hỗn hợp ban đầu về Fe và O ⇒ nO = nH2O = 0,225 mol.
⇒ nFe = (17,04 - 0,225 × 16) ÷ 56 = 0,24 mol. Bảo toàn electron cả quá trình:
3nFe = 2nO + 2nH2 + 3nNO + nAg ⇒ nAg = 0,075 mol.
► Kết tủa gồm 0,075 mol Ag và 0,66 mol AgCl
⇒ m = 0,075 × 108 + 0,66 × 143,5 = 102,81(g)
Đáp án A
Đúng 0
Bình luận (0)
Để m (g) bột sắt ngoài không khí một thời gian thu được 12 gam hỗn hợp các chất rắn FeO, Fe3O4, Fe2O3, Fe. Hòa tan hoàn toàn hỗn hợp đó bằng dung dịch HNO3 loãng thu được 2,24 lít khí NO duy nhất (đktc). a) Tính m . b) tính m muối tạo thành
Chỉ đáp án thôi ạ em đang cần gấp
Quy đổi hỗn hợp thành : Fe ( x mol ) , O ( y mol )
\(m=56x+16y=12\left(g\right)\left(1\right)\)
Bảo toàn e :
\(3x=0.1\cdot3+2y\left(2\right)\)
\(\left(1\right),\left(2\right):x=0.18,y=0.12\)
\(m_{Fe}=0.18\cdot56=10.08\cdot\left(g\right)\)
\(m_{Fe\left(NO_3\right)_3}=0.18\cdot242=43.56\left(g\right)\)
Đúng 4
Bình luận (0)
a)
Coi hỗn hợp gồm Fe(x mol) và O(y mol)
Ta có :
$56x + 16y = 12$
Bảo toàn e : $3x - 2y = 0,1.3$
Suy ra x = 0,18 ; y = 0,12
$m = 0,18.56 = 10,08(gam)$
b)
$n_{Fe(NO_3)_3} = 0,18(mol)$
$m_{Fe(NO_3)_3} = 0,18.242 = 43,56(gam)$
Đúng 2
Bình luận (0)