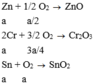Cho 6,72lit hh X( O2 & Cl2) co ti khoi so vs H2 la 22,5 td vua du vs hh Y (Al va Mg) thu duoc 23,7g hh clorua va oxit cua 2 kim loai. Tinh % ve khoi luong cac chat trong X va Y

Những câu hỏi liên quan
hòa tan hỗn hợp gồm 0,65 mol Mg và 0,2 mol Fe vào 2400 ml dung dịch HNO3 1m vừa đủ Sau phản ứng thu được 6,72lit hh khí X gồm N2O,NO2,N2.% theo thể tích của N2 trong X
Ta có: \(n_{N_2O}+n_{NO_2}+n_{N_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\left(1\right)\)
BT e, có: 2nMg + 3nFe = 8nN2O + nNO2 + 10nN2
⇒ 8nN2O + nNO2 + 10nN2 = 1,9 (2)
Có: nHNO3 = 10nN2O + 2nNO2 + 12nN2 = 2,4.1 = 2,4 (mol) (3)
Từ (1), (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}n_{N_2O}=0,1\left(mol\right)\\n_{NO_2}=0,1\left(mol\right)\\n_{N_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%V_{N_2}=\dfrac{0,1.22,4}{6,72.}100\%\approx33,33\%\)
Đúng 2
Bình luận (0)
\(n_{N_2O}=a\left(mol\right)\)
\(n_{NO_2}=b\left(mol\right)\)
\(n_{N_2}=c\left(mol\right)\)
\(\Rightarrow n_X=a+b+c=\dfrac{6.72}{22.4}=0.3\left(mol\right)\left(1\right)\)
Bảo toàn e :
\(8a+b+10c=0.65\cdot2+0.2\cdot3=1.9\left(2\right)\)
\(n_{H^+}=10a+2b+12c=2.4\left(mol\right)\left(3\right)\)
\(\left(1\right),\left(2\right),\left(3\right):a=b=c=0.1\left(mol\right)\)
\(\%V_{N_2}=\dfrac{0.1}{0.3}\cdot100\%=33.33\%\)
Đúng 1
Bình luận (0)
cho 11,2 g fe vào 400 ml dung dịch Fe(NO3)2 0,8M, phản ứng hoàn toàn dung dịch chứa m gam chất tan.tính giá trị m
Đúng 0
Bình luận (0)
Đốt một lượng nhôm trong 6,72 lít O2(đktc). Sau khi kết thúc phản ứng cho chất rắn thu đc hoà ta hoàn toàn vào dd H2SO4 loãng dư , thấy giải phóng ra 6,72lit H2(đktc) .Khối lượng nhôm đã dùng là:
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
0,4 0,3 0,2 ( mol )
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\) ( không giải phóng H2)
=> Chất rắn tạo ra H2 là Al
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,2 0,3 ( mol )
\(\Rightarrow m_{Al}=\left(0,2.27\right)+\left(0,4.27\right)=16,2g\)
Đúng 2
Bình luận (0)
Trộn m gam khí CH4 với m gam khí O2 thu dc hh X . Tỉ số mol của khí CH4 và khí O2 trong hh X tương ứng là
nCH4=\(\dfrac{m}{16}\), mol
nO2=\(\dfrac{m}{32}\), mol
=>\(\dfrac{nO2}{nCH4}\)=\(\dfrac{m}{32}:\dfrac{m}{16}\)=\(\dfrac{1}{2}\)
Đúng 2
Bình luận (0)
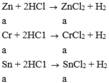
Cho m gam hh bột X gồm ba kim loại Zn, Cr, Sn có số mol bằng nhau t/d hết với lượng dư dd HCl loãng, nóng thu được dd Y và khí H2. Cô cạn dd Y thu được 8,98 gam muối khan. Nếu cho m gam hh X t/d hoàn toàn với O2 (dư) để tạo hh 3 oxit thì thể tích khí O2 (đktc) pư là A. 2, 016 lít. B. 1,008 lít. C. 0,672 lít. D. 1,344 lít.
Đọc tiếp
Cho m gam hh bột X gồm ba kim loại Zn, Cr, Sn có số mol bằng nhau t/d hết với lượng dư dd HCl loãng, nóng thu được dd Y và khí H2. Cô cạn dd Y thu được 8,98 gam muối khan. Nếu cho m gam hh X t/d hoàn toàn với O2 (dư) để tạo hh 3 oxit thì thể tích khí O2 (đktc) pư là
A. 2, 016 lít.
B. 1,008 lít.
C. 0,672 lít.
D. 1,344 lít.
1 hh khí X gồm CO2 và O2 có tỉ khối so với khí metan bằng 2,5. thêm V lít khí O2 và 30 lít hh X thu đc hh Y có tỉ khối so với khí metan bằng 2,25. tính V
1 hh khí X gồm CO2 và O2 có tỉ khối so với khí metan bằng 2,5. thêm V lít khí O2 và 30 lít hh X thu đc hh Y có tỉ khối so với khí metan bằng 2,25. tính V
\(M_X=2,5.16=40\)(g/mol)
\(\rightarrow\dfrac{V_{CO_2}}{V_{O_2}}=\dfrac{n_{CO_2}}{n_{O_2}}=\dfrac{40-32}{44-40}=2\)
Mà \(V_{CO_2}+V_{O_2}=30\left(L\right)\)
\(\rightarrow V_{CO_2}=20\left(L\right);V_{O_2}=10\left(L\right)\)
\(\rightarrow M_Y=\dfrac{20.44+10.32+32V}{V+20+10}=2,25.16=36\)
\(\rightarrow V=30\left(L\right)\)
Đúng 2
Bình luận (0)
Cho hh x gồm 3 este đơn chức .Đốt cháy m gam x cần vừa đủ 0.465 mol O2 , sản phẩm cháy thu đc chứa x mol CO2.Thủy phân m gam x trong 90ml dd NaOH 1M ( vừa đủ ) thì thu được 8.86 gam hh muối Y và ancol Z no đơn hở . Đem đốt cháy hoàn toàn hh muối Y thì cần vừa đủ 7.392 l O2 . x là
hh X gồm những khí sau: H2, O2, NOx. bt rằng hh X
-tỉ lệ về thể tích của H2 chiếm 25%, O2 chiếm 50%, còn lại là NOx
-tỉ lệ về khối lượng NOx chiếm 31,25%
a) xác định cthh của NOx
b) tính tỷ khối của X so vs O2
Cho 6,72lit khí etilen và propilen qua dd Br2 thì thấy dd nhạt màu hoàn toàn và khong có khí thoát ra, Khối lượng đ sau pư tăng 9,8g , tính thaafnh phần phần trăm khối luwowjg mõi khí trong hh?
C2H4: a mol, C3H6: b mol
Ta có hệ: a+b=0,3
28a+42b=9,8
\(\Rightarrow\)a=0,2 , b=0,1
%\(V_{C2H4}\)=\(\dfrac{0,2.100}{0,2+0,1}\)=66,67
%\(V_{C3H6}\)=33,33
Đúng 0
Bình luận (2)