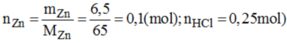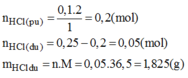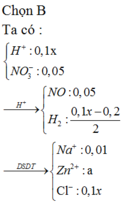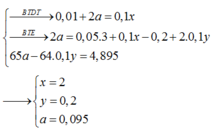Cho 6,5g kẽm vào bình chứa dung dich HCl, sau phản ứng thấy khối lượng của bình tăng 6,34g. Hỏi miếng kẽm còn hay hết? Vì sao?![]()

Những câu hỏi liên quan
Cho 6,5g kẽm vào bình dung dịch chứa 0,25mol axit clohidric. Sau phản ứng còn dư chất nào? Khối lượng là bao nhiêu gam?
cho 6,5g kẽm vào bình dd chứa 0,25mol HCl
a,tính thể tích khí H (ĐKTC)
b,sau phản ứng chất naò còn dư khối lượng là bao nhiêu
a) \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,25}{2}\) => Zn hết, HCl dư
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,1--->0,2------------>0,1
=> VH2 = 0,1.22,4 = 2,24 (l)
b) mHCl(dư) = (0,25 - 0,2).36,5 = 1,825 (g)
Đúng 9
Bình luận (0)
Cho 6,5g kẽm vào dung dịch có chứa 7,3g axit clohiđric (HCl). Sau phản ứng tạo thành muối
kẽm clorua (ZnCl2) và 0,2g khí hiđro.
a. Lập phương trình hóa học của phản ứng trên
b. Tính khối lượng muối kẽm clorua tạo thành
\(a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ b,\text {Bảo toàn KL: }m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\\ \Rightarrow m_{ZnCl_2}=6,5+7,3-0,2=13,6(g)\)
Đúng 2
Bình luận (0)
cho 6,5g zn vào bình đựng dung dịch chứa 0,25 mol HCl thu đc muối kẽm clorua
a tính thể tích khíH2(đktc)thu được
b tính khối lượng muối kẽm clorua thu được
\(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.1.......0.2..........0.1.......0.1\)
\(V_{_{ }H_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(m_{ZnCl_2}=0.1\cdot136=13.6\left(g\right)\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 5,91 gam NaCl và KBr vào 100 ml dung dịch hỗn hợp Cu(NO3)2 0,1M và AgNO3 a mol/l, thu được 11,38 gam kết tủa. Cho miếng kẽm vào dung dịch Y, sau khi phản ứng xong lấy miếng kẽm ra khỏi dung dịch, thấy khối lượng miếng kẽm tăng 1,1225 gam. Giá trị của a là: A. 0,85 B. 0,5 C. 0,775 D. 0,7
Đọc tiếp
Hòa tan hoàn toàn 5,91 gam NaCl và KBr vào 100 ml dung dịch hỗn hợp Cu(NO3)2 0,1M và AgNO3 a mol/l, thu được 11,38 gam kết tủa. Cho miếng kẽm vào dung dịch Y, sau khi phản ứng xong lấy miếng kẽm ra khỏi dung dịch, thấy khối lượng miếng kẽm tăng 1,1225 gam. Giá trị của a là:
A. 0,85
B. 0,5
C. 0,775
D. 0,7
Đáp án A
Khi cho kẽm vào dung dịch Y, sau khi phản ứng xong thì thấy khối lượng thanh kẽm tăng nên trong Y phải có ion Ag+. Do AgNO3 dư nên đặt

Đúng 0
Bình luận (0)
Nhúng thanh kẽm vào bình chứa 100 ml dung dịch HCl xM, NaNO3 0,1M và Cu(NO3)2 yM . Sau khi kết thúc các phản ứng, nhấc thanh kẽm ra thấy cân lại thấy khối lượng giảm 4,895 gam. Biết khí NO là sản phẩm khử duy nhất của N+5. Giá trị của (x+y) là
A. 2M
B. 2,2M
C. 2,25M
D. 2,5M
Nhúng thanh kẽm vào bình chứa 100 ml dung dịch HCl xM, NaNO3 0,1M và Cu(NO3)2 yM . Sau khi kết thúc các phản ứng, nhấc thanh kẽm ra thấy cân lại thấy khối lượng giảm 4,895 gam. Biết khí NO là sản phẩm khử duy nhất của N+5. Giá trị của x là
A. 1M
B. 2M
C. 1,25M
D. 1,5M
Nhúng một thanh kẽm vào dung dịch chứa 8,5 gam AgNO3. Sau phản ứng thấy khối lượng thanh kẽm tăng lên 8% so với khối lượng ban đầu. Xác định khối lượng thanh kẽm ban đầu?
PT: \(Zn+2AgNO_3\rightarrow Zn\left(NO_3\right)_2+2Ag\)
Ta có: \(n_{AgNO_3}=\dfrac{8,5}{170}=0,05\left(mol\right)\)
Theo PT: \(n_{Zn\left(pư\right)}=\dfrac{1}{2}n_{AgNO_3}=0,025\left(mol\right)\)
\(n_{Ag}=n_{AgNO_3}=0,05\left(mol\right)\)
Có: m tăng = mAg - mZn (pư) = 0,05.108 - 0,025.65 = 3,775 (g)
Mà: m tăng = 8%mZn ban đầu
⇒ m Zn ban đầu = 47,1875 (g)
Đúng 0
Bình luận (0)
Cho 6,5g kẽm vào dung dịch HCl.
a) Viêt phương trình hóa học.
b)Tính khối lượng của hidro. Biết khối lượng của chất sau phản ứng gấp 6,3 lần khối lượng chất trước phản ứng.
a/ PTHH: Zn + 2HCl ===> ZnCl2 + H2
b/
Đúng 0
Bình luận (2)