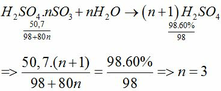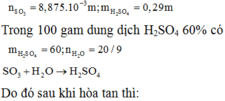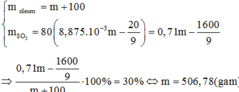Cho 25,8g một oleum X hòa tan trong 174,2g H2O thu được dung dịch H2SO4 14,7%. Xác định công thức oleum X, tính C% khối lượng SO3 trong X

Những câu hỏi liên quan
Oleum X có công thức H2SO4.aSO3, trong đó So3 chiếm 71% về khối lượng .
a. Xác định a
b. Cần bao nhiêu gam oleum cho vào 147g dd H2SO4 40% để thu được oleum Y, trong đó So3 chiếm 10% về khối lượng
Ta có công thức tổng quát của Oleum là H2SO4.nSO3
SO3 chiếm 71% về khối lượng
⇒ (80n/98 + 80n).100% = 71%
⇔ (80n/98 + 80n) = 0,71
⇒ 80n = 0,71.(98+80n)
⇔ 23,2n = 69,58
⇔ n = 3
⇒ CTHH của Oleum X là H2SO4.3SO3
Đúng 1
Bình luận (0)
Hòa tan 50,7 gam oleum có công thức H2SO4.nSO3 vào nước, thu được 98 gam dung dịch H2SO4 60%. Xác định giá trị n. H2SO4 nguyên chất có khả năng hấp thụ SO3 tạo oleum theo phương trình sau: H2SO4 + nSO3 → H2SO4.nSO3 (oleum)
Đọc tiếp
Hòa tan 50,7 gam oleum có công thức H2SO4.nSO3 vào nước, thu được 98 gam dung dịch H2SO4 60%. Xác định giá trị n.
H2SO4 nguyên chất có khả năng hấp thụ SO3 tạo oleum theo phương trình sau:
H2SO4 + nSO3 → H2SO4.nSO3 (oleum)
6. Khi hấp thụ SO3 vào dd H2SO4 đặc , người ta thu đc 1 loại oleum có công thức H2SO4.nSO3. Biết rằng , trong loại oleum trên chứa 36,7% về khối lượng là nguyên tố lưu huỳnh. Công thức của loại oleum trên là?
10. Một loại oleum có công thức H2SO4.nSO3 chứa 37,21% về khối lượng là nguyên tố lưu huỳnh. Hoà tan 25,8g loại oleum trên vào 74,2g nước thu đc dd X có nồng độ a%. Giá trị của a là?
12. Một loại oleum chứa 55,05% về khối lượng là SO3. Hoà tan 21,8g loại oleum trên vào 103,2g nước thì th...
Đọc tiếp
6. Khi hấp thụ SO3 vào dd H2SO4 đặc , người ta thu đc 1 loại oleum có công thức H2SO4.nSO3. Biết rằng , trong loại oleum trên chứa 36,7% về khối lượng là nguyên tố lưu huỳnh. Công thức của loại oleum trên là?
10. Một loại oleum có công thức H2SO4.nSO3 chứa 37,21% về khối lượng là nguyên tố lưu huỳnh. Hoà tan 25,8g loại oleum trên vào 74,2g nước thu đc dd X có nồng độ a%. Giá trị của a là?
12. Một loại oleum chứa 55,05% về khối lượng là SO3. Hoà tan 21,8g loại oleum trên vào 103,2g nước thì thu đc dd X có nồng độ c%. Giá trị của c là?
Câu 6:
Ta có:
\(\%m_S=\frac{32\left(n+1\right)}{98+80n}=36,7\%\)
\(\Leftrightarrow n=1,5\)
Vậy oleum này có dạng H2SO4.1,5SO3
Câu 10:
Hàm lượng S trong oleum trên là \(\%m_S=\frac{32\left(n+1\right)}{98+80n}=37,21\%\Leftrightarrow n=2\)
Oleum là H2SO4.2SO3
Ta có:
\(n_{oleum}=\frac{25,8}{98+80.2}=0,1\left(mol\right)\)
\(\Rightarrow n_{H2SO4}=3n_{oleum}=0,3\left(mol\right)\Rightarrow m_{H2SO4}=0,3.98=29,4\left(g\right)\)
\(m_{dd\left(X\right)}=25,8+74,2=100\left(g\right)\)
\(\Rightarrow C\%_{H2SO4}=\frac{29,4}{100}.100\%=29,4\%\)
Câu 12:
Gọi CTTQ của oleum là H2SO4.nSO3
\(\%_{SO3}=\frac{80n}{98+80n}.100\%=55,05\%\)
\(\Leftrightarrow n=1,5\)
\(n_{oleum}=\frac{21,8}{218}=0,1\left(mol\right)\)
\(PTHH:H_2SO_4.1,5SO_3+1,5H_2O\rightarrow2,5H_2SO_4\)
\(\Rightarrow n_{H2SO4}=n_{oleum}.2,5=0,1.2,5=0,25\left(mol\right)\)
\(m_{dd\left(spu\right)}=21,8+103,2=125\left(g\right)\)
\(\Rightarrow C\%_{H2SO4}=\frac{0,25.98}{125}.100\%=19,6\%\)
Đúng 0
Bình luận (0)
Cho 4,98 gam oleum hòa tan vào nước thu được dung dịch A. Để trung hòa hết A cần 600ml Ba(OH)2 0,1M thu được m gam kết tủa.
a, Xác định công thức của oleum
b, Tính khối lượng kết tủa ?
c, Tính khối lượng oleum cần để hòa tan vào 500ml nước tạo thành dung dịch H2SO4 20%
H2SO4.nSO3+H2O --> (n+1)H2SO4
H2SO4+Ba(OH)2 -> BaSO4 + 2H2O
a.nBaSO4= 0,06 mol
=> nH2SO4=0,06 mol
ta có PT
\(\dfrac{4,98}{98+80n}=\dfrac{0,06}{n+1}\)
=> n=5. CT H2SO4.5SO3
b. mBaSO4= 0,06*233=13,98(g)
c)a mol H2SO4 5SO3
=> mol SO3 = 5a và H2SO4 a mol
SO3 + H2O --> H2SO4
5a--------5a----------5a
=> mol H2SO4 6a mol => mH2SO4 = 588a
=>
m dd sau hòa tan = mH2O + mA = 500 + 498a
Bảo toàn m H2SO4: 588a = 0,2(500 + 498a) => a => mA = 498a
Đúng 3
Bình luận (1)
Khối lượng oleum chứa 71% SO3 về khối lượng cần lấy để hòa tan vào 100 gam dung dịch H2SO4 60% thì thu được oleum chứa 30% SO3 về khối lượng là: A. 312,56 gam B. 539,68 gam C. 506,78 gam D. 496,68 gam
Đọc tiếp
Khối lượng oleum chứa 71% SO3 về khối lượng cần lấy để hòa tan vào 100 gam dung dịch H2SO4 60% thì thu được oleum chứa 30% SO3 về khối lượng là:
A. 312,56 gam
B. 539,68 gam
C. 506,78 gam
D. 496,68 gam
Khối lượng oleum chứa 71% SO3 về khối lượng cần lấy để hòa tan vào 100 gam dung dịch H2SO4 60% thì thu được oleum chứa 30% SO3 về khối lượng là: A. 312,56 gam B. 539,68 gam C. 506,78 gam D. 496,68 gam
Đọc tiếp
Khối lượng oleum chứa 71% SO3 về khối lượng cần lấy để hòa tan vào 100 gam dung dịch H2SO4 60% thì thu được oleum chứa 30% SO3 về khối lượng là:
A. 312,56 gam
B. 539,68 gam
C. 506,78 gam
D. 496,68 gam
axit H2SO4 100% hấp thụ SO3 tạo ra oleum theo phương trình H2SO4 + SO3 -> H2SO4.nSO3 . Hòa tan 6,76 gam gam oleum vào nước thành 200 ml dung dịch H2SO4 . 10 ml dung dịch trung hòa vừa hết 16 ml dung dịch NaOH 0,5 M a- tính n b- tính hàm lượng % SO3 trong oleum c- cần có bao nhiêu gam oleum có hàm lượng SO3 như trên để pha vào 100 ml dung dịch H2SO4 40% , d= 1,31 g/ml để tạo ra oleum có hàm lượng SO3 là 10%.
H2SO4 + nSO3 => H2SO4.nSO3
H2SO4.nSO3 + nH2O >> n+1H2SO4
H2SO4 + 2NaOH >> Na2SO4 + 2H2O
Số mol NaOH = 0,008 , số mol H2SO4 200ml = 0,008/2 . 200/10 =0,08
Theo (2) nH2SO4.nSO3 =0,08/n+1
MH2SO4.nSO3 =98 +80n = 6,76/0,08/n+1 =84,5n+ 84,5
13,5 =4,5n
=>n=3
%SO3=3.80/2.80+98 =71%
c,Theo câu b , hàm lượng % của SO3 có trong oleum trên là 71
Cứ 100g oleum có 71g SO3 và 29g H2SO4 Khi đó mdd = 1,31.100 = 131g
a g có 71a/100 ...............29a/100
Vì dd H2SO4 có C=40%
Cứ 100g dd có 40g H2SO4 và 60g H2O
=>131g >> 131.40/100 = 52,4g H2SO4 và 131.60/100 = 78,6 g H2O
Khi cho oleum vào dd H2SO4 thì SO3+H2O
SO3 + H2O >> H2SO4
Cứ 80g cần 18g >> 98g
Vậy ..x..g cần 78,6g >>..y..g
x= 78,6.80/18 = 349,3g
y= 78,6.98/18 = 427,9g
Trong loại oleum mới 10% thì mSO3 = 71a/100 -349,3g
và mH2SO4 = 29a/100 +52,4+ 427,9
=> 71a/100 -349,4 / 29a/100 +480,3 = 10/90
=> Bạn ấn máy tìm a nhé
Đúng 1
Bình luận (0)
Có 1 loại oleum X trong đó SO3 chiếm 70% theo khối lượng. Tính khối lượng nước cần thêm vào 100 gam oleum trên để thu được dung dịch mới trong đó H2SO4 chiếm 80% theo khối lượng A. 16,2 B. 21,6 C. 10,8 D. 8,8
Đọc tiếp
Có 1 loại oleum X trong đó SO3 chiếm 70% theo khối lượng. Tính khối lượng nước cần thêm vào 100 gam oleum trên để thu được dung dịch mới trong đó H2SO4 chiếm 80% theo khối lượng
A. 16,2
B. 21,6
C. 10,8
D. 8,8
Đáp án : C
Xét 100g Oleum có 70g SO3 và 30g H2SO4
Khi hòa tn vào nước thu được dung dịch có H2SO4 chiếm 80%
=> SO3 chiếm 20%
n S = n H 2 S O 4 + n S O 3 = 1,18 mol
Dung dịch sau :
⇒ n H 2 S O 4 = 0 , 9 m o l
=> n H 2 S O 4 m ớ i = n H 2 S O 4 s a u - n H 2 S O 4 đ ầ u = 0 , 6 m o l = n H 2 O
=> m H 2 O = 10,8g
Đúng 0
Bình luận (0)
Hấp thụ hết 0,15 mol SO3 bằng H2SO4 đặc, thu đc 1 loại hợp chất oleum X. Cho X vào nước, thu đc dung dịch Y. Để trung hòa Y cần dùng 50 ml KOH 8M, thu đc khôi trung hòa. Tính phần trăm khối lượng cua nguyên tố oxi trong oleum trên.
n KOH = 0,05.8 = 0,4(mol)
$2KOH + H_2SO_4 \to K_2SO_4 + 2H_2O$
n H2SO4 = 1/2 n KOH = 0,2(mol)
X : H2SO4.nSO3
$H_2SO_4 + n SO_3 \to H_2SO_4.nSO_3$
$H_2SO_4.nSO_3 + nH_2O \to (n + 1)H_2SO_4$
Theo PTHH :
n X = 1/n .n SO3 = 0,15/n(mol)
n X = 1/(n + 1) .n H2SO4 = 0,2/(n + 1)
Suy ra : 0,15/n = 0,2/(n + 1)
=> n = 3
Vậy X là H2SO4.3SO3
%O = 16.13/338 .100% = 61,54%
Đúng 1
Bình luận (0)