Hòa tan dung dịch KOH 15,33M. Biết rằng để pha chế 1l dung dịch trêm cần dùng 731,52g H2O .Tính C%

Những câu hỏi liên quan
Cho 21,7 gam Na2O hòa tan H2O để được 450 ml dung dịch bazơ
A) tính nồng độ mol của dung dịch 3 giờ pha chế
B) tính thể tích dung dịch HNO3 30% cần dùng để trung hòa dung dịch bazơ trên(D=1,08g/ml)
nNa2O = 21.7 : 62 = 0.35 mol
Na2O + H2O => 2NaOH
mol : 0.35 -> 0.7
CM NaOH = 0.7 : 0.45 = 1.6 M
NaOH + HNO3 => NaNO3 + H2O
mol : 0.7 => 0.7
VHNO3 30% = 0.7 x 63 : 30% : 1.08 = 136.1 ml
Đúng 0
Bình luận (0)
Tính khối lượng chất tan cần dùng để pha chế các dung dịch sau:
a. 300 ml dung dịch KCl 2M.
b. 20 gam dung dịch NaOH 25%.
c. 100 gam dung dịch MgCl2 bão hòa biết độ tan của MgCl2 là 53,6 gam.
a) \(n_{KCl}=0,3.2=0,6\left(mol\right)\)
=> \(m_{KCl}=0,6.74,5=44,7\left(g\right)\)
b) \(m_{NaOH}=20.25\%=5\left(g\right)\)
c) \(S=\dfrac{m_{ct}}{m_{dd}}.100\)
=> \(53,6=\dfrac{m_{MgCl_2}}{100}.100\)
=> mMgCl2 = 53,6 (g)
Đúng 3
Bình luận (0)
a) Trong 200 ml dung dịch CuSO4 có hòa tan 16gam CuSO4. Hãy tính nồng độ mol của dung dịch trên.b)Tính số gam chất tan cần dùng để pha chế 2lít dung dịch NaCl 0,9M.
Đọc tiếp
a) Trong 200 ml dung dịch CuSO4 có hòa tan 16gam CuSO4. Hãy tính nồng độ mol của dung dịch trên.
b)Tính số gam chất tan cần dùng để pha chế 2lít dung dịch NaCl 0,9M.
a)
$n_{CuSO_4} = \dfrac{16}{160} = 0,1(mol)$
$C_{M_{CuSO_4}} = \dfrac{0,1}{0,2} = 0,5M$
b)
$n_{NaCl} = 0,9.2 = 1,8(mol)$
$m_{NaCl} = 1,8.58,5 = 105,3(gam)$
Đúng 2
Bình luận (0)
tính khối lượng K2O và khối lượng dung dịch KOH 8% cần dùng để pha chế được 653g dung dịch KOH 28%
Coi K2O là dd có nồng độ là 100%
Gọi khối lượng K2O cần dùng m1 gam (m1>0)
Khối lượng dd KOH 8% cần dùng là m2 gam (m2>0)
Ta có quy tắc đường chéo:

=> \(\dfrac{m1}{m2}=\dfrac{20}{72}=\dfrac{5}{18}\)
=> 5m2= 18m1 <=> 5m2 - 18m1=0
T có hệ phương trình: \(\left\{{}\begin{matrix}5m_2-18m_1=0\\m_2+m_1=653\end{matrix}\right.\)
=> m1= 141,957 (g) ; m2= 511,043 (g)
Vậy cần 141,957 gam K2O và 511,043 gam dd KOH để pha chế được 652 gam dd KOH 28%
Đúng 0
Bình luận (1)
a) Hòa tan 2g NaCl trong 80g H2O . Tính nồng độ phần trăm của dung dịch
b) Chuyển sang nồng độ phần trăm dung dịch NaOH 2M có khối lượng riêng D = 1,08 g/ml
c) Cần bao nhiêu gam NaOH để pha chế được 3 lít dung dịch NaOH 100/0 biết khối lượng riêng của dung dịch là 1,115 g/ml
a)
m dd = 2 + 80 = 82(gam)
C% NaCl = 2/82 .100% = 2,44%
b) Coi V dd = 100(ml)
Ta có :
m dd = D.V = 1,08.100 = 108(gam)
n NaOH = 0,1.2 = 0,2(mol)
Suy ra : C% NaOH = 0,2.40/108 .100% = 7,41%
Đúng 4
Bình luận (1)
c)
m dd = 1,115.3.1000 = 3345(gam)
m NaOH = m dd . C% = 3345.10% = 334,5(gam)
Đúng 4
Bình luận (1)
Hòa tan 50 gam đường vào nước , đựng dung dịch đường cs nồng độ 25% . Hãy tính a) khối lượng dung dịch đường pha chế được b) khối lượng nc cần dùng cho sự pha chế
a) khối lượng dung dịch đường pha chế được:
\(m_{dd}=\dfrac{m_{ct}\times100}{C\%}=\dfrac{50\times100}{25}=200\left(g\right)\)
b) khối lượng nc cần dùng cho sự pha chế:
\(m_{H_2O}=m_{dd}-m_{ct}=200-50=150\left(g\right)\)
Đúng 6
Bình luận (0)
\(a) \)\(m_{dd}= \dfrac{ m_{ct} }{C} \)\(\%\)\(.100\)\(\%\)\( = \dfrac{ 50 }{25}.100\)\(\%\)\(=200(g) \)
\(b)\) \(m_{H_2O}= m_{dd}- m_{ct}=200-50=150(g)\)
Đúng 4
Bình luận (0)
Tính số gam chất tan cần dùng để pha chế mỗi dung dịch sau:
a) 2,5 lít dung dịch NaCl 0,9M.
b) 50g dụng dịch MgCl2 4%.
c) 250ml dung dịch MgSO4 0,1M.
Số gam chất tan cần dùng để pha chế các dung dịch:
a) nNaCl = CM .V = 2,5.0,9 = 2,25 (mol)
→ mNaCl = 2,25.(23 + 35,5) = 131,625 (g)
b) 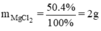
c) nMgSO4 = 0,1.0,25 = 0,025 (mol)
→ mMgSO4 = 0,025.(24 + 64 + 32) = 3 (g)
Đúng 1
Bình luận (0)
Tính số gam chất tan cần dùng để pha chế mỗi dung dịch sau: a)2,5 lít dung dịch NaCl 0,9M b)50 g dung dịch MgCl2 4% c)250 ml dung dịch MgSO4 0,1M
a)
$n_{NaCl} = 2,5.0,9 = 2,25(mol)$
$m_{NaCl} = 2,25.58,5 = 131,625(gam)$
b)
$m_{MgCl_2} = 50.4\% = 2(gam)$
c)
$n_{MgSO_4} = 0,25.0,1 = 0,025(mol)$
$m_{MgSO_4} = 0,025.120= 3(gam)$
Đúng 3
Bình luận (1)
Hòa tan 50 g CuSO 4 vào nước được dung dịch có nồng độ 20 %. Tính khối lượng dung dịch thu được ? Tính khối lượng nước cần dùng cho sự pha chế ?
\(m_{dd}=\dfrac{50.100}{20}=250\left(g\right)\\ \rightarrow m_{H_2O}=250-50=200\left(g\right)\)
Đúng 2
Bình luận (0)






















