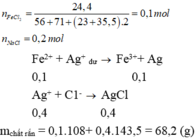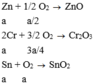Đun sôi a gam một trigilxerit X với lượng dư dd NaOH cho đến khi pư xảy ra hoàn toàn thu đc 0,92g glixerol và 9,12g muối. Để hidro hoá hoàn toàn a gam X thì số mol H2 cần cho pư là?

Những câu hỏi liên quan
Đun sôi a gam 1 triglixerit X với lượng dư dd KOH cho đên khi pư xảy ra hoàn toàn thu đc 0,92g glixerol và 9,62g hỗn hợp muối của axit oleic và axit stearic. Để hidro hoá hoàn toàn a gam X thì số mol H2 cần cho pư là?
Ta có :
$n_X = n_{glixerol} = \dfrac{0,92}{92} = 0,01(mol)$
Gọi CTHH của X là : \(\left(C_{17}H_{33}COO\right)_a\left(C_{17}H_{35}COO\right)_{3-a}C_3H_5\)
Ta có :
\(n_{C_{17}H_{33}COOK}=0,01a\left(mol\right)\\ n_{C_{17}H_{35}COOK}=0,01\left(3-a\right)=0,03-0,01a\left(mol\right)\)
Suy ra:
0,01a.320 + (0,03 - 0,01a).322 = 9,62
Suy ra: a = 2
Do đó X có 2 liên kết C=C
Suy ra: $n_{H_2} = 2n_X = 0,02(mol)$
Đúng 1
Bình luận (1)
Xà phòng hoá hoàn toàn 66,6g một hỗn hợp 2 este gồm: HCOOC2H5 và CH3COOCH3 bằng dd NaOH , sau pư thu đc hỗn hợp X gồm 2 ancol. Đun nóng hỗn hợp X với H2SO4 đặc ở 140°C sau khi pư xảy ra hoàn toàn thu đc m gam nước. Giá trị của m là?
Theo gt ta có: $n_{este}=0,9(mol)$
$\Rightarrow n_{ancol}=0,9(mol)$
$\Rightarrow n_{H_2O}=\frac{1}{2}.n_{ancol}=0,45(mol)\Rightarrow m=8,1(g)$
Đúng 2
Bình luận (0)
$HCOOC_2H_5 + NaOH \to HCOONa + C_2H_5OH$
$CH_3COOCH_3 + NaOH \to CH_3COONa + CH_3OH$
$2C_2H_5OH \xrightarrow{t^o,xt} C_2H_5OC_2H_5 + H_2O$
$2CH_3OH \xrightarrow{t^o,xt} CH_3OCH_3 + H_2O$
$M_{HCOOC_2H_5} = M_{CH_3COOCH_3} = 74$
$n_{ancol} = n_{este} = \dfrac{66,6}{74} = 0,9(mol)$
$n_{H_2O} = \dfrac{1}{2}n_{ancol} = 0,45(mol)$
$m = 0,45.18 = 8,1(gam)$
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn a mol X là trieste của glixerol vs các axit đơn chức mạch hở) thu đc b mol CO2 và c mol H2O( b-c =4a) . Hiđrô hoá hoàn toàn m gam X cần 4,48 lít H2 thu đc 20,4g Y (este no) . Đun nóng m gam X với lượng dư dd chứa AgNO3/NH3 , đun nóng thì có x mol AgNO3 pư. Biết rằng các pư xảy ra hoàn toàn . Giá trị x là?
CTTQ của este là CnH2n+2-2k-2zO2z với k là số liên kết pi giữa C và C, z là số nhóm chức este.
=> CTTQ của X là: CnH2n-2k-4O6
CnH2n-2k-4O6 + O2 → nCO2 + (n - k -2)H2O
Theo đề bài ta có: n - (n - k -2) = 4
<=> k = 2
Vậy X sẽ phản ứng với H2 theo tỉ lệ 1 : 2
=> nX = 1/2nH2 = 0,1 mol = nY
BTKL => mX = mY - mH2 = 20gam
=> MX = 20:0,1 = 200
X có dạng (\(\overline{R}\)COO)3C3H5
=> \(\overline{R}\) = 27
Vì X có phản ứng tráng gương và 2 liên kết pi C với C => X tạo bởi 2 axit đơn chức là HCOOH và 1 axit đơn chức CH\(\equiv\)C-COOH
=> X sẽ phản ứng được với 4AgNO3 /NH3
<=> x = 4a = 0,4
Đúng 2
Bình luận (0)
Hoà tan hoàn toàn 24,4 gam hh gồm FeCl2 và NaCl (có tỉ lệ số mol tương ứng là 1:2) vào một lượng nước (dư), thu được dd X. Cho dd AgNO3 (dư) vào dd X, sau khi pư xảy ra hoàn toàn sinh ra m gam chất rắn. Giá trị của m là A. 57,4 B. 28,7 C. 10,8 D. 68,2
Đọc tiếp
Hoà tan hoàn toàn 24,4 gam hh gồm FeCl2 và NaCl (có tỉ lệ số mol tương ứng là 1:2) vào một lượng nước (dư), thu được dd X. Cho dd AgNO3 (dư) vào dd X, sau khi pư xảy ra hoàn toàn sinh ra m gam chất rắn. Giá trị của m là
A. 57,4
B. 28,7
C. 10,8
D. 68,2
Đốt cháy hoàn toàn m gam 1 triglixerit A cần vừa đủ a mol O2 sau pư thu đc CO2 và b mol H2O . Biết m= 78a -103b. Nếu cho x mol A tác dụng vs dd nước dư thì lượng br2 pư tối đa là 0,3 mol . Giá trị x ?
Bảo toàn khối lượng :
$m_{CO_2} = 78a - 103b + 32a - 18b = 110a - 121b(gam)$
$n_{CO_2} = 2,5a - 2,75b(mol)$
Bảo toàn O :
$n_A = \dfrac{2(2,5a -2,75b) + b -2a)}{6} = 0,5a - 0,75b(mol)$
Ta có :
$n_{CO_2} - n_{H_2O} = 2,5a - 3,75b = (k - 1).n_A$
Suy ra : k = 6
Suy ra số liên kết C=C = 6 - 3 = 3
Suy ra:
$n_{Br_2} = 3n_A \Rightarrow x = 0,3 : 3 = 0,1(mol)$
Đúng 1
Bình luận (0)
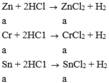
Cho m gam hh bột X gồm ba kim loại Zn, Cr, Sn có số mol bằng nhau t/d hết với lượng dư dd HCl loãng, nóng thu được dd Y và khí H2. Cô cạn dd Y thu được 8,98 gam muối khan. Nếu cho m gam hh X t/d hoàn toàn với O2 (dư) để tạo hh 3 oxit thì thể tích khí O2 (đktc) pư là A. 2, 016 lít. B. 1,008 lít. C. 0,672 lít. D. 1,344 lít.
Đọc tiếp
Cho m gam hh bột X gồm ba kim loại Zn, Cr, Sn có số mol bằng nhau t/d hết với lượng dư dd HCl loãng, nóng thu được dd Y và khí H2. Cô cạn dd Y thu được 8,98 gam muối khan. Nếu cho m gam hh X t/d hoàn toàn với O2 (dư) để tạo hh 3 oxit thì thể tích khí O2 (đktc) pư là
A. 2, 016 lít.
B. 1,008 lít.
C. 0,672 lít.
D. 1,344 lít.
Cho 6,72 l Co2 t/d vs 100ml dd chứa Naoh 1,5 ml và KOh 2M thì thu đc dd X. Thêm dd CaCl2 dư vào toàn bộ X thì đc m gam kết tủa. tính m. bt các pư xảy ra hoàn toàn
\(n_{CO_2}=0,3\left(mol\right)\\ n_{OH^-}=1,5.0,1+0,1.2=0,35\left(mol\right)\\ 2>T=\dfrac{n_{OH^-}}{n_{CO_2}}=\dfrac{0,35}{0,3}=\dfrac{7}{6}>1\\ PTHH:CO_2+2OH^-\rightarrow CO^{2-}_3+H_2O\left(1\right)\\CO_2+OH^-\rightarrow HCO^-_3\left(2\right)\\ Đặt:n_{CO_2\left(1\right)}=a\left(mol\right);n_{CO_2\left(2\right)}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}a+b=0,3\\2a+b=0,35\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,05\\b=0,25\end{matrix}\right.\\ \Rightarrow Tạo:CO^{2-}_3,HCO^-_3\\ Ca^{2+}+CO^{2-}_3\rightarrow CaCO_3\downarrow\\ n_{CaCO_3}=n_{CO^{2-}_3}=a=0,05\left(mol\right)\\ m=m_{CaCO_3}=0,05.100=5\left(g\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 0,32 mol O2 thu đc 0,228 mol CO2 và 0,208 mol h2o. Mặt khác cho a gam X vào 45ml NaOH 0,1M và KOH 0,1M sau pư cô cạn dd thu đc chât rắn chứa m gam muối khan. Giá trị m?
Bảo toàn khối lượng : $a = 0,208.18 + 0,228.44 - 0,32.32 = 3,536(gam)$
Bảo toàn nguyên tố với O : $n_X = \dfrac{0,208 + 0,228.2 - 0,32.2}{6} =0,004(mol)$
$n_{NaOH} = 0,0045(mol) ; n_{KOH} = 0,0045(mol)$
Coi hỗn hợp bazo là $ROH$
Ta có : $M_{ROH} = R + 17 = \dfrac{0,0045.40 + 0,0045.56}{0,0045 + 0,0045} = 48$
Ta có : $n_{C_3H_5(OH)_3} = n_X = 0,004(mol)$
$n_{bazo\ pư} = 3n_X = 0,004.3 = 0,012(mol)$
Bảo toàn khối lượng : $m_{muối} = 3,536 + 0,012.48 - 0,004.92 = 3,744(gam)$
Đúng 1
Bình luận (0)
Hiđro hoá hoàn toàn m gam hỗn hợp chất béo X cần vừa đủ 0,15 mol H2 thì thử đc hỗn hợp chất béo Y. Đốt cháy hoàn toàn Y cần dùng 9,15 mol O2 thu đc H2O và 6,42 mol CO2. Mặt khác thủy phân hoàn toàn m gam X trong dd KOH ( dư) thu đc a gam muối. Giá trị của a là?
Gọi $n_X = n_Y = x(mol)$
Gọi $n_{H_2O} = y(mol)$
Gọi k là độ bất bão hòa của chất béo X
Ta có :
$x(k - 3) = 0,15$
$2x = 6,42 - y$
Bảo toàn O : $6x + 9,15.2 = 6,42.2 + y$
Suy ra: xk = 0,51 ; x = 0,12 ; y = 6,18
Bảo toàn khối lượng : $m_Y = 6,18.18 + 6,42.44 - 9,15.32 = 100,92(gam)$
$m_X = 100,92 - 0,15.2 = 100,62(gam)$
$a = 100,62 + 0,12.3.56 - 0,12.92 = 109,74(gam)$
Đúng 3
Bình luận (1)