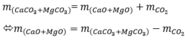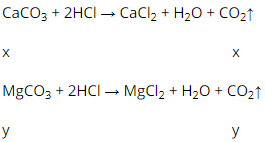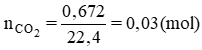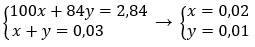nhiệt phân hoàn toàn hỗn hợp A gồm MgCO3 và CaCO3 thu được 11,2 l CO2 và 2,2 g hỗn hợp B oxit của Mg và Ca. Tính hàm lượng CaCO3 có trong hỗn hợp? Tính khối lượng HCl cần để tác dụng hết với hỗn hợp ban đầu?

Những câu hỏi liên quan
Chia 1 lượng hỗn hợp gồm MgCO3 và CaCO3 thành 2 phần bằng nhau.
Phần 1 nhiệt phân hoàn toàn thu được 3.36 l khí CO2 đktc
Phần 2 hòa tan hết trong dd HCl, sau đó cô cạn dd thu được 15.85g hỗn hợp muối khan.
Tính % về khối lượng của các muối trong hỗn hợp ban đầu
MgCO3 ----> MgO + CO2
CaCO3 -----> CaO + CO2
0,15 (mol) <------------ 0,15 (mol) (1) đây ý nói là tổng lượng mol CO2 = tổng lượng hỗn hợp muối
MgCO3 + HCl -------> MgCl2 + CO2 + H20
CaCO3 + HCl --------> CaCl2 + CO2 + H20
=> n(MgCO3,CaCO3) = n(MgCl2,CaCl2) = 0,15 (mol)
=> M(MgCl2,CaCl2) = 317/3
Sau đó, ta đặt: C (là phần trăm của CaCl2 trong hỗn hợp muối)
1-C (là phần trăm của MgCl2 trong hỗn hợp muối)
Với C là 100% trong hỗn hợp đó
=> 111C + 95x(1-C) = 317/3
Từ đó suy ra: C= 2/3
Vì lượng muối trong hỗn hợp tác dụng với HCl bằng lượng từng muối trong hỗn hợp ban đầu nên
%CaCO3 = 2/3x100% = 66,667%
%MgCO3 = 1/3x100% = 33,33%
Đúng 0
Bình luận (0)
Cho 2,84g hỗn hợp
C
a
C
O
3
và
M
g
C
O
3
tác dụng hết với dung dịch HCl thu được 0,03 mol khí
C
O
2
. Thành phần % theo khối lượng của
C
a
C
O
3
và
M
g
C
O
3
trong hỗn hợp lần lượt là A. 70,4% và 29,6%. B. 29,6% và 70,4%. C. 59,15% và 40,85%. ...
Đọc tiếp
Cho 2,84g hỗn hợp C a C O 3 và M g C O 3 tác dụng hết với dung dịch HCl thu được 0,03 mol khí C O 2 . Thành phần % theo khối lượng của C a C O 3 và M g C O 3 trong hỗn hợp lần lượt là
A. 70,4% và 29,6%.
B. 29,6% và 70,4%.
C. 59,15% và 40,85%.
D. 40,85% và 59,15%.
Nung hỗn hợp X gồm
C
a
C
O
3
và
M
g
C
O
3
theo phản ứng :
C
a
C
O
3
→
t
°
C
a
O
+
C
O
2
M
g
C
O
3
→
t
°
M
g...
Đọc tiếp
Nung hỗn hợp X gồm C a C O 3 và M g C O 3 theo phản ứng :
C a C O 3 → t ° C a O + C O 2
M g C O 3 → t ° M g O + C O 2
Nếu đem nung 31,8 gam hỗn hợp X thì thu được 7,84 lít C O 2 (đktc). Tính khối lượng của hỗn hợp của oxit thu được.
hòa tan hoàn toàn hỗn hợp gồm Fe và MgCO3 bằng dung dịch HCl dư, thu đc hỗn hợp khí A gồm H2 và CO2. nếu cũng lượng hỗn hợp trteen tác dụng hết vs dung dịch H2SO4 đặc nóng dư thu đc hỗn hợp khí B gồm SO2 và CO2. tỉ khối hơi của B đối vs A là 3,6875. tính % khối lượng Fe và MgCO3
Nung hỗn hợp gồm 2 muối CaCO3 và MgCO3 thu được 76 g 2 oxit và 66g CO2 (đktc). Tính khối lượng hỗn hợp 2 muối ban đầu
$CaCO_3 \xrightarrow{t^o} CaO + CO_2$
$MgCO_3 \xrightarrow{t^o} MgO + CO_2$
Áp dụng định luật bảo toàn khối lượng :
$m_{muối} = m_{oxit} + m_{CO_2} = 76 + 66 = 142(gam)$
Đúng 4
Bình luận (0)
Cho 2,84 g hỗn hợp CaCO3 và MgCO3 tác dụng hết với dung dịch HCl thấy bay ra 672 ml khí CO2 (đktc). Phần trăm khối lượng của hai muối( CaCO3 , MgCO3) trong hỗn hợp là :
A. 35,2 % và 64,8%.
B. 70,4% và 29,6%.
C. 85,49% và 14,51%.
D. 17,6% và 82,4%.
Đáp án B.
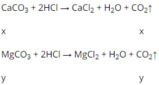
Số mol CO2: 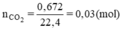
Gọi x, y lần lượt là số mol của CaCO3 và MgCO3 trong hỗn hợp
Theo bài ra ta có hệ phương trình:
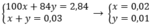
%mNa = 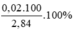 = 70,42%
= 70,42%
%mK = 100% - 70,42% = 29,58%
Đúng 0
Bình luận (0)
Cho 2,84 g hỗn hợp CaCO3 và MgCO3 tác dụng hết với dung dịch HCl thấy bay ra 672 ml khí CO2 (đktc). Phần trăm khối lượng của hai muối (CaCO3, MgCO3) trong hỗn hợp là
A. 35,2% và 64,8%.
B. 70,4% và 29,6%.
C. 85,49% và 14,51%.
D. 17,6% và 82,4%.
Số mol CO2:
Gọi x, y lần lượt là số mol của CaCO3 và MgCO3 trong hỗn hợp
Theo bài ra ta có hệ phương trình:
%mNa = 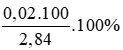
%mK = 100% - 70,42% = 29,58%
Chọn B
Đúng 1
Bình luận (0)
Câu 1: Hòa tan hoàn toàn 12,725g hỗn hợp Mg, Al, Zn bằng dung dịch HCl thu được dung dịch A và 11,2 l H2 ở đktc. Tính khối lượng muối có trong dung dịch A.
Câu 2: Cho 11,8g hỗn hợp Cu, Al tác dụng với khí õi thu được 18,2g hỗn hợp oxit. Tính % khối lượng của Cu trong hỗn hợp ban đầu.
Câu 2 :
\(n_{Cu}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(m=64a+27b=11.8\left(g\right)\left(1\right)\)
\(BTKL:m_{O_2}=18.2-11.8=6.4\left(g\right)\)
\(n_{O_2}=\dfrac{6.4}{32}=0.2\left(mol\right)\)
\(2Cu+O_2\underrightarrow{^{^{t^0}}}2CuO\)
\(4Al+3O_2\underrightarrow{^{^{t^0}}}2Al_2O_3\)
\(n_{O_2}=0.5a+0.75b=0.2\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.2\)
\(\%Cu=\dfrac{0.1\cdot64}{11.8}\cdot100\%=54.23\%\)
Đúng 1
Bình luận (0)
Câu 1 :
\(n_{HCl}=2n_{H_2}=2\cdot\dfrac{11.2}{22.4}=1\left(mol\right)\)
\(BTKL:\)
\(m_{Muối}=12.725+1\cdot36.5-0.5\cdot2=48.225\left(g\right)\)
Đúng 1
Bình luận (0)
Nhiệt phân hoàn toàn 1,84 gam hỗn hợp X gồm MgCO3 và CaCO3 thu được 0,448 lít khí ở đktc. Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp X ban đầu.
Gọi số mol MgCO3, CaCO3 là a, b (mol)
=> 84a + 100b = 1,84 (1)
PTHH: MgCO3 --to--> MgO + CO2
a-------------------->a
CaCO3 --to--> CaO + CO2
b-------------------->b
=> a + b = \(\dfrac{0,448}{22,4}=0,02\) (2)
(1)(2) => a = 0,01 (mol); b = 0,01 (mol)
=> \(\left\{{}\begin{matrix}\%m_{MgCO_3}=\dfrac{0,01.84}{1,84}.100\%=45,65\%\\\%m_{CaCO_3}=\dfrac{0,01.100}{1,84}.100\%=54,35\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)