Hạt proton, neutron nặng hơn hạt electron bao nhiêu lần?

Những câu hỏi liên quan
Nguyên tử X có tổng số hạt proton,neutron và electron là 48. Số hạt proton bằng số hạt neutron. Em hãy cho biết a. Số hạt mỗi loại trong nguyên tử X b. Tính khối lượng nguyên tử X c. Vẽ mô hình nguyên tử X, cho biết X có mấy lớp electron, có bao nhiêu electron lớp ngoài cùng?
`#3107.101107`
a.
Gọi số hạt proton, neutron, electron trong nguyên tử X lần lượt là `p, n, e`
Tổng số hạt trong nguyên tử X là `48`
`=> p + n + e = 48`
Mà trong nguyên tử, số `p = e`
`=> 2p + n = 48`
Mà số hạt `p = n`
`=> 3p = 48`
`=> p = 48 \div 3`
`=> p = 16`
Vậy, số `p = n = e = 16`
b.
Khối lượng nguyên tử X là: `16 + 16 = 32` (amu)
c.
Bạn tham khảo mô hình NT X:
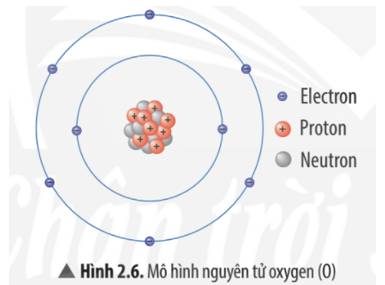
- X có `3` lớp electron
- X có `6` electron lớp ngoài cùng.
Đúng 3
Bình luận (0)
Hợp chất A có công thức M4X3. Tổng số hạt proton, electron và neutron trong phân tử A là 214. Tổng số hạt proton, neutron, electron của [M]4 nhiều hơn so với [X] 3 trong A là 106.
a) Xác định công thức hóa học của A
b) Viết cấu hình electron của các nguyên tử tạo nên A
a, Ta có: P = E (Do nguyên tử trung hòa về điện)
- Tổng số hạt p, n, e trong A là 214.
⇒ 4.2PM + 4NM + 3.2PX + 3NX = 214 (1)
- Tổng số hạt p, n, e của [M]4 nhiều hơn so với [X]3 trong A là 106.
⇒ 4.2PM + 4NM - 3.2PX - 3NX = 106 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}2P_M+N_M=40\\2P_X+N_X=18\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}N_M=40-2P_M\\N_X=18-2P_X\end{matrix}\right.\)
Luôn có: \(1\le\dfrac{N}{P}\le1,5\)
\(\Rightarrow\left\{{}\begin{matrix}P_M\le40-2P_M\le1,5P_M\\P_X\le18-2P_X\le1,5P_X\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}11,4\le P_M\le13,3\\5,1\le P_X\le6\end{matrix}\right.\)
⇒ PM = 12 (Mg) hoặc PM = 13 (Al)
PX = 6 (C)
Mà: A có CTHH dạng M4X3 nên A là Al4C3.
b, Al: 1s22s22p63s23p1
C: 1s22s22p2
Đúng 2
Bình luận (0)
Nguyên tử X có tổng số hạt cơ bản electron, proton, neutron bằng 18. Biết trong tự nhiên, các đồng vị bền luôn có tỉ lệ . Xác định số hạt electron, proton, neutron của nguyên tử X.
Ta có: P + N + E = 18
Mà: P = E (do nguyên tử trung hòa về điện)
⇒ 2P + N = 18 ⇒ N = 18 - 2P
Luôn có: \(1\le\dfrac{N}{P}\le1,5\) \(\Rightarrow P\le18-2P\le1,5P\)
\(\Rightarrow5,14\le P\le6\)
⇒ P = E = 6
N = 6
Đúng 0
Bình luận (0)
Một ion XO43- có tổng số hạt proton, neutron, electron là 145, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 49. Tìm tên X?
một nguyên tử của nguyên tố có tổng số hạt proton notron và electron là 28 . Số Neutron trong nguyên tử khối là bao nhiêu
Câu 1: Trong nguyên tử, loại hạt nào có khối lượng không đáng kể so với các hạt còn lại? A. electron. B. neutron và electron. C. neutron. D. proton.
Câu 1: Trong nguyên tử, loại hạt nào có khối lượng không đáng kể so với các hạt còn lại? A. electron. B. neutron và electron. C. neutron. D. proton.
Đúng 1
Bình luận (0)
Trong nguyên tử X có tổng số hạt proton, neutron, electron là 24. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 8 hạt. Số electron lớp ngoài cùng của nguyên tử X là:
A. 6
D. 4
B. 2
C. 8
Ta có: P + N + E = 24
Mà: P = E (do nguyên tử trung hòa về điện)
⇒ 2P + N = 24 (1)
- Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 8.
⇒ 2P - N = 8 (2)
Từ (1) và (2) ⇒ P = E = N = 8
Cấu hình e: 1s22s22p4
→ Số e lớp ngoài cùng là 6.
Đáp án: A
Đúng 0
Bình luận (0)
Đây là nguyên tử oxygen nên số lớp electron ngoài cùng là 6
Chọn: A
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Nguyên tử của nguyên tố X có tổng số hạt cơ bản (proton, electron, neutron) là 49, trong đó số hạt không mang điện bằng 53,125% số hạt mang điện. Xác định điện tích hạt nhận, số proton, số electron, số neutron và số khối của X?
Ta có Nguyên tử của nguyên tố X có tổng số hạt cơ bản là 49:
=> 2Z + N = 49 (1)
Lại có, số hạt không mang điện bằng 53,125% số hạt mang điện:
=>N = 2Z x 53,125% = 1716Z
<=>17Z – 16N = 0 (2)
Từ (1) & (2) ta có: 2Z + N = 49
17Z – 16N = 0
=> Z=16 N =17
Vậy nguyên tử nguyên tố X có : điện tích hạt nhân là 16+, 16 proton, 16 electron, 17 neutron và có số khối là 33.
Đúng 1
Bình luận (0)
nguyên tử của nguyên tố X có tổng số hạt proton,neutron,electron là 52,trong đó số hạt không mang điện hơn số hạt mang điện âm là 1 hạt.số khối của nguyên tử X là?
\(2p+n=52\\ n-e=n-p=1\\ p=\dfrac{51}{3}=17\\ n=52-34=18\\ A_X=17+18=35\)
Đúng 1
Bình luận (0)





















