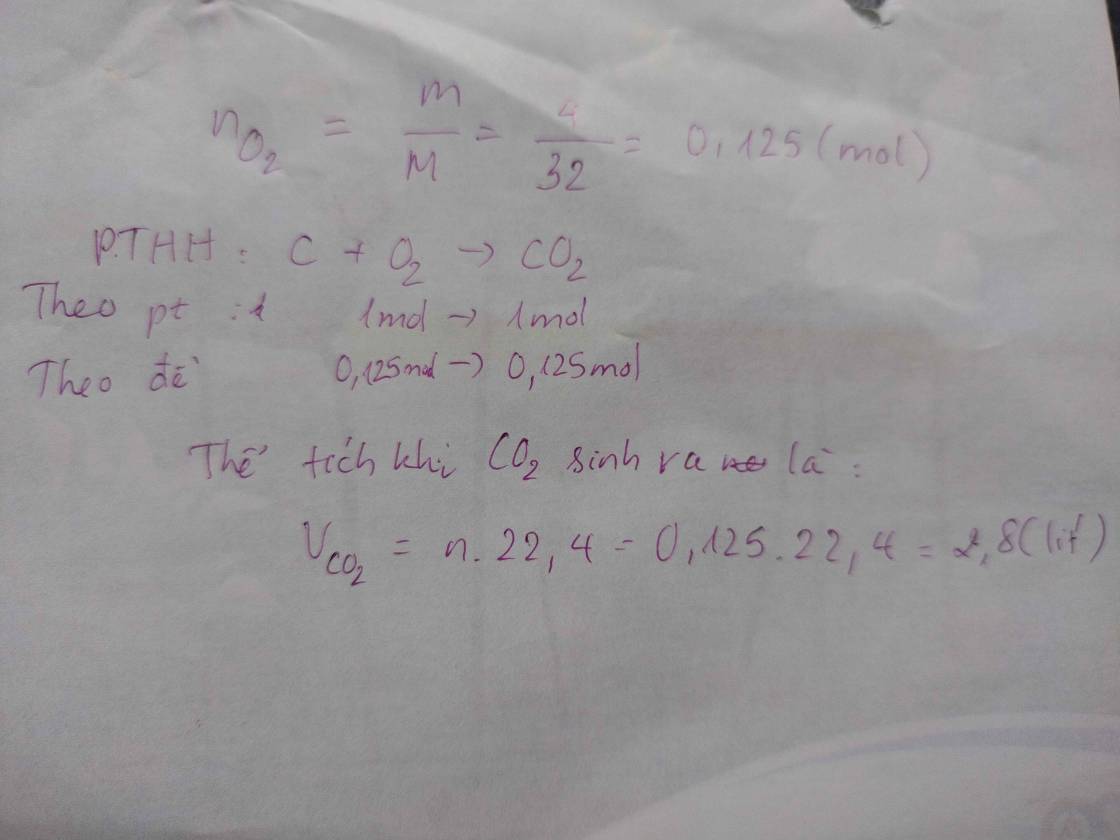Tính hiệu suất phản ứng khi đốt 12 gam carbon trong khí oxygen thu được 39,6 gam, CO2 biết phản ứng xảy ra theo phương trình: C + O2 = CO2

Những câu hỏi liên quan
Đốt 12g carbon trong oxygen dư thu được 39.6 g carbon dioxide CO2 theo pthh C + O2 suy ra CO2 Tính hiệu suất của phản ứng trên
`#3107.101107`
PTHH: \(\text{ C}+\text{O}_2\) \(\underrightarrow{\text{ }\text{ }\text{ }\text{ }\text{t}^0\text{ }\text{ }\text{ }}\) \(\text{CO}_2\)
Số mol của C là:
\(n_C=\dfrac{m_C}{M_C}=\dfrac{12}{12}=1\left(\text{mol}\right)\)
Theo PT: `1` mol C thu được 1 mol \(\text{CO}_2\)
Vậy, n \(\text{CO}_2\) là 1 mol
m của \(\text{CO}_2\) là:
\(\text{m}_{\text{CO}_2}=\text{n}_{\text{CO}_2}\cdot\text{M}_{\text{CO}_2}=1\cdot44=44\left(\text{g}\right)\)
Hiệu suất của phản ứng trên là:
\(\text{H}=\dfrac{\text{ m}'_{\text{CO}_2}}{\text{m}_{\text{CO}_2}}=\dfrac{39,6}{44}\cdot100=90\%\)
Đúng 1
Bình luận (2)
cho 1.2 gam cacbon cháy hết trong khí oxi sau phản ứng thu được khi cacbondioxit (co2)
theo sơ đồ phản ứng : C + O2 ---> CO2
a. lập phương trình phản ứng
b. tính khối lượng cacbondioxit (CO2) tạo thành
c. tính thể tích O2 tham gia phản ứng (đktc)
Bài 5: Đốt cháy hoàn toàn 5,6 gam hỗn hợp khí X gồm C,H, và C,Hg .Sau phản ứng thu được 16,5 gam CO2 . a. Viết phương trình phản ứng hoá học xảy ra . b. Tính thành phần phần trăm theo khối lượng của mỗi khí có trong hỗn hợp X. c. Hai chất khí trong hỗn hợp khí X nói trên, thì chất khí nào có thể làm mất màu dung dịch brom. Vi sao?
Carbon cháy trong khí oxygen hoặc trong không khí sinh ra khí carbon dioxxide: C + O2 → CO2 Hãy tìm thể tích khí carbon dioxide (đktc) sinh ra nếu có 4 gam khí oxi tham gia phản ứng
Đun nóng 27,40 gam CH3CHBrCH2CH3 với KOH dư trong C2H5OH, sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp khí X gồm hai olefin trong đó sản phẩm chính chiếm 80%, sản phẩm phụ chiếm 20%. Đốt cháy hoàn toàn X thu được bao nhiêu lít CO2 (đktc)? Biết các phản ứng xảy ra với hiệu suất phản ứng là 100%. A. 4,48 lít. B. 8,96 lít. C. 11,20 lít. D. 17,92 lít.
Đọc tiếp
Đun nóng 27,40 gam CH3CHBrCH2CH3 với KOH dư trong C2H5OH, sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp khí X gồm hai olefin trong đó sản phẩm chính chiếm 80%, sản phẩm phụ chiếm 20%. Đốt cháy hoàn toàn X thu được bao nhiêu lít CO2 (đktc)? Biết các phản ứng xảy ra với hiệu suất phản ứng là 100%.
A. 4,48 lít.
B. 8,96 lít.
C. 11,20 lít.
D. 17,92 lít.
Đáp án D
Hướng dẫn:
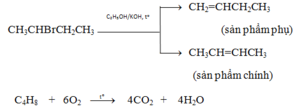
Khi đun nóng CH3CHBrCH2CH3 với KOH dư trong C2H5OH thì thu được hai sản phẩm hữu cơ là:
but-1-en và but-2-en.
Phương trình phản ứng :
Theo các phương trình phản ứng và giả thiết ta thấy:

Đúng 0
Bình luận (0)
Đun nóng 27,40 gam CH3CHBrCH2CH3 với KOH dư trong C2H5OH, sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp khí X gồm hai olefin trong đó sản phẩm chính chiếm 80%, sản phẩm phụ chiếm 20%. Đốt cháy hoàn toàn X thu được bao nhiêu lít CO2 (đktc)? Biết các phản ứng xảy ra với hiệu suất phản ứng là 100%. A. 4,48 lít B. 8,96 lít. C. 11,20 lít. D. 17,92 lít.
Đọc tiếp
Đun nóng 27,40 gam CH3CHBrCH2CH3 với KOH dư trong C2H5OH, sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp khí X gồm hai olefin trong đó sản phẩm chính chiếm 80%, sản phẩm phụ chiếm 20%. Đốt cháy hoàn toàn X thu được bao nhiêu lít CO2 (đktc)? Biết các phản ứng xảy ra với hiệu suất phản ứng là 100%.
A. 4,48 lít
B. 8,96 lít.
C. 11,20 lít.
D. 17,92 lít.
Đáp án D
Khi đun nóng CH3CHBrCH2CH3 với KOH dư trong C2H5OH thì thu được hai sản phẩm hữu cơ là but-1-en và but-2-en (đều có CTPT là C4H8).
C4H8 + 6O2 → t o 4CO2 + 4H2O
![]()
Vậy V C O 2 = 0 , 8 . 22 , 4 = 17 , 92 l í t lít.
Đúng 0
Bình luận (0)
Nung 16,8 gam magnesium carbonate (MgCO3), thu được khí carbon dioxide (CO2) và 6 gam magnesium oxide (MgO). Tính hiệu suất phản ứng ?
`#3107.101107`
Khối lượng mol của \(\text{MgCO}_3\) là:
\(\text{M}_{\text{MgCO}_3}=24+12+16\cdot3=84\left(\text{mol}\right)\)
Số mol của \(\text{MgCO}_3\) là:
\(\text{n}_{\text{MgCO}_3}=\dfrac{\text{m}_{\text{MgCO}_3}}{\text{M}_{\text{MgCO}_3}}=\dfrac{16,8}{84}=0,2\left(\text{mol}\right)\)
PTHH: \(\text{MgCO}_3\text{ }\underrightarrow{t^0}\text{ CO}_2+\text{MgO}\)
Theo PT: 1 : 1 : 1 (mol)
`=>` n của MgO là `0,2` mol
Khối lượng của MgO thu được là:
\(\text{m}_{\text{MgO}}=\text{n}_{\text{MgO}}\cdot\text{ M}_{\text{MgO}_2}=0,2\cdot\left(24+16\right)=0,2\cdot40=8\left(\text{g}\right)\)
Hiệu suất của pứ trên là:
\(\text{H = }\dfrac{\text{m'}}{\text{m}}\cdot100=\dfrac{6}{8}\cdot100=75\%\)
Vậy, hiệu suất của phản ứng trên là `75%.`
Đúng 1
Bình luận (0)
1. Chọn chất thích hợp điền vào chỗ trống rồi cân bằng phương trình Na + O2 - .....Al2O3 + ...... - AlCl3 + H2O........ + NaCl - AgCl + NaNO3CuSO4 + NaOH - Na2SO4 + .......2. Cho Đá vôi có thành phần chính là Canxi cacbonat (CaCO3) vào dung dịch axit Clohiđric (HCl) phản ứng tạo thành Canxi Clorua (CaCl2), Nước và khí Cacbon đioxi (CO2)a. Viết phương trình phản ứng xảy rab. Nếu cho 12 (g) CaCO3 phản ứng với 7,3 (g) HCl thu được 11,1 (g) CaCl2, 1,8 (g) Nước và được 4,4(g) CO2. Tính độ tinh kh...
Đọc tiếp
1. Chọn chất thích hợp điền vào chỗ trống rồi cân bằng phương trình
Na + O2 -> .....
Al2O3 + ...... -> AlCl3 + H2O
........ + NaCl -> AgCl + NaNO3
CuSO4 + NaOH -> Na2SO4 + .......
2. Cho Đá vôi có thành phần chính là Canxi cacbonat (CaCO3) vào dung dịch axit Clohiđric (HCl) phản ứng tạo thành Canxi Clorua (CaCl2), Nước và khí Cacbon đioxi (CO2)a. Viết phương trình phản ứng xảy rab. Nếu cho 12 (g) CaCO3 phản ứng với 7,3 (g) HCl thu được 11,1 (g) CaCl2, 1,8 (g) Nước và được 4,4(g) CO2. Tính độ tinh khiết của canxi cacbonat trong mẫu đá vôi trên. Biết rằng tạp chất không tham gia phản ứng.c. Nếu có 200 phân tử CaCO3 phản ứng thì cần bao gam HCl và tạo thành bao nhiêm gam CaCl2
3. Đốt cháy hoàn toàn hỗn hợp gồm 2,4 gam C và 9,6 gam S trong khí oxi sau phản ứng thu được 8,8 gam CO2 và 19,2 gam SO2. Tính khối lượng của Oxi tham cần dùng.
4. Cho sơ đồ phản ứng. Fe + O2 -> Fe3O4
a. Cân bằng phương trình phản ứng trên
b. Nếu có 6x10^23 phân tử O2 phản ứng thì có bao nhiêu phân tử Fe3O4 được tạo thành và bao nhiêu gam Fe tham gia phản ứng.
Na + O2 -> .....
Al2O3 + ...... -> AlCl3 + H2O
........ + NaCl -> AgCl + NaNO3
CuSO4 + NaOH -> Na2SO4 + .......
2. Cho Đá vôi có thành phần chính là Canxi cacbonat (CaCO3) vào dung dịch axit Clohiđric (HCl) phản ứng tạo thành Canxi Clorua (CaCl2), Nước và khí Cacbon đioxi (CO2)a. Viết phương trình phản ứng xảy rab. Nếu cho 12 (g) CaCO3 phản ứng với 7,3 (g) HCl thu được 11,1 (g) CaCl2, 1,8 (g) Nước và được 4,4(g) CO2. Tính độ tinh khiết của canxi cacbonat trong mẫu đá vôi trên. Biết rằng tạp chất không tham gia phản ứng.c. Nếu có 200 phân tử CaCO3 phản ứng thì cần bao gam HCl và tạo thành bao nhiêm gam CaCl2
3. Đốt cháy hoàn toàn hỗn hợp gồm 2,4 gam C và 9,6 gam S trong khí oxi sau phản ứng thu được 8,8 gam CO2 và 19,2 gam SO2. Tính khối lượng của Oxi tham cần dùng.
4. Cho sơ đồ phản ứng. Fe + O2 -> Fe3O4
a. Cân bằng phương trình phản ứng trên
b. Nếu có 6x10^23 phân tử O2 phản ứng thì có bao nhiêu phân tử Fe3O4 được tạo thành và bao nhiêu gam Fe tham gia phản ứng.
1. Na + 1/2O2 -> NaO
Al2O3 + 6HCl -> 2AlCl3 + 3H2O
AgNO3 + NaCl -> AgCl + NaNO3
CuSO4 + 2NaOH -> Na2SO4 + Cu(OH)2
Đúng 0
Bình luận (0)
Đốt cháy carbon C cần dùng 16 g khí oxygen O2, thu được 22 g khí carbonic CO2
a) Viết công thức về khối lượng của phản ứng xảy ra.
b) Tính khối lượng carbon đã phản ứng.
a) C+O2→CO2(đk nhiệt độ)
b)Áp dụng định luật bảo toàn khối lượng,có:
mC+mO2=mCO2
=>mC=22-16=6 g
Đúng 1
Bình luận (1)