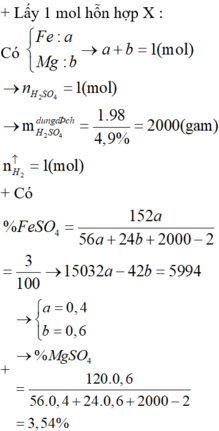tiính pH của dung dịch chứa 4,9 g H2SO4 trong 500ml

Những câu hỏi liên quan
Pha loãng 500ml dung dịch H2SO4 bằng 2,5 lít nước thu được dung dịch có pH3. Tính nồng độ mol ban đầu của dung dịch H2SO4? A. 3.10-3M B. 5.10-3 M C. 0,215M D. 0,235M
Đọc tiếp
Pha loãng 500ml dung dịch H2SO4 bằng 2,5 lít nước thu được dung dịch có pH=3. Tính nồng độ mol ban đầu của dung dịch H2SO4?
A. 3.10-3M
B. 5.10-3 M
C. 0,215M
D. 0,235M
Đáp án A
Gọi nồng độ ban đầu của H2SO4 là xM
nH+ = 0,5.x.2 = x mol
[H+] = x/3 = 10-3 suy ra x = 3.10-3M
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Mg và Fe hoà tan vừa hết trong dng dịch H2SO4 4,9% thì thu được dung dịch chứa 2 muối trong đó nồng độ % của FeSO4 3%.Nồng độ % của MgSO4 là : A. 3,25% B. 4,41% C. 3,54% D. 4.65%
Đọc tiếp
Hỗn hợp X gồm Mg và Fe hoà tan vừa hết trong dng dịch H2SO4 4,9% thì thu được dung dịch chứa 2 muối trong đó nồng độ % của FeSO4 = 3%.Nồng độ % của MgSO4 là :
A. 3,25%
B. 4,41%
C. 3,54%
D. 4.65%
Trộn 200 gam dung dịch NaOH 10% vào 500ml dung dịch chứa H2SO4 0,2M và MgSO4 0,4M thu được dung dịch X và m1 g kết tủa. Lọc kết tủa đem nung đến khối lượng không đổi thu được m2 g chất rắn. Tính m1, m2 và CM các chất trong X, biết kiềm sẽ phản ứng với axit hết rồi sau đó mới tác dụng với muối.
mNaOH = 200.10% = 20 gam ➝ nNaOH = 0,5 mol
nH2SO4 = 0,1 mol, nMgSO4 = 0,2 mol
Phản ứng:
(1) 2NaOH + H2SO4 ➝ Na2SO4 + 2H2O
0,2 0,1 0,1 (mol)
(2) 2NaOH + MgSO4 ➝ Mg(OH)2 + Na2SO4
0,3 0,15 0,15 0,15 (mol)
Dung dịch X: Na2SO4: 0,25 mol, MgSO4 dư: 0,05 mol
Kết tủa Mg(OH)2: 0,15 mol
Mg(OH)2 ➝ MgO + H2O
0,15 0,15
m1 = 0,15.58 = 8,7 gam
m2 = 0,15.40 = 6 gam
Đúng 1
Bình luận (0)
mọi người giúp e với ạ
Tính pH:
a) cho 500ml dung dịch H2SO4 0,01M + 300ml dung dịch HNO3 0,02
b) cho 500ml dung dịch Ca(OH)2 0,01M + 300ml dung dịch NaOH 0,02M
c) cho 500ml dung dịch Ca(OH)2 0,01M + 300ml dung dịch H2SO4 0,01M
Trộn 500ml dung dịch X gồm H2SO4 0.05M với 500ml dung dịch Ba(OH)2 aM. Thu được dung dịch Y có pH =12. Tính giá trị của a
Trộn m1 gam dung dịch NaOH 10% vào 500ml dung dịch chứa H2SO4 0,2M và MgSO4 0,3M thu được dung dịch X và m2 g kết tủa. Lọc kết tủa đem nung đến khối lượng không đổi thu được 4 g chất rắn. Tính m1, m2.
\(\left\{{}\begin{matrix}n_{H_2SO_4}=0,2.0,5=0,1\left(mol\right)\\n_{MgSO_4}=0,3.0,5=0,15\left(mol\right)\end{matrix}\right.\)
\(n_{MgO}=\dfrac{4}{40}=0,1\left(mol\right)\)
PTHH: 2NaOH + H2SO4 --> Na2SO4 + 2H2O
0,2<-----0,1
2NaOH + MgSO4 --> Mg(OH)2 + Na2SO4
0,2<------------------0,1
Mg(OH)2 --to--> MgO + H2O
0,1<------------0,1
=> nNaOH = 0,2 + 0,2 = 0,4 (mol)
=> mNaOH = 0,4.40 = 16 (g)
=> \(m_1=\dfrac{16.100}{10}=160\left(g\right)\)
m2 = 0,1.58 = 5,8 (g)
Đúng 2
Bình luận (0)
Trộn m1 gam dung dịch NaOH 10% vào 500ml dung dịch chứa H2SO4 0,2M và CuSO4 0,3M thu được dung dịch X và m2 g kết tủa. Lọc kết tủa đem nung đến khối lượng không đổi thu được 4 g chất rắn. Tính m1, m2
nH2SO4=0,2.0,5=0,1(mol)
nMgSO4=0,3.0,5=0,15(mol)
nMgO=\(\dfrac{4}{40}=0,1mol\)
PTHH: 2NaOH + H2SO4 --> Na2SO4 + 2H2O
0,2<-----0,1
2NaOH + MgSO4 --> Mg(OH)2 + Na2SO4
0,2<------------------0,1
Mg(OH)2 --to--> MgO + H2O
0,1<------------0,1
=> nNaOH = 0,2 + 0,2 = 0,4 (mol)
=> mNaOH = 0,4.40 = 16 (g)
=>
Đúng 1
Bình luận (0)
cho 3,2 g cuo tác dụng vừa đủ với dung dịch H2SO4 , 4,9%. Tính nồng độ phần trăm của dung dịch CuSO4
nCuO=0,04 mol
CuO + H2SO4 =>CuSO4 + H2O
0,04 mol=>0,04 mol=>0,04 mol
mH2SO4=0,04.98=3,92 gam
=>m dd H2SO4=3,92/4,9%=80 gam
mCuSO4 sau=0,04.160=6,4 gam
mdd CuSO4=3,2+80=83,2 gam
C% dd CuSO4=6,4/83,2.100%=7,69%
Đúng 0
Bình luận (0)
cho \(m_{CuO}=3,2g\Rightarrow n_{CuO}=\frac{3,2}{80}=0,04mol\)
PTHH:
CuO + H2SO4 -> CuSO4 + H2O
0,04mol----------->0,04mol--------->0,04mol
ta có: \(m_{H_2SO_4}=0,04.98=3,92g\)
\(C\%_{d^2H_2SO_{4_{ }}}=4,9\%\)
=. \(m_{d^2H_2SO_4}=\frac{m_{H_2SO_4}.100}{C\%}=\frac{3,92.100}{4,9}=80g\)
áp dụng ĐLBTKL ta có: \(m_{d^2CUSO_4}=m_{CuO}+m_{d^2H_2SO_4}=3,2+80=83,2g\)
\(m_{CuSO_4}=0,04.160=6,4g\)
\(\Rightarrow C\%_{d^2CuSO_4}=\frac{m_{CuSO_4}}{m_{d^2CuSO_4}}.100=\frac{6,4}{83,2}.100=7,69\%\)
Đúng 0
Bình luận (0)
Trộn 200ml dung dịch hỗn hợp HCl 0,1M và H2SO4 0,05M với 300ml dung dịch Ba(OH)2 a M thu được m (g) kết tủa và 500ml dung dịch ph=13. Tìm a , m .
a=0,12
m=2,33g