tìm pH, xđ môi trường, màu của pp và quì tím
Ba(OH)2 0,005M
tìm pH, xđ môi trường, màu của pp và quì tím
HNO3 0,004M
`HNO_3 -> H^{+} + NO_3^{-}`
`0,004 -> 0,004`
`-> pH = -log(0,004) ~~ 2,4 < 7`
Môi trường axit
Màu phenolphtalein là không màu và quỳ tím hóa đỏ
Tính pH và xác định môi trường của dung dịch H2SO4 0,005M
Ta có: \(\left[H^+\right]=0,005.2=0,01\left(M\right)\)
\(\Rightarrow pH=-log\left[H^+\right]=2\)
→ Môi trường của dd: axit.
Tính pH của dung dịch sau:
a, 1 lít dung dịch hỗn hợp NaOH 0,005M; KOH 0,005M và Ba(OH)2 0,005M
NaOH và KOH: \(pOH=2,3\Rightarrow pH=11,7\)
\(Ba\left(OH\right)_2:\) \(\left[OH^-\right]=0,005\cdot2=0,01M\)
\(pOH=2\Rightarrow pH=12\)
*Tính [H+], [OH-], pH và cho biết môi trường, màu của quỳ tím của các dd sau khi pha trộn:
a/ Trộn lẫn 400ml dd NaOH 0,5M với 200ml dd NaOH 0,2M
b/ Trộn lẫn 100 ml dd NaOH 0,01 M với 400 ml dd Ba(OH)2 0,005M
Xin cảm ơn nhiều ạ![]()
Tính [H+], [OH-], pH và cho biết môi trường, màu của quỳ tím của các dd sau khi pha trộn:
a/ Trộn lẫn 400ml dd NaOH 0,5M với 200ml dd NaOH 0,2M
b/ Trộn lẫn 100 ml dd NaOH 0,01 M với 400 ml dd Ba(OH)2 0,005M
Xin cảm ơn nhiều ạ![]()
Tính [H+], [OH-], pH và cho biết môi trường, màu của quỳ tím của dd sau khi pha trộn:
50 ml dd H2SO4 0,4M với 350 ml dd HCl 0,2M
Xin cảm ơn nhiều ạ![]()
Ta có: \(n_{H^+}=2n_{H_2SO_4}+n_{HCl}=2\cdot0,02+0,07=0,11\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\dfrac{0,11}{0,35+0,05}=0,275\left(M\right)\) \(\Rightarrow\left[OH^-\right]=\dfrac{10^{-14}}{\left[H^+\right]}\approx3,64\cdot10^{-14}\left(M\right)\)
\(\Rightarrow pH=-log\left(0,275\right)\approx0,56\)
*Môi trường axit và làm quỳ tím hóa đỏ
\(n_{H_2SO_4}=0,05.0,4=0,02\left(mol\right)\\ n_{HCl}=0,2.0,35=0,07\left(mol\right)\\ \left[H^+\right]=\dfrac{0,02.2+0,07}{0,05+0,35}=0,275\left(M\right)\\ pH=-log\left[H^+\right]=-log\left[0,275\right]=0,56\\ \Rightarrow Qùy.hóa.đỏ\)
Một dung dịch có [H+] = 0,010 M. Tính [OH-] và pH của dung dịch. Môi trường của dung dịch này là axit, trung tính hay kiềm? Hãy cho biết màu của quỳ trong dung dịch này?
[H+] = 0,010M = 10-2M ⇒ pH = -log[H+] = -log(1,0.10-2) = 2
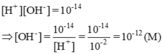
Môi trường của dung dịch này là axit (pH < 7)
Cho quỳ tím vào dung dịch này quỳ sẽ chuyển thành màu đỏ
Dung dịch Ba(OH)2 0,005M có pH bằng
A. 3.
B. 2.
C. 11.
D. 12
Chọn đáp án D
CM Ba(OH)2 = 0,005M ⇒ CM OH– = 0,005 × 2 = 0,01M
⇒ pOH = 2 ⇒ pH = 14 – 2 = 12 ⇒ Chọn D
Dung dịch Ba(OH)2 0,005M có pH bằng
A. 3.
B. 2.
C. 11.
D. 12
Chọn đáp án D
CM Ba(OH)2 = 0,005M ⇒ CM OH– = 0,005 × 2 = 0,01M
⇒ pOH = 2 ⇒ pH = 14 – 2 = 12