Hãy giải thích vì sao ở giai đoạn tạo ra SO3 người ta chọn điều kiện phản ứng ở nhiệt độ cao (450 °C - 500 °C).

Những câu hỏi liên quan
Người ta đốt 32 gam khí SO2 với 10 gam khí oxi( ở nhiệt độ 450°C có xúc tác là V2O5) sau phản ứng thu được SO3.Giả sử phản ứng xảy ra hoàn toàn.
a) Viết PTHH.Chất nào dư? dư bao nhiêu gam
b) Tính khối lượng SO3?
Giúp mình với ạ mình đang cần gấp
Cảm ơn
Xem chi tiết
a) \(PTHH:2SO_2+O_2\xrightarrow[V_2O_5]{450^oC}2SO_3\)
\(n_{SO_2}=\dfrac{32}{64}=0,5\left(mol\right)\\ n_{O_2}=\dfrac{10}{32}=0,3125\left(mol\right)\)
Lập tỉ lệ: \(\dfrac{n_{SO_2}}{2}< \dfrac{n_{O_2}}{1}\left(\dfrac{0,5}{2}< 0,3125\right)\)
=> SO2 hết O2 dư
Theo pt: \(n_{O_2\left(pư\right)}=\dfrac{n_{SO_2}.2}{3}=\dfrac{0,5.1}{2}=0,25\left(mol\right)\)
\(n_{O_2\left(dư\right)}=0,3125-0,25=0,0625\left(mol\right)\\ m_{O_2}=0,0625.32=2\left(g\right)\)
c) Theo pt, ta có:\(n_{SO_3}=n_{SO_2}=0,5\left(mol\right)\)
\(m_{SO_3}=0,5.80=40\left(g\right)\)
Đúng 2
Bình luận (0)
Một trong những ứng dụng của axetilen là làm nhiên liệu trong đnè xì để hàn và cắt kim loại. Hãy giải thích vì sao người ta ko dùng etan(C2H6) thay cho axetilen, mặ dù nhiệt đốt cháy ở cùng điều kiện của etan (1562kJ/mol) cao hơn của axetilen (1302kJ/mol)
PTHH: \(C_2H_2+\dfrac{5}{2}O_2\xrightarrow[]{t^o}2CO_2+H_2O\)
\(C_2H_6+\dfrac{7}{2}O_2\xrightarrow[]{t^o}2CO_2+3H_2O\)
Ta thấy khi đốt axetilen, lượng nước giải phóng ra ít hơn so với đốt etan. Vì vậy lượng nước thoát ra làm nguội cũng ít hơn. Do đó đốt axetilen nhiệt độ cao hơn
Đúng 2
Bình luận (0)
PTHH :
`C_2H_2 + 5/2O_2` `->^{t^o} CO_2 + H_2O`
`C_2H_6 + 7/2O_2 ->^{t^o} CO_2 + 3H_2O`
Dựa vào PTHH ta thấy được lượng nước giải phóng của etan nhiều hơn của axetilen. Nên khi đốt axetilen có nhiệt độ cao hơn giúp cắt kim loại và làm đèn xì tốt hơn.
Đúng 0
Bình luận (2)
Nung 6,06g kali nitrat ở nhiệt độ cao để phản ứng xảy ra hoàn toàn, cân lại chất rắn sau phản ứng thì thấy khối lượng chất rắn thu được là 5,1g.
PT pư chữ: Kali nitrat(rắn) --> Kali nitrat(rắn) + oxi (khí)
Em hãy giải thích vì sao khối lượng chất rắn giảm. Tính thể tích khí Oxi sinh ra (điều kiện thường) biết ở điều kiện thuwongfm 1 mol chất khí chiếm thể tích 24 lít.
Khối lượng rắn sau khi nung giảm do có khí O2 thoát ra
Theo ĐLBTKL: \(m_{KNO_3}=m_{KNO_2}+m_{O_2}\)
=> \(m_{O_2}=6,06-5,1=0,96\left(mol\right)\)
=> \(n_{O_2}=\dfrac{0,96}{32}=0,03\left(mol\right)\)
=> VO2 = 0,03.24 = 0,72 (l)
Đúng 6
Bình luận (0)
\(n_{KNO_3}=\dfrac{6,06}{101}=0,06mol\)
\(n_{KNO_2}=\dfrac{5,1}{85}=0,06mol\)
\(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\)
0,06 0,06 0,03
Ở điều kiện thường, cứ 1 mol chất khí chiếm 24l về thể tích.
\(\Rightarrow\)0,03mol chất khí \(O_2\) có thể tích là:
\(V_{O_2}=0,03\cdot24=0,72l=720ml\)
Đúng 4
Bình luận (0)
Hãy chọn câu trả lời sai?Những điều kiện cần phải có để tạo nên phản ứng hạt nhân dây chuyền là gì ?A. Sau mỗi lần phân hạch, số n giải phóng phải lớn hơn hoặc bằng 1.B. Lượng nhiên liệu (urani, plutôni) phải đủ lớn để tạơ nên phán ứng dây chuyền.C. Phải có nguồn tạo ra nơtron.D. Nhiệt độ phải được đưa lên cao.
Đọc tiếp
Hãy chọn câu trả lời sai?
Những điều kiện cần phải có để tạo nên phản ứng hạt nhân dây chuyền là gì ?
A. Sau mỗi lần phân hạch, số n giải phóng phải lớn hơn hoặc bằng 1.
B. Lượng nhiên liệu (urani, plutôni) phải đủ lớn để tạơ nên phán ứng dây chuyền.
C. Phải có nguồn tạo ra nơtron.
D. Nhiệt độ phải được đưa lên cao.
Trong phòng thí nghiệm khi đốt cháy sắt trong oxi ở nhiệt độ cao được oxit sắt từ
F
e
3
O
4
Số gam kali pemanganat
K
M
n
O
4
cần dùng để điều chế lượng khí oxi cần dùng cho phản ứng trên là: A.3,16g B. 9,48g C.5,24g D.6,32g Hãy giải thích sự lựa chọn.
Đọc tiếp
Trong phòng thí nghiệm khi đốt cháy sắt trong oxi ở nhiệt độ cao được oxit sắt từ F e 3 O 4
Số gam kali pemanganat K M n O 4 cần dùng để điều chế lượng khí oxi cần dùng cho phản ứng trên là:
A.3,16g B. 9,48g C.5,24g D.6,32g
Hãy giải thích sự lựa chọn.
Theo câu a: số mol của O 2 : n O 2 = 0,02mol
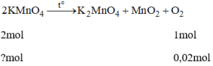
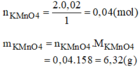
Đúng 0
Bình luận (0)
Để tạo ra phản ứng hạt nhân có điều khiển cần phải
A. dùng những thanh điều khiển có chứa Bo hay Cd.
B. chế tạo các lò phản ứng chứa nước áp suất cao (có vai trộ làm chậm nơtron).
C. tạo nên một chu trình trong lò phản ứng.
D. tạo ra nhiệt độ cao trong lò (500 ° C).
Để sản xuất axit sunfuric, người ta dung nhiên liệu là quặng pirit sắt
(
F
e
S
2
)
đem nghiền nhỏ rồi nung ở nhiệt độ cao thu được sắt III oxit
(
F
e
2
O
3
)
và khí sunfuro
(
S
O
2
)
.
Oxi hóa có
V
2
O
5
làm xúc tác ở nhiệt độ...
Đọc tiếp
Để sản xuất axit sunfuric, người ta dung nhiên liệu là quặng pirit sắt ( F e S 2 ) đem nghiền nhỏ rồi nung ở nhiệt độ cao thu được sắt III oxit ( F e 2 O 3 ) và khí sunfuro ( S O 2 ) . Oxi hóa có V 2 O 5 làm xúc tác ở nhiệt độ 450 ° C thu được S O 3 , cho S O 3 hợp với nước thu được axit sunfuric ( H 2 S O 4 ) . Hãy xác định đâu là hiện tượng vật lý, đâu là hiện tượng hóa học?
- Hiện tượng vật lý: nghiền nhỏ quặng pirit sắt ( F e S 2 )
- Hiện tượng hóa học:
+Quặng pirit sắt cháy tạo thành F e 2 O 3 và S O 2
+Oxi hóa S O 2 thành S O 3
+Hợp chất nước và S O 3 tạo thành axit sunfuric ( H 2 S O 4 )
Đúng 0
Bình luận (0)
Viết PTHH của các phản ứng xảy ra khi cho clo và iot lần lượt tác dụng với dung dịch KOH ở nhiệt độ thường. Giải thích vì sao có sự khác nhau ở 2 phản ứng đó:
Cl 2 + 2KOH → KCl + KClO + H 2 O
3 I 2 + 6KOH → 5KI + KI O 3 + 3 H 2 O
Trong môi trường kiềm, ion XO - phân huỷ theo phản ứng sau :
3 XO - → 2 X - + XO 3 - (kí hiệu X là halogen)
Ion ClO - phân huỷ rất chậm ở nhiệt độ thường, phân huỷ nhanh ở nhiệt độ trên 75 ° C
Ion IO - phân huỷ ở tất cả các nhiệt độ trên, do đó ở nhiệt độ thường, ta có 2 phản ứng trên.
Đúng 0
Bình luận (0)
khi NH3 có thể được tổng hợp bằng cách nung nóng. Hỗn hợp gồm khí N2 và H2 ở nhiệt độ 450- 500 độ C , áp suất 200-300 atm và dùng chất xúc tác bột Fe.
a) viết các PTHH
b) cho 4lít N2 và 14lít H2 vào bình phản ứng. Hỗn hợp sau phản ứng có V 16,4l .tính thể tích NH3 tạo thành và hiệu suất phản ứng.
biết thể tích các khí đo ở cùng điều kiện về nhiệt độ và áp suất
Đọc tiếp
khi NH3 có thể được tổng hợp bằng cách nung nóng. Hỗn hợp gồm khí N2 và H2 ở nhiệt độ 450- 500 độ C , áp suất 200-300 atm và dùng chất xúc tác bột Fe.
a) viết các PTHH
b) cho 4lít N2 và 14lít H2 vào bình phản ứng. Hỗn hợp sau phản ứng có V= 16,4l .tính thể tích NH3 tạo thành và hiệu suất phản ứng.
biết thể tích các khí đo ở cùng điều kiện về nhiệt độ và áp suất



















