Trong phòng thí nghiệm người ta điều chế oxi bằng nung nóng KMnO4.Tính khối lượng KMnO4cần dùng để thu được 3,36lít O2.Cho biết Ca=40,Cu=64,Fe=56,Mg=24,O=16,K=39,Mn=55

Những câu hỏi liên quan
Trong phòng thí nghiệm người ta điều chế được oxit săt từ(Fe3O4) bằng cách dùng oxi hóa sắt ở nhiệt độ cao.
Tính thể tích khí oxi cần dùng (ở đktc) để điều chế được 6,96g oxit sắt từ.
( Cho biết : C = 12; O=16 ; H=1; Fe= 56; K=39; Mn =55 , Cl = 35,5 )
ai giup minh voi a
3Fe+2O2-to>Fe3O4
0,06----------------0,03
n Fe3O4 =\(\dfrac{6,96}{232}\)=0,03 mol
=>VO2=0,06.22,4=1,344l
Đúng 2
Bình luận (0)
\(n_{Fe_3O_4}=\dfrac{6.96}{232}=0,03\left(mol\right)\)
PTHH : 3Fe + 2O2 -> Fe3O4
0,06 0,03
\(V_{O_2}=0,06.22,4=1,344\left(l\right)\)
Đúng 0
Bình luận (4)
Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi hóa sắt ở nhiệt độ cao. a) Tính số gam sắt và oxi cần dùng để điều chế được 2,32g oxi sắt từ? b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên, biết rằng khi nung nóng 2 mol KMnO4 thì thu được 1 mol O2.
Đọc tiếp
Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi hóa sắt ở nhiệt độ cao.
a) Tính số gam sắt và oxi cần dùng để điều chế được 2,32g oxi sắt từ?
b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên, biết rằng khi nung nóng 2 mol KMnO4 thì thu được 1 mol O2.
a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 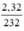 = 0,01 mol.
= 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
Đúng 0
Bình luận (0)
Trong vòng thí nghiệm, người ta điều chế khí oxi bằng cách nung Kali pemanganat (KMnO4) ở nhiệt độ cao, theo sơ đồ sau: KMnO4-----to--- K2MnO4 + MnO2 + O2
a/ tính khối lượng của KMnO4 cần dùng để điều chế được 4,48 lít khí oxi ở đktc( biết phản ứng xảy ra hoàn toàn)
b/ nếu cho bộ lượng thu đc ở trên vào bình chứa 16 gam bột sắt (lll) oxit (Fe2O3) và đun nóng,sau phản ứng chất nào còn dư và dư bao nhiêu gam?
(Biết Cu64,O16,K39,Mn55,S32,Al27,Cr52,Fe56
Đọc tiếp
Trong vòng thí nghiệm, người ta điều chế khí oxi bằng cách nung Kali pemanganat (KMnO4) ở nhiệt độ cao, theo sơ đồ sau: KMnO4-----to---> K2MnO4 + MnO2 + O2
a/ tính khối lượng của KMnO4 cần dùng để điều chế được 4,48 lít khí oxi ở đktc( biết phản ứng xảy ra hoàn toàn)
b/ nếu cho bộ lượng thu đc ở trên vào bình chứa 16 gam bột sắt (lll) oxit (Fe2O3) và đun nóng,sau phản ứng chất nào còn dư và dư bao nhiêu gam?
(Biết Cu=64,O=16,K=39,Mn=55,S=32,Al=27,Cr=52,Fe=56
2KMnO4-----to---> K2MnO4 + MnO2 + O2
0,4<-----------------------------------------------0,2
mKMnO4=158.0,4=63,2(g)
b,chịu
Đúng 0
Bình luận (0)
Câu 11: (2,0 điểm) Đế oxi hóa 6,75 gam nhôm người ta dùng 3,36 lít khí oxi (đktc).
a. Tính khối lượng chất dư.
b. Tính khối lượng KMNO4 cần dùng để điều chế lượng oxi dùng trong phản ứng trên.
(Biết NTK: CI = 35,5; K = 39; Cu = 64; 0= 16, Al-27; Mn= 55)
\(n_{Al}=\dfrac{6,75}{27}=0,25mol\)
\(n_{O_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
0,25 0,15 0
0,2 0,15 0,1
0,05 0 0,1
\(m_{dư}=m_{Aldư}=0,05\cdot27=1,35g\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,3 0,15
\(m_{KMnO_4}=0,3\cdot158=47,4g\)
Đúng 3
Bình luận (0)
Để điều chế oxi trong phòng thí nghiệm người ta nung nóng kali clorat
a) Viết phương trình hoá học
b) Tính khối lượng kali clorua và thể tích khí oxi thu được ( ở đktc) khi nung nóng 12,25g KCLO3. Biết hiệu suất là 85%
c) Tính kali clorat cần dùng để thu được 4,032 lít khí oxi ( ở đktc) khi nung nóng. Biết hiệu suất phản ứng là 80%.
Bài 2: Trong phòng thí nghiệm, người ta điều chế oxit sắt từ bằng cách dùng oxi để oxi hoá sắt ở nhiệt độ cao.a. Tính thể tích khí oxi cần dùng để điều chế được 4,64 g oxit sắt từ ?b. Tính khối lượng KMnO4 cần dùng để điều chế được lượng oxi cho phản ứng trên (giả sử không có sự hao hụt trong quá trình điều chế)?
Xem chi tiết
a, Ta có: \(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02\left(mol\right)\)
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
THeo PT: \(n_{O_2}=2n_{Fe_3O_4}=0,04\left(mol\right)\Rightarrow V_{O_2}=0,04.22,4=0,896\left(l\right)\)
b, PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
\(n_{KMnO_4}=2n_{O_2}=0,08\left(mol\right)\Rightarrow m_{KMnO_4}=0,08.158=12,64\left(g\right)\)
Đúng 1
Bình luận (0)
a) \(n_{Fe_3O_4}=\dfrac{m_{Fe_3O_4}}{M_{Fe_3O_4}}=\dfrac{4,64}{232}=0,02\left(mol\right)\).
PTHH : \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Mol : 3 : 2 : 1
Mol 0,04 ← 0,02
\(\Rightarrow V_{O_2}=n_{O_2}.22,4=\left(0,04\right).\left(22,4\right)=0,896\left(l\right)\).
b) Từ phương trình ở câu a \(\Rightarrow n_{O_2}=0,04\left(mol\right)\).
PTHH : \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Mol : 2 : 1 : 1 : 1
Mol : 0,08 ← 0,04
\(\Rightarrow m_{KMnO_4}=n_{KMnO_4}.M_{KMnO_4}=\left(0,08\right).158=12,64\left(g\right)\).
Đúng 0
Bình luận (0)
Trong phòng thí nghiệm, người ta thường dùng KMnO4, KClO3 để điều chế oxi.
1. Nêu và giải thích phương pháp thu khí oxi vào lọ?
2. Khi nung nóng lần lượt a gam KMnO4 và b gam KClO3 sau phản ứng hoàn toàn thu được cùng một lượng khí oxi. Hãy tính tỉ lệ a/b?
-thu oxi có 2 loại
-Đẩy kk ; là ta lật ngửa bình để thu=>O2 nặng hơn kk
-Đẩy nước : ta có thể dời nước =>O2 ko tan trong nước , ko td vs nước
2
cùng 1 lượng oxi
2KMNO4-to>K2MnO4+MnO2+O2
2KClO3-to>2KClO3+3O2
=>\(\dfrac{a}{b}=\dfrac{2.158}{2\backslash3.122,5}=3.869\)
Đúng 2
Bình luận (0)
thu khí O2 bằng 2pp :
đẩy nước vì O2 ít tan trong nước
đẩy KK bằng cách đặt ngửa bình vì O2 nhẹ hơn KK
gọi nO2 là x
\(pthh:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
2x x
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(\dfrac{2}{3}x\) x
=> \(\left\{{}\begin{matrix}m_{KMnO_4}=2x.158=316x\\m_{KClO_3}=\dfrac{2}{3}x.122,5=81,6x\end{matrix}\right.\)
=> \(\dfrac{a}{b}=\dfrac{316x}{81,6x}=\dfrac{395}{102}\)
Đúng 1
Bình luận (0)
trong phòng thí nghiệm người ta thường dùng KMnO4 KClO3 để điều chế khí Oxi
a, Nêu và giải thích phương pháp thu khí oxi vào lọ ?
b,khi nung nóng lần lượt a gam KMnO4 và b gam KClO3 sau phản ứng hoàn toàn thu được cùng một lượng khí oxy. Hãy tính tỉ lệ a/b?
a. Phương pháp: đẩy nước vì oxi ít tan trong nước, đẩy không khí vì oxi nặng hơn không khí
b.Giả sử có 1 mol O2
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
2 1 ( mol )
\(m_{KMnO_4}=2.158=316g\)
\(2KClO_3\rightarrow\left(t^o,MnO_2\right)2KCl+3O_2\)
2/3 1 ( mol )
\(m_{KClO_3}=\dfrac{2}{3}.122,5=\dfrac{245}{3}g\)
\(\dfrac{a}{b}=\dfrac{m_{KMnO_4}}{m_{KClO_3}}=316:\dfrac{245}{3}=\dfrac{948}{245}\)
Đúng 3
Bình luận (0)
a ) pp đẩy kk và đẩy nước
nKMnO4 = a / 158 (MOL)
nKClO3 = b / 122,5 (MOL)
b) gọi số mol O2 là x
pthh : 2KMnO4 -t--> K2MnO4 + MnO2 + O2
2x ---------------------------------> x (mol)
2KClO3 -t--> 2KCl+ 3O2
2/3x -----------> x(mol)
=> mKMnO4 = 2x . 158 = 316 x (g)
=> mKClO3 = 2/3 x . 122,5 = 81,67 x (g)
=> a/b = 316x/81,67x = 316 / 81,67
Đúng 1
Bình luận (0)
cho 3,24 g Al tác dụng với Oxi vừa đủ thu được Al2O3 a. tính Vo2 ( đktc) b. tính mAl2O3 c.tính Vkk cần dùng ( biết Vo=21% kk) d tính khối lượng KMnO4 cần dùng để điều chế chất lượng oxi ở câu a. ? (Al=27 ,O=16, K=39,Mn=55)
Bạn xem lời giải ở đây nhé.
https://hoc24.vn/cau-hoi/cho-324-g-al-tac-dung-voi-oxi-vua-du-th-duoc-al2o3-a-tinh-vo2-b-tinh-m-al2o3-c-trong-vkk-can-dung-biet-vo2-21-vkk-d-tinh-khoi-luong-kmno.7651142171785
Đúng 0
Bình luận (0)
























