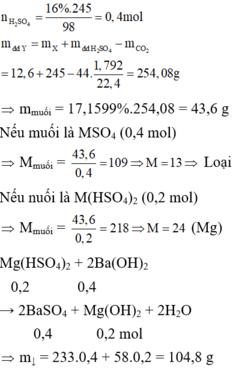Cho m (gam) CaS tác dụng vừa đủ với M1 (gam) dung dịch HBr 9,72%. Thu được dung dịch M2 (gam) nồng độ x% và 672ml khí H2S (đktc). Tìm M; M1; M2; x.

Những câu hỏi liên quan
Cho m gam CaS tác dụng đủ với m1 gam dung dịch axit HBr 9,72% thu được m2 gam dung dịch muối x% và 672ml khí H2S (đktc). Tính m, m1, m2, x.
Giúp toi với:))((
vừa đủ thì dễ rồi
PTHH : \(CaS+2HBr-->CaBr_2+H_2S\uparrow\)
\(n_{H_2S}=\frac{0,672}{22,4}=0,03\left(mol\right)\)
Theo pthh : \(n_{CaS}=n_{H_2S}=0,03\left(mol\right)\)
\(n_{HBr}=2n_{H_2S}=0,06\left(mol\right)\)
\(n_{CaBr_2}=n_{H_2S}=0,03\left(mol\right)\)
\(\Rightarrow\hept{\begin{cases}m_{CaS}=0,03\cdot72=2,16\left(g\right)=m\\m_{ddHBr}=\frac{0,06\cdot81}{9,72}\cdot100=50\left(g\right)=m_1\end{cases}}\)
Theo ĐLBTKL :
\(m_{CaS}+m_{ddHBr}=m_{ddCaBr_2}+m_{H_2S}\)
=> \(2,16+50=m_{ddCaBr_2}+0,03\cdot34\)
=> \(m_{ddCaBr_2}=51,14\left(g\right)=m_2\)
=> \(C\%_{ddCaBr_2}=\frac{0,03\cdot200}{51,14}\cdot100\%\approx11,73\%\)
=> \(x\approx11,73\)
dễ nhưng vẫn nên check lại ...
cho m1 gam Fe tác dụng vừa đủ với m2 gam dung dịch HCl 7,3% .Sau phản ứng thu được 5,6 lít khí H2 ở đktc. Xác định m1 và m2
Ta có: \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{Fe}=n_{H_2}=0,25\left(mol\right)\Rightarrow m_{Fe}=0,25.56=14\left(g\right)=m_1\)
\(n_{HCl}=2n_{H_2}=0,5\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,5.36,5=18,25\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{18,25}{7,3\%}=250\left(g\right)=m_2\)
Đúng 2
Bình luận (0)
Hỗn hợp X gồm Fe3O4 và Cu (tỉ lệ mol là 1:2). Cho m gam X tác dụng vừa đủ với dung dịch chứa 0,08 mol HCl, kết thúc phản ứng thu được dung dịch Y và còn lại m1 gam chất rắn Z. Cho dung dịch Y tác dụng với dung dịch AgNO3 dư thu được m2 gam kết tủa. Giá trị của m1, m2 lần lượt là A. 0,64 và 11,48 gam B. 0,64 và 3,24 gam. C. 0,64 và 14,72 gam D. 0,32 và 14,72 gam.
Đọc tiếp
Hỗn hợp X gồm Fe3O4 và Cu (tỉ lệ mol là 1:2). Cho m gam X tác dụng vừa đủ với dung dịch chứa 0,08 mol HCl, kết thúc phản ứng thu được dung dịch Y và còn lại m1 gam chất rắn Z. Cho dung dịch Y tác dụng với dung dịch AgNO3 dư thu được m2 gam kết tủa. Giá trị của m1, m2 lần lượt là
A. 0,64 và 11,48 gam
B. 0,64 và 3,24 gam.
C. 0,64 và 14,72 gam
D. 0,32 và 14,72 gam.
Hỗn hợp X gồm
F
e
3
O
4
và Cu (tỉ lệ mol là 1: 2). Cho m gam X tác dụng vừa đủ với dung dịch chứa 0,08 mol HCl, kết thúc phản ứng thu được dung dịch Y và còn lại m1 gam chất rắn Z. Cho dung dịch Y tác dụng với dung dịch
A
g
N
O
3...
Đọc tiếp
Hỗn hợp X gồm F e 3 O 4 và Cu (tỉ lệ mol là 1: 2). Cho m gam X tác dụng vừa đủ với dung dịch chứa 0,08 mol HCl, kết thúc phản ứng thu được dung dịch Y và còn lại m1 gam chất rắn Z. Cho dung dịch Y tác dụng với dung dịch A g N O 3 (dư) thu được m2 gam kết tủa. Giá trị của m1, m2 lần lượt là
A. 0,64 và 14,72
B. 0,64 và 3,24
C. 0,32 và 14,72
D. 0,64 và 11,48
Đáp án A
Kết thúc phản ứng còn dư lại m1 (g) chất rắn Z
=> Z là Cu, dd Y gồm FeCl2 và CuCl2.
Fe3O4 + 8HCl → 2FeCl3 + FeCl2
0,01<---- 0,08 ------> 0,01
=> n C u = 0,02
2FeCl3 + Cu → 2FeCl2 + CuCl2
0,02 -----> 0,01 --> 0,02
=> n C u dư = 0,01 => m1 = 6,4g
dd Y tác dụng với A g N O 3
Ag+ + Cl- → AgCl
0,08 <--- 0,08 ----> 0,08
Fe2+ + Ag+ → Fe3+ + Ag
0,03 → 0,03
=> m2 = 0,03.108 + 0,08.143,5 = 14,72g
Đúng 0
Bình luận (0)
Cho m gam CaS tác dụng vừa đủ với m1 gam dd HBr 9,72% thu được m2 gam dd muối X% và 672 ml khí H2S(đktc). Tính m, m1,m2, X
Hoà tan m1 gam bột Zn cần dùng vừa đủ m2 gam dung dịch HCl 14.6%. Phản ứng kết thúc, thu được 0.896 lít khí (ở đktc).
a. Tính m1 và m2
b. Tính nồng độ phần trăm của dung dịch thu được sau phản ứng.
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,04\left(mol\right)\Rightarrow m_1=m_{Zn}=0,04.65=2,6\left(g\right)\)
\(n_{HCl}=2n_{H_2}=0,08\left(mol\right)\Rightarrow m_{HCl}=0,08.36,5=2,92\left(g\right)\)
\(\Rightarrow m_2=m_{ddHCl}=\dfrac{2,92}{14,6\%}=20\left(g\right)\)
b, Ta có: m dd sau pư = mZn + m dd HCl - mH2 = 22,52 (g)
\(n_{ZnCl_2}=n_{H_2}=0,04\left(mol\right)\)
\(\Rightarrow C\%_{ZnCl_2}=\dfrac{0,04.136}{22,52}.100\%\approx24,16\%\)
Đúng 1
Bình luận (0)
Cho m gam hỗn hợp kim loại có hóa trị không đổi thành hai phần bằng nhau. Phần I cho tác dụng hoàn toàn với dung dịch H2SO4 vừa đủ thu đượ 4,48l khí H2 (đktc) và m1 gam muối sunfat khan. Phần II cho tác dụng hoàn toàn với oxi thu được m2 gam oxit. Giá trị m1 - m2 có giá trị là
PTHH:
\(M+H_2SO_4\rightarrow M_2\left(SO_4\right)_x+H_2\left(1\right)\)
\(M+O_2\rightarrow M_2O_x\left(2\right)\)
Phần 1:
\(n_{SO_4}=n_{H_2SO_4}=n_{H_2}=0,2\left(mol\right)\)
Ta có: \(m_{M_2\left(SO_4\right)_x}=m_M+m_{SO_4}\Leftrightarrow m_1=\dfrac{m}{2}+0,2.96=\dfrac{m}{2}+19,2\left(3\right)\)
Phần 2:
Ta có: \(m_O=m_{M_2O_x}-m_M=m_2-\dfrac{m}{2}\Rightarrow n_O=\dfrac{m_2}{16}-\dfrac{m}{32}\left(mol\right)\)
Lại có: \(n_{SO_4\left(1\right)}=x.n_{M_2\left(SO_4\right)_n}=\dfrac{x}{2}.n_M=x.n_{M_2O_x}=n_{O\left(2\right)}\)
\(\Leftrightarrow0,2=\dfrac{m_2}{16}-\dfrac{m}{32}\)
\(\Leftrightarrow3,2=m_2-\dfrac{m}{2}\)
\(\Leftrightarrow m_2=\dfrac{m}{2}+3,2\left(4\right)\)
Từ \(\left(3\right)\) và \(\left(4\right)\Rightarrow m_1-m_2=16\)
Đúng 1
Bình luận (0)
Cho m gam hỗn hợp Al,
A
l
2
O
3
,
A
l
O
H
3
tác dụng với dung dịch
H
2
S
O
4
19,6% vừa đủ, thu được dung dịch X có nồng độ là 21,302% và 3,36 lít
H
2...
Đọc tiếp
Cho m gam hỗn hợp Al, A l 2 O 3 , A l O H 3 tác dụng với dung dịch H 2 S O 4 19,6% vừa đủ, thu được dung dịch X có nồng độ là 21,302% và 3,36 lít H 2 (đktc). Cô cạn dung dịch X thu được 80,37 gam muối khan m có giá trị là
A. 28,98.
B. 18,78.
C. 25,09
D. 24,18.
Cho 12,6 gam hỗn hợp X gồm MO, M(OH)2 và MCO3 tác dụng vừa đủ với 245 gam dung dịch H2SO4 16% sau khi X tan hết thu được 1,792 lít khí (đktc) và dung dịch Y chỉ chứa một muối duy nhất có nồng độ là 17,1599%. Cho 500ml dung dịch Ba(OH)2 1M vào Y, thu được m gam kết tủa. Giá trị gần nhất với m là A. 120 B. 105 C. 110 D. 125
Đọc tiếp
Cho 12,6 gam hỗn hợp X gồm MO, M(OH)2 và MCO3 tác dụng vừa đủ với 245 gam dung dịch H2SO4 16% sau khi X tan hết thu được 1,792 lít khí (đktc) và dung dịch Y chỉ chứa một muối duy nhất có nồng độ là 17,1599%. Cho 500ml dung dịch Ba(OH)2 1M vào Y, thu được m gam kết tủa. Giá trị gần nhất với m là
A. 120
B. 105
C. 110
D. 125