cho 7,8 gam kim loại a(có hóa trị 1) tác dụng hoàn toàn với nc sau phản ứng thu đc 2,24l khí hidro(ở đktc) xác định tên và kí hiệu hóa học của kim loại trên

Những câu hỏi liên quan
Cho 7,8 gam kim loại X có hóa trị III tác dụng vừa đủ với dung dịch NaOH sau phản ứng thấy thoát ra 5,04 lít H2 (đktc). Hãy cho xác định tên và kí hiệu hóa học của X.
\(n_{H_2}=\dfrac{5,04}{22,4}=0,225\left(mol\right)\)
\(2X+2NaOH+2H_2O->2NaXO_2+3H_2\)
0,15<---------------------------------------0,225
=> \(M_X=\dfrac{7,8}{0,15}=52\left(g/mol\right)\)
=> X là Cr(Crom)
Đúng 3
Bình luận (0)
Cho 7,2 gam kim loại X có hóa trị II tác dụng vừa đủ với dung dịch H2SO4 loãng. Cô cạn dung dịch sau phản ứng thu được 36 gam muối. Hãy cho biết tên và kí hiệu hóa học của X.
Đúng 0
Bình luận (0)
Clus. Cho 13,5 gam kim loại M hóa trị x tác dụng 6,72 lít O_{2} ở đktc phản ứng hoàn toàn thu được m gam chất rắn A A tác dụng với dd HCl dư thu được 3,36 lít H_{2} ở dktc . Xác định m và tên kim loại
Ta có: \(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
BT e, có: x.nM = 4nO2 + 2nH2
\(\Rightarrow n_M=\dfrac{1,5}{x}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{13,5}{\dfrac{1,5}{x}}=9x\left(g/mol\right)\)
Với x = 3 thì MM = 27 (g/mol)
→ M là nhôm (Al)
m = mKL + mO2 = 13,5 + 0,3.32 = 23,1 (g)
Đúng 2
Bình luận (0)
`n_(O_2)=0,3(mol)`
`n_(H_2)=0,15(mol)`
`4M+xO_2 \rightarrow M_2O_x` (Đk: nhiệt độ)(1)
Từ (1) có `n_M=\frac{1,2}{x} (mol) (I)`
`\Rightarrow n_(M_(dư))=\frac{13,5}{M}-\frac{1,2}{x} (mol)`
PTHH:
`2M+2xHCl\rightarrow 2MCl_x+xH_2` (2)
Từ (2) có: `n_M=\frac{0,3}{x} (mol)(II)`
Từ (I), (II) có:
`\frac{13,5}{M}-\frac{1,2}{x}=\frac{0,3}{x}`
Với `x=3` `\Rightarrow M=27`
M là Al.
`m=102.0,1+0,1.27=12,9(g)`
Đúng 1
Bình luận (2)
Cho 2,16 gam một kim loại R hóa trị (III) tác dụng hết với lượng khí oxi dư, thu được 4,08 gam một oxit có dạng R 2 O 3 . Xác định tên và kí hiệu hóa học của kim loại R.
Cho 4,6 gam kim loại R có hóa trị I tác dụng hoàn toàn với nước ở nhiệt độ thường , sau phản ứng thu được 8 gam base và thấy có khí hydrogen thoát ra ngoài .
a. Viết PTHH của phản ứng
b. Xác định kim loại R
4.Cho cùng một lượng các kim loại Mg,Al,Fe vào dung dịch H2SO4.Kim loại nào cho nhiều hidro hơn ?5.a)Cho 7,8 gam một kim loại X hóa trị I tác dụng hoàn toàn với nước tạo thành 2,24 lít khí H2(đktc).Xác định kim loại X.b)Hòa tan hoàn toàn 7,65 gam một kim loại M chưa rõ hóa trị vào dung dịch axit HCL dư,thu được 9,408 lít khí H2(đktc).Tìm kim loại M.6.A là oxit của một kim loại ,khử hoàn toàn 1,6(g) A thì cần 672ml Hidro(đktc).Nếu lấy toàn bộ kim loại vừa thu được cho phản ứng với dung dịch HCL d...
Đọc tiếp
4.Cho cùng một lượng các kim loại Mg,Al,Fe vào dung dịch H2SO4.Kim loại nào cho nhiều hidro hơn ?
5.a)Cho 7,8 gam một kim loại X hóa trị I tác dụng hoàn toàn với nước tạo thành 2,24 lít khí H2(đktc).Xác định kim loại X.
b)Hòa tan hoàn toàn 7,65 gam một kim loại M chưa rõ hóa trị vào dung dịch axit HCL dư,thu được 9,408 lít khí H2(đktc).Tìm kim loại M.
6.A là oxit của một kim loại ,khử hoàn toàn 1,6(g) A thì cần 672ml Hidro(đktc).Nếu lấy toàn bộ kim loại vừa thu được cho phản ứng với dung dịch HCL dư thì thu được 0,448 lít hidro (đktc).Xác định CTHH của A
hic :'( tuần sau em kiểm tra rồi
Đốt cháy hoàn toàn 1,08 gam bột nhôm.
a. Tính thể tích khí oxi cần dùng (đktc).
b. Lượng khí oxi đã phản ứng ở trên vừa đủ tác dụng với 3,84 gam một kim loại A có hóa trị II. Xác định kim loại A.
4Al+3O2-to>2Al2O3
0,04---0,03------0,02 mol
n Al=\(\dfrac{1,08}{27}\)=0,04 mol
=>VO2=0,03.22,4=0,672l
b)
2A+O2-to>2AO
0,06--0,03 mol
=>\(\dfrac{3,84}{A}=0,06\)
=>A=64 :=>Al là Đồng
Đúng 2
Bình luận (2)
Cho 3,36 lit khí oxi (ở đktc) phản ứng hoàn toàn với 1 kim loại hóa trị III thu được 10,2g oxit. Xác định tên kim loại.
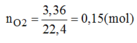
Gọi A là kí hiệu của kim loại có hóa trị III, M A là nguyên tử khối của A.
Ta có PTHH:

Theo PTHH trên ta có:
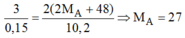
Vậy A là nhôm.
Đúng 0
Bình luận (0)
Cho 20 gam kim loại R có hóa trị II tác dụng hoàn toàn với nước ở nhiệt độ thường , sau phản ứng thu được dung dịch base và thấy có 11,2 lít khí hydrogen thoát ra ngoài .
a. Viết PTHH của phản ứng
b. Xác định kim loại R. Biết thể tích các khí đo ở đktc
\(a.R+2H_2O\rightarrow R\left(OH\right)_2+H_2\\
b.n_{H_2}=\dfrac{11,2}{22,4}=0,5mol\\
n_R=n_{H_2}=0,5mol\\
M_R=\dfrac{20}{0,5}=40g/mol\)
Vậy kim loại R là Ca
Đúng 2
Bình luận (0)
Khử hoàn toàn 24 gam Oxit của một kim loại hóa trị II cần dùng hết 6,72 lít khí Hidro( đktc) ở nhiệt độ cao thu được kim loại và nước. Xác định kim loại, Công thức Oxit và gọi tên Oxít trên
Gọi CTHH oxit là RO
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: RO + H2 --to--> R + H2O
0,3<-0,3
=> \(M_{RO}=\dfrac{24}{0,3}=80\left(g/mol\right)\)
=> MR = 64 (g/mol)
=> R là Cu
CTHH của oxit là CuO (đồng(II) oxit)
Đúng 2
Bình luận (0)
gọi cthh là R
nH2 = 6,72 : 22,4 = 0,3 (mol)
pthh : RO + H2 -t--> R +H2O
0,3<-0,3 (mol)
=> M Oxit = 24 : 0,3 = 80 (g/mol)
=> M R = 80 - 16 = 64 (g/mol )
=> R là Cu
=> CTHH của Oxit là CuO ( đồng (!!) Oxit)
Đúng 0
Bình luận (0)
Gọi công thức của oxit cần tìm là RO.
RO (0,3 mol) + H2 (0,3 mol) \(\underrightarrow{t^o}\) R + H2O.
Phân tử khối của oxit là 24/0,3=80 (g/mol).
Kim loại và công thức của oxit lần lượt là đồng (Cu) và CuO (đồng (II) oxit).
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
























