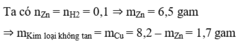Cho 2,1 gam kim loại A hoá trị I vào nước dư thu được lượng H2 nhỏ hơn 1,12 lít khí ở(đkt). Nếu cho 8,2 gam kim loại A vào nước dư thì lượng H2 thoát ra vượt quá 2,24 lít ở (đkt). Xác định kim loại A ?

Những câu hỏi liên quan
Cho 2,1 gam kim loại A hoá trị I vào nước dư thu được lượng H2 nhỏ hơn 1,12 lít khí ở(đkt). Nếu cho 8,2 gam kim loại A vào nước dư thì lượng H2 thoát ra vượt quá 2,24 lít ở (đkt). Xác định kim loại A ?
2A + H20 ---> H2 + A20
Trường hợp 1 : nH2 < 0,05 ⇒⇒ nA < 0,1 => MA > 2,1 / 0,1 = 21
Trường hợp 2 : nH2 > 0,1 => nA > 0,2 => MA < 41
=> A là Rb ( 37 , hóa trị l )
Đúng 3
Bình luận (0)
Cho 2,1g kim loại A có hóa trị I vào nước dư thu được lượng khí H2 nhỏ hơn 1,12 lít (dktc). Nếu cho 8,2g kim loại A vào nước dư thu được lượng khí H2 thoát ra vượt quá 2,24 lít (Đktc). Xác định kim loại A.
2A +H2O ----> H2 +A2O
trường hợp 1: nH2< 0,05 => nA< 0,1 => MA > 2,1/0,1=21
trường hợp 2:nH2>0,1 => nA> 0,2 => MA < 41
=> A là Rb(37,hóa trị I )
Đúng 0
Bình luận (1)
theo mik thì là như vậy :
2A +H2O ----> H2 +A2O
trường hợp 1: nH2< 0,05 => nA< 0,1 => MA > 2,1/0,1=21
trường hợp 2:nH2>0,1 => nA> 0,2 => MA < 41
=> A là Rb(37,hóa trị I )
Chúc bn học tốt
Đúng 0
Bình luận (0)
2A + H20 ---> H2 + A20
Trường hợp 1 : nH2 < 0,05 \(\Rightarrow\) nA < 0,1 => MA > 2,1 / 0,1 = 21
Trường hợp 2 : nH2 > 0,1 => nA > 0,2 => MA < 41
=> A là Rb ( 37 , hóa trị l )
Đúng 0
Bình luận (1)
Cho 2,1 gam kim loại A hóa trị I vào nước dư thu được lượng khí H2 nhỏ hơn 1,12 lít (dktc). Nếu cho 8,2g kim loại A vào nước dư thu được lượng khí H2 thoát ra vượt quá 2,24 lít (Đktc). Xác định kim loại A.
2A + H2O \(\rightarrow\) H2 + A2O
Trường hợp 1 : nH2 < 0,05 \(\Rightarrow\) nA < 0,1 \(\Rightarrow\) MA > 2,1/0,1 = 21
Trường hợp 2 : nH2 > 0,1 \(\Rightarrow\) nA > 0,2 \(\Rightarrow\) MA < 41
\(\Rightarrow\) A là Rb ( 37 , hóa trị 1 )
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 4g hỗn hợp X gồm Fe và kim loại hóa trị II vào dung dịch HCl dư thu được 2,24 lít khí H2 ở (đkt). Nếu dùng 2,4g kim loại hóa trị II hòa tan vào dung dịch HCl thì dùng không hết 0,5 mol dung dich HCl.
a. Xác định tên kim loại hóa trị II.
b. Tính thành phần % theo khối lượng của mỗi kim loại trong 4g hỗn hợp X
Cho 2,1g kim loại A có hóa trị I vào nước dư thu được lượng khí H2 nhỏ hơn 1,12 lít (dktc). Nếu cho 8,2g kim loại A vào nước dư thu được lượng khí H2 thoát ra vượt quá 2,24 lít (Đktc). Xác định kim loại A.
\(2A+2HCl\rightarrow2ACl+H_2\)
TH1:
\(n_A=\frac{2,1}{A}\left(mol\right)\)
\(\Rightarrow n_{H_2}=\frac{2,1}{2A}< \frac{1,12}{22,4}=0,05\)
\(\Leftrightarrow A>21\left(1\right)\)
TH2:
\(n_A=\frac{8,2}{A}\left(mol\right)\)
\(\Rightarrow n_{H_2}=\frac{8,2}{2A}>\frac{2,24}{22,4}=0,1\)
\(\Leftrightarrow A< 41\left(2\right)\)
Từ (1) và (2) ta suy ra A là Na hoặc K
Đúng 0
Bình luận (2)
Cho 2,1g kim loại A hoá trị I vào nước(dư) thu đc lượng H2 nhỏ hơn 1,12 lít khí (đktc). Nếu cho 8,2g kim loại A tan hết trong nước thì lượng H2 thoát ra vượt quá 2,24 lít(đktc). Xác định kim loại A
\(n_{A\left(1\right)}=\frac{2,1}{A}\left(mol\right);n_{A\left(2\right)}=\frac{8,2}{A}\left(mol\right)\)
PTHH 1: 2A + 2H2O --> 2AOH + H2
\(\frac{2,1}{A}\) -------------------------> \(\frac{1,05}{A}\) (mol)
PTHH 2: 2A + 2H2O --> 2AOH + H2
\(\frac{8,2}{A}\) --------------------------> \(\frac{4,1}{A}\) (mol)
=> \(\frac{1,05}{A}< \frac{1,12}{22,4}\) ; \(\frac{4,1}{A}>\frac{2,24}{22,4}\)
=> \(\frac{1,05}{A}< 0,05\); \(\frac{4,1}{A}>0,1\)
=> 21<A<41 => A là Na,K
MIK NGHĨ ZẬY
\(2A+2H_2O\rightarrow2Aoh+H_2\)
- TN1:
\(n_{H2}=0,05\left(mol\right)\)
\(n_A=\frac{2,1}{A}\left(mol\right)\)
\(\Rightarrow\frac{1,05}{A}< 0,05\Rightarrow A>21\left(1\right)\)
- TN2:
\(n_{H2}=0,1\left(mol\right)\)
\(n_A=\frac{8,2}{A}\left(mol\right)\)
\(\Rightarrow\frac{4,1}{A}>0,1\Rightarrow A< 41\left(2\right)\)
\(\left(1\right)+\left(2\right)\Rightarrow21< A< 41\)
Vậy A= 23 (Na) hoặc A= 39 (K)
Cho 8,2 gam hỗn hợp kim loại Zn và Cu vào dung dịch HCl (dư). Sau khi phản ứng xảy ra hoàn toàn, thu được 2,24 lít khí
H
2
(ở đktc) và m gam kim loại không tan. Giá trị của m là A. 6,4. B. 1,7. C. 1,8. D. 6,5.
Đọc tiếp
Cho 8,2 gam hỗn hợp kim loại Zn và Cu vào dung dịch HCl (dư). Sau khi phản ứng xảy ra hoàn toàn, thu được 2,24 lít khí H 2 (ở đktc) và m gam kim loại không tan. Giá trị của m là
A. 6,4.
B. 1,7.
C. 1,8.
D. 6,5.
Cho 8,2 gam hỗn hợp kim loại Zn và Cu vào dung dịch HCl (dư). Sau khi phản ứng xảy ra hoàn toàn, thu được 2,24 lít khí H2 (ở đktc) và m gam kim loại không tan. Giá trị của m là
A. 6,4.
B. 1,7.
C. 1,8.
D. 6,5.
Chọn đáp án B
Ta có nZn = nH2 = 0,1 ⇒ mZn = 6,5 gam
⇒ mKim loại không tan = mCu = 8,2 – mZn = 1,7 gam
Đúng 0
Bình luận (0)
Cho 29,34 gam hỗn hợp A gồm kim loại R (hóa trị I) và kim loại t (hóa trị II) tan hoàn toàn trong nước dư, thu được 5,376 lít khí H2 (ở đktc). Đem 10,66 gam kim loại kali trộn thêm vào 29,34 gam hỗn hợp A ở trên thì thu được hỗn hợp B có thành phần % theo khối lượng của kim loại kali là 29 35%. Xác định kim loại R và M?
Nếu A không có K:
\(\%m_K=\dfrac{10,66}{29,34+10,66}\cdot100\%=26,65\%\ne29,35\%\\ R:Kali\\ K+H_2O->KOH+\dfrac{1}{2}H_2\\ M+2H_2O->M\left(OH\right)_2+H_2\\ n_K=a,n_M=b\left(mol\right)\\ n_{H_2}=0,5a+b=\dfrac{5,376}{22,4}=0,24mol\\ \%m_{K\left(B\right)}=\dfrac{39a+10,66}{29,34+10,66}\cdot100=29,35\\ a=0,028\\ b=0,226\\ M_M=\dfrac{29,34-39\cdot0,028}{0,226}=125\left(g\cdot mol^{^{-1}}\right)\)
Vậy không có kim loại kiềm thổ thoả đề
Đúng 1
Bình luận (0)