26
Đốt cháy hoàn toàn 13,44 lít khí H2 (đktc) với khí oxi. Khối lượng nước sẽ thu được là
A.
18,0g.
B.
6,4g.
C.
10,8g.
D.
5,4g.
Đốt cháy hoàn toàn 13,44 lít khí H2(ở đktc) với khí oxi.Khối lượng nước sẽ thu được là:
A 18 gam
B 10,8 gam
C 6,4 gam
D 5,4 gam
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Theo PT: \(n_{H_2O}=n_{H_2}=0,6\left(mol\right)\Rightarrow m_{H_2O}=0,6.18=10,8\left(g\right)\)
→ Đáp án: B
Hòa tan hoàn toàn 11,2 gam Fe trong d.d HCl dư
a. Tính khối lượng FeCl2 thu được?
b. Tính khối lượng và thể tích (đktc) khí H2 thu được
c. Lượng H2 đó muốn đốt cháy hoàn toàn cần bao nhiêu lít khí oxi (đktc)
\(a,PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ \Rightarrow n_{Fe}=n_{FeCl_2}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ \Rightarrow m_{FeCl_2}=0,2\cdot127=25,4\left(g\right)\\ b,n_{H_2}=n_{Fe}=0,2\left(mol\right)\\ \Rightarrow\left\{{}\begin{matrix}m_{H_2}=0,2\cdot2=0,4\left(g\right)\\V_{H_2\left(đktc\right)}=0,2\cdot22,4=4,48\left(l\right)\end{matrix}\right.\)
\(c,PTHH:2H_2+O_2\rightarrow^{t^0}2H_2O\\ \Rightarrow n_{O_2}=\dfrac{1}{2}n_{H_2}=0,1\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,1\cdot22,4=2,24\left(l\right)\)
Tính khối lượng của nước ở trạng thái lỏng khi đốt cháy hoàn toàn 13,44 lít khí oxi ( ở đktc) với hidro.
Số mol của khí oxi là:
\(n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
\(PTHH:2H_2+O_2\xrightarrow[]{t^0}2H_2O\)
tỉ lệ : 2 1 2 (mol)
số mol : 1,2 0,6 1,2 (mol)
Khối lượng nước là:
\(m_{H_2O}=1,2.18=21,6\left(g\right)\)
a. Đun nóng hoàn toàn 18,96 gam KMnO4 thu đc bao nhiêu lít khí oxi ở đktc?
b. Đốt cháy 5,4g nhôm trong lượng khí oxi thu đc ở trên.
- Nhôm hay khí oxi, chất nào còn dư và dư bao nhiêu gam?
- Tính khối lượng nhôm oxit thu đc.
\(n_{KMnO_4}=\dfrac{18.96}{158}=0.12\left(mol\right)\)
\(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
\(0.12...........................................0.06\)
\(V_{O_2}=0.06\cdot22.4=1.344\left(l\right)\)
\(n_{Al}=\dfrac{5.4}{27}=0.2\left(mol\right)\)
\(4Al+3O_2\underrightarrow{t^0}2Al_2O_3\)
\(0.08.....0.06.......0.04\)
\(m_{Al\left(dư\right)}=\left(0.2-0.08\right)\cdot27=3.24\left(g\right)\)
\(m_{Al_2O_3}=0.04\cdot102=4.08\left(g\right)\)
Khối lượng nước (ở trạng thái lỏng) sẽ thu được khi đốt cháy hoàn toàn 1,12 lít khí hiđro (đktc) với khí oxi là (H = 1; O = 16)
Mn giúp em vs ạ em cảm ơn \(@^0^@)/
Câu 7: Đốt cháy hoàn toàn 10,8 gam hợp chất hữu cơ X ( C, H, O) thu được 13,44 lít CO2 (đktc) và
10,8 gam H2 O. Biết tỉ khối của X so với khí oxi bằng 2,25. Công thức phân tử của X
Câu 6: Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ X thu được 5,6 lít CO2 (đktc) và 5,4 gam H2O.
Biết tỉ khối của X so với CO2 bằng 2. Công thức phân tử của X
Câu 8: Kết quả phân tích nguyên tố hợp chất X cho biết %mC = 40% ; %mH = 6,67% còn lại là oxi.
Tỉ khối hơi của X so với khí oxi bằng 1,875. Công thức phân tử của X
Câu 7:
\(n_{CO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\)
Bảo toàn C: nC = 0,6 (mol)
Bảo toàn H: nH = 1,2 (mol)
=> \(n_O=\dfrac{10,8-0,6.12-1,2}{16}=0,15\left(mol\right)\)
=> nC : nH : nO = 0,6 : 1,2 : 0,15 = 4:8:1
=> CTPT: (C4H8O)n
Mà M = 2,25.32 = 72(g/mol)
=> n = 1
=> CTPT: C4H8O
Câu 6
\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
Bảo toàn C: nC = 0,25 (mol)
Bảo toàn H: nH = 0,6 (mol)
=> \(n_O=\dfrac{4,4-0,25.12-0,6.1}{16}=0,05\left(mol\right)\)
nC : nH : nO = 0,25 : 0,6 : 0,05 = 5:12:1
=> CTPT: (C5H12O)n
Mà M = 44.2=88(g/mol)
=> n = 1
=> CTPT: C5H12O
Câu 8:
MX = 1,875.32 = 60 (g/mol)
Giả sử có 1 mol chất X => mX = 60.1 = 60 (g)
\(m_C=\dfrac{60.40}{100}=24\left(g\right)=>n_C=\dfrac{24}{12}=2\left(mol\right)\)
\(m_H=\dfrac{60.6,67}{100}=4\left(g\right)=>n_H=\dfrac{4}{1}=4\left(mol\right)\)
\(m_O=60-24-4=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> Trong 1 mol X chứa 2 mol C, 4 mol H, 2 mol O
=> CTPT: C2H4O2
Câu 7: Đốt cháy hoàn toàn 10,8 gam hợp chất hữu cơ X ( C, H, O) thu được 13,44 lít CO2 (đktc) và
10,8 gam H2 O. Biết tỉ khối của X so với khí oxi bằng 2,25. Công thức phân tử của X
Câu 6: Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ X thu được 5,6 lít CO2 (đktc) và 5,4 gam H2O.
Biết tỉ khối của X so với CO2 bằng 2. Công thức phân tử của X
Câu 8: Kết quả phân tích nguyên tố hợp chất X cho biết %mC = 40% ; %mH = 6,67% còn lại là oxi.
Tỉ khối hơi của X so với khí oxi bằng 1,875. Công thức phân tử của X
Nhiệt phân hoàn toàn m (g) KMnO4 thu được 3,36 lít khí O2(đktc).
a. Tìm m?
b. Nếu cho lượng oxi trên tác dụng với 8,96 lít khí H2. Tính khối lượng nước tạo thành. Biết phản ứng xảy ra hoàn toàn
a)nO2=\(\dfrac{3.36}{22.4}\)=0,15(mol)
2KMnO4(to)→K2MnO4+MnO2+O2
Theo PT: nKMnO4=2nO2=0,3(mol)
→m=mKMnO4=0,3.158=47,4(g)
b)nH2=\(\dfrac{8.96}{22.4}\)=0,4(mol)
2H2+O2(to)→2H2O
Vì \(\dfrac{nH_2}{2}\)<nO2→O2nH2 dư
Theo PT: nH2O=nH2=0,4(mol)
→mH2O=0,4.18=7,2(g)
Tính khối lượng nước ở trạng thái lỏng sẽ thu được khí đốt cháy hoàn toàn 112l khí hiđro (đktc) với oxi?
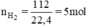
Phương trình phản ứng tổng hợp nước:
2H2 + O2 → 2H2O.
Theo pt: nH2O = nH2 = 5mol.
mH2O= 5.18 = 90g.
Khối lượng riêng của nước là 1g/ml thể tích nước lỏng thu được là 90ml.