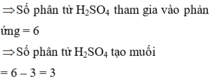H2SO4(đặc nóng)+Fe→Fe2(SO4)3+........+SO2↑

Những câu hỏi liên quan
Trong các sơ đồ phản ứng hóa học sau đây: 1. Fe3O4 + HCl → FeCl2 + FeCl3 + H2O 2. Fe(OH)3 + H2SO4 đặc, nóng → Fe2(SO4)3 + SO2 + H2O 3. FeO + HNO3 loãng → Fe(NO3)3 + NO + H2O 4. FeCl2 + HNO3 loãng → Fe(NO3)3 + HCl + NO + H2O 5. Al + HNO3 loãng → Al(NO3)3 + H2 6. FeO + H2SO4 đặc, nóng → Fe2(SO4)3 + SO2 + H2O Có bao nhiêu phản ứng viết sai? A. 1 B. 2 C. 3 D. 4
Đọc tiếp
Trong các sơ đồ phản ứng hóa học sau đây:
1. Fe3O4 + HCl → FeCl2 + FeCl3 + H2O
2. Fe(OH)3 + H2SO4 đặc, nóng → Fe2(SO4)3 + SO2 + H2O
3. FeO + HNO3 loãng → Fe(NO3)3 + NO + H2O
4. FeCl2 + HNO3 loãng → Fe(NO3)3 + HCl + NO + H2O
5. Al + HNO3 loãng → Al(NO3)3 + H2
6. FeO + H2SO4 đặc, nóng → Fe2(SO4)3 + SO2 + H2O
Có bao nhiêu phản ứng viết sai?
A. 1
B. 2
C. 3
D. 4
Fe(OH)2+H2SO4 đặc nóng ----->Fe2(SO4)3+SO2+H2O
Cu2O+HNO3---->Cu(NO3)2+NH4NO3+H2O
FexOy+H2SO4---->Fe2(SO4)3+SO2+H2O
FexOy+HNO3---->Fe(NO3)2+NO2+H2O
FexOy+NO3---->Fe(NO3)3+NtOz+H2O
2Fe(OH)2 + 4H2SO4 ---> Fe2(SO4)3 + SO2 + 6H2O
4Cu2O + 18HNO3 ---> 8Cu(NO3)2 + NH4NO3 + 7H2O
4FexOy + (12x-4y) H2SO4 ---> 2x Fe2(SO4)3 + (6x-4y) SO2 + (12x-4y) H2O
FexOy + (4x-2y) HNO3 ---> x Fe(NO3)2 + (2x-2y) NO2 + (2x-y) H2O
(5t-2z) FexOy + (18xt - 2yt - 6xz) HNO3---> (5tx-2zx) Fe(NO3)3 + (3x-2y) NtOz + (9xt-yt-3xz) H2O
Đúng 0
Bình luận (0)
Cho sơ đồ phản ứng:
Fe
+
H
2
SO
4
đặc/nóng
→
Fe
2
(
SO
4
)
3
+
SO
2
+
H
2
O
Số phân tử
H
2
SO
4
bị khử và số phân tử ...
Đọc tiếp
Cho sơ đồ phản ứng:
Fe + H 2 SO 4 đặc/nóng → Fe 2 ( SO 4 ) 3 + SO 2 + H 2 O
Số phân tử H 2 SO 4 bị khử và số phân tử H 2 SO 4 tạo muối là
A. 6 và 3.
B. 3 và 6.
C. 6 và 6.
D. 3 và 3.
Cho sơ đồ phản ứng: H2SO4 (đặc nóng) + Fe ® Fe2(SO4)3 + SO2 +H2O Số phân tử H2SO4 bị khử trong phương trình hoá học của phản ứng trên là A. 2. B. 4. C. 6. D. 3.
Đọc tiếp
Cho sơ đồ phản ứng: H2SO4 (đặc nóng) + Fe ® Fe2(SO4)3 + SO2 +H2O
Số phân tử H2SO4 bị khử trong phương trình hoá học của phản ứng trên là
A. 2.
B. 4.
C. 6.
D. 3.
Đáp án D
Số oxi hoá các nguyên tố thay đổi:
Fe 0 + H 2 S + 6 O 4 ( đặc ) → t ° Fe 2 + 3 ( SO 4 ) 3 + S + 4 O 2 + H 2 O
Số phân tử H2SO4 bị khử chính là số phân tử H2SO4 là chất oxi hoá. H2SO4 là chất oxi hoá khi S + 6 chuyển thành S + 4
Các quá trình nhường, nhận electron:
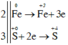
=> Số phân tử H2SO4 bị khử là 3
Đúng 0
Bình luận (0)
Cho sơ đồ phản ứng: H2SO4 (đặc, nóng) + Fe - Fe2(SO4)3 + H2O + SO2. Số phân tử H2SO4 bị khử và số phân tử H2SO4 trong phương trình hóa học của phản ứng trên là: A. 3 và 6 B. 3 và 3 C. 6 và 3 D. 6 và 6
Đọc tiếp
Cho sơ đồ phản ứng:
H2SO4 (đặc, nóng) + Fe -> Fe2(SO4)3 + H2O + SO2.
Số phân tử H2SO4 bị khử và số phân tử H2SO4 trong phương trình hóa học của phản ứng trên là:
A. 3 và 6
B. 3 và 3
C. 6 và 3
D. 6 và 6
Chọn B
2Fe + 6H2SO4 -> Fe2(SO4)3 + 3SO2 + 6H2O
Số phân tử bị khử thành SO2 chính bằng số SO2
Đúng 0
Bình luận (0)
Cân bằng các phương trình sao1. FeCO3 + H2SO4 --- Fe2(SO4)3 + SO2 + CO2 + H2O.2. FeSO4 + H2SO4 ---- Fe2(SO4)3 + SO2 + H2O.3. Fe(OH)2 + H2SO4 ------ Fe2(SO4)3 + SO2 + H2O.4. Fe(NO3)2 + HNO3 ------- Fe(NO3)3 + NO + H2O.5. K2Cr2O7 + HCl → KCl + CrCl3 + Cl2 + H2O6. KClO3 + HCl → KCl + Cl2 + H2O7. KNO3+ Al → KNO2 + Al2O38. KClO3+ S → KCl + SO29. KMnO4 + SO2 + H2O ---- MnSO4 + K2SO4 + H2SO4.10. K2Cr2O7 + FeSO4 + H2SO4 -------- Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 +...
Đọc tiếp
Cân bằng các phương trình sao
1. FeCO3 + H2SO4 ---> Fe2(SO4)3 + SO2 + CO2 + H2O.
2. FeSO4 + H2SO4 ----> Fe2(SO4)3 + SO2 + H2O.
3. Fe(OH)2 + H2SO4 ------> Fe2(SO4)3 + SO2 + H2O.
4. Fe(NO3)2 + HNO3 -------> Fe(NO3)3 + NO + H2O.
5. K2Cr2O7 + HCl → KCl + CrCl3 + Cl2 + H2O
6. KClO3 + HCl → KCl + Cl2 + H2O
7. KNO3+ Al → KNO2 + Al2O3
8. KClO3+ S → KCl + SO2
9. KMnO4 + SO2 + H2O ----> MnSO4 + K2SO4 + H2SO4.
10. K2Cr2O7 + FeSO4 + H2SO4 --------> Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O.
Cân bằng các phương trình sao
1. 2FeCO3 + 4H2SO4 → Fe2(SO4)3 + SO2 + 2CO2 + 4H2O
2. 2FeSO4 + 2H2SO4 → Fe2(SO4)3 + SO2 + 2H2O
3. 2Fe(OH)2 + 4H2SO4 → Fe2(SO4)3 + SO2 + 6H2O
4. 3Fe(NO2)2 + 8HNO3 → 3Fe(NO3)3 + 5NO + 4H2O
5. K2Cr2O7 + 14HCl → 2KCl + 2CrCl3 + 3Cl2 + 7H2O
Đúng 4
Bình luận (0)
6. KClO3 + 6HCl → 3Cl2 + KCl + 3H2O
7. 3KNO3+ 2Al → 3KNO2 + Al2O3
8. 2KClO3 + 3S → 2KCl + 3SO2
9. 5SO2 + 2KMNO4 + 2H2O → 2MNSO4 + K2SO4 + 2H2SO4
10. 6FeSO4 + K2Cr2O7 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
Đúng 3
Bình luận (0)
Cân bằng các PTHH sau bằng phương pháp oxi hóa khử
1. FeO + H2SO4 → Fe2(SO4)3 + SO2 + H2O
2. FeCO3 + H2SO4 → Fe2(SO4)3 + SO2 + CO2 + H2O
3. FeSO4 + H2SO4 → Fe2(SO4)3 + SO2 + H2O
4. Fe(OH)2 + H2SO4 → Fe2(SO4)3 + H2S + H2O
5. Al + HNO3 → Al(NO3)3 + N2 + H2O
1.
| 2Fe+2 ---> 2Fe+3 + 1e | x1 |
| S+6 + 2e ---> S+4 | x1 |
2FeO + 4H2SO4 ---> Fe2(SO4)3 + SO2 + 4H2O
2.
| 2Fe+2 ---> 2Fe+3 + 2e | x1 |
| S+6 + 2e ---> S+4 | x1 |
2FeCO3 + 4H2SO4 ---> Fe2(SO4)3 + 2CO2 + SO2 + 4H2O
3.
| 2Fe+2 ---> 2Fe+3 + 2e | x1 |
| S+6 + 2e ---> S+4 | x1 |
2FeSO4 + 2H2SO4 ---> Fe2(SO4)3 + SO2 + 2H2O
4.
| 2Fe+2 ---> 2Fe+3 + 2e | x4 |
| S+6 + 8e ---> S-2 | x1 |
8Fe(OH)2 + 13H2SO4 ---> 4Fe2(SO4)3 + H2S + 20H2O
5.
| Al0 ---> Al+3 + 3e | x10 |
| 2N+5 ---> 2N0 | x3 |
10Al + 36HNO3 ---> 10Al(NO3)3 + 3N2 + 18H2O
Đúng 0
Bình luận (0)
Viết các PTHH biểu diễn các chuyển đổi saU:a)S→ SO2→ SO3→ H2SO4→ SO2→ H2SO3→ CaSO3→ SO2 ↓ ↓ Na2SO3→NaCl Na2SO4 b)Fe2(SO4)3→ FeCl3→ Fe(OH)3→ Fe2O3→ Fe2(SO4)3→Fe(OH)3→Fe2(SO4)3
Đọc tiếp
Viết các PTHH biểu diễn các chuyển đổi saU:
a)
S→ SO2→ SO3→ H2SO4→ SO2→ H2SO3→ CaSO3→ SO2
↓ ↓
Na2SO3→NaCl Na2SO4
b)
Fe2(SO4)3→ FeCl3→ Fe(OH)3→ Fe2O3→ Fe2(SO4)3→Fe(OH)3→Fe2(SO4)3
\(a)\left(1\right)S+O_2\xrightarrow[]{t^0}SO_2\\ \left(2\right)2SO_2+O_2\xrightarrow[V_2O_5]{t^0}2SO_3\\ \left(3\right)SO_3+H_2O\rightarrow H_2SO_4\\ \left(4\right)H_2SO_4+Na_2SO_3\rightarrow Na_2SO_4+SO_2+H_2O\\ \left(5\right)SO_2+H_2O\rightarrow H_2SO_3\\ \left(6\right)H_2SO_3+Ca\left(OH\right)_2\rightarrow CaSO_3+2H_2O\\ \left(7\right)CaSO_3+H_2SO_4\rightarrow CaSO_4+SO_2+H_2O\\ \left(8\right)SO_2+Na_2O\rightarrow Na_2SO_3\\ \left(9\right)Na_2SO_3+2HCl\rightarrow2NaCl+SO_2+H_2O\\ \left(10\right)H_2SO_4+2NaOH\rightarrow Na_2SO_4+2H_2O\)
\(b)\left(1\right)Fe_2\left(SO_4\right)_3+3BaCl_2\rightarrow2FeCl_3+3BaSO_4\\ \left(2\right)FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\\ \left(3\right)2Fe\left(OH\right)_3\xrightarrow[]{t^0}Fe_2O_3+3H_2O\\ \left(4\right)Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ \left(5\right)Fe_2\left(SO_4\right)_3+6NaOH\rightarrow2Fe\left(OH\right)_3+3Na_2SO_4\\ \left(5\right)2Fe\left(OH\right)_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+6H_2O\)
Đúng 2
Bình luận (1)
\(a,S+O_2\rightarrow\left(t^o\right)SO_2\)
\(2O_2+O_2\xrightarrow[V_2O_5]{t^o}2SO_3\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(H_2SO_4+Na_2CO_3\rightarrow Na_2SO_4+H_2O+SO_2\uparrow\)
\(SO_2+H_2O\leftrightarrow H_2SO_3\)
\(H_2SO_3+Ca\left(OH\right)_2\rightarrow CaSO_3+2H_2O\)
\(CaSO_3\rightarrow\left(t^o\right)CaO+SO_2\)
\(SO_2+Na_2O\rightarrow Na_2SO_3\)
\(Na_2SO_3+2HCl\rightarrow2NaCl+H_2O+SO_2\uparrow\)
\(b,Fe_2\left(SO_4\right)_3+3BaCl_2\rightarrow2FeCl_3+3BaSO_4\downarrow\)
\(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\)
\(2Fe\left(OH\right)_3\rightarrow Fe_2O_3+3H_2O\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(Fe_2\left(SO_4\right)_3+6NaOH\rightarrow2Fe\left(OH\right)_3+3Na_2SO_4\)
\(2Fe\left(OH\right)_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+6H_2O\)
Đúng 2
Bình luận (0)
Fe(OH)2+H2SO4 đặc nóng -----> Fe(SO4)3+SO2+H2O
\(2Fe\left(OH\right)_2+4H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+SO_2+6H_2O\)
Đúng 0
Bình luận (3)
Cách tính:
\(|^{Fe^{+2}--1e\rightarrow Fe^{+3}}_{S^{+6}-+2e\rightarrow S^{+4}}|^2_1\)
Đúng 0
Bình luận (0)