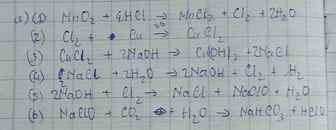Cl2 + H20 —--------> |
Cl2 + NaOH —--------> |
MnO2 + HCL —--------> |
KMnO + HCL —--------> |
NaCl + H2O —--------> |

Những câu hỏi liên quan
Hoàn thành phương trình phản ứng theo chuỗi biên hóa sau (ghi rõ đk nếu có)
a/ MnO2 Cl2→ CuCl2→ NaCl →NAOH → NaClO -→ HC1O
b/ KMNO4→ Cl2→ HCl → KCI → KOH → KCI → Cl2→ FeCl3→ Fe(N03)3
c/ Cl2→ NaCl → AgCl → Cl2→ NaClO –→ Cl2→ CaOCl2
d/ H2 HCl - FeCl2 FeCl3→NaCl → HCI → CaCl2→ CACO3
$a) MnO_2 + 4HCl \xrightarrow{t^o} MnCl_2 + Cl_2 + 2H_2O$
$Cl_2 + Cu \xrightarrow{t^o} CuCl_2$
$CuCl_2 + 2NaOH \to Cu(OH)_2 + 2NaCl$
$2NaCl + 2H_2O \xrightarrow{đpdd, cmn} 2NaOH + H_2 + Cl_2$
$2NaOH + Cl_2 \to NaCl + NaClO + H_2O$
$NaClO + HCl \to NaCl + HClO$
b)
$2KMnO_4 + 16HCl \to 2KCl + 2MnCl_2 + 5Cl_2 + 8H_2O$
$Cl_2 + H_2 \xrightarrow{ánh\ sáng} 2HCl$
$HCl + KOH \to KCl + H_2O$
$2KCl + 2H_2O \xrightarrow{đpdd, cmn} 2KOH + H_2 + Cl_2$
$3Cl_2 + 2Fe \xrightarrow{t^o} 2FeCl_3$
$FeCl_3 + 3AgNO_3 \to Fe(NO_3)_3 + 3AgCl$
Đúng 6
Bình luận (4)
a) Cl ➝(1) NaCl ➝(2) HCl ➝(3) Cl ➝(4) CaOCl
b) HCl ➝ Cl2 ➝ FeCl3 ➝ NaCl ➝ HCl
c) MnO2 ➝ Cl2 ➝ KCl ➝ HCl ➝ Cl2 ➝ Clorua vôi
d) KMnO4 ➝ Cl2 ➝ KCl ➝ Cl2 ➝ Br2 ➝I2
giúp em với ạ
a, Cl2 + 2Na -> (t°) 2NaCl
2NaCl + H2SO4 -> Na2SO4 + 2HCl
4HCl + MnO2 -> MnCl2 + 2H2O + Cl2
Ca + Cl2 -> (t°) CaCl2
b, 4HCl + MnO2 -> MnCl2 + 2H2O + Cl2
2Fe + 3Cl2 -> (t°) 2FeCl3
FeCl3 + 3NaOH -> Fe(OH)3 + 3NaCl
2NaCl + H2SO4 -> Na2SO4 + 2HCl
c, MnO2 + 4HCl -> MnCl2 + 2H2O + Cl2
3Cl2 + 6KOH (đặc nóng) -> 5KCl + KClO3 + 3H2O
2KCl + H2SO4 -> K2SO4 + 2HCl
4HCl + MnO2 -> MnCl2 + 2H2O + Cl2
2Cl2 + 2Ca(OH)2 -> CaCl2 + Ca(OCl)2 + 2H2O
d, 16HCl + 2KMnO4 -> 5Cl2 + 8H2O + 2KCl + 2MnCl2
3Cl2 + 6KOH (đặc nóng) -> 5KCl + KClO3 + 3H2O
2KCl -> (đpnc) 2K + Cl2
Cl2 + 2NaBr -> 2NaCl + Br2
Br2 + 2NaI -> 2NaBr + I2
Đúng 3
Bình luận (0)
Bài 1: Hoàn thành sơ đồ phản ứng sau kèm theo điều kiện (nếu có): a. HCl → Cl2 → FeCl3 → NaCl → HCl → CuCl2→ Cu(OH)2→ CuO→ Cu→CuCl2. b. KMnO4→Cl2→HCl →FeCl3→AgCl→ Cl2→Br2→I2 →NaI →AgI c. MnO2 → Cl2 → NaCl → HCl → Cl2 → nước giaven CaOCl2 d. HCl → Cl2→ FeCl3 → Fe(OH)3 → Fe2(SO4)3→ Fe(OH)3→ Fe2O3→ FeCl3→AgCl→ Cl2.
Cho các phản ứng : 1. Cl2 + NaBr→ NaCl + Br2 2. Cu + Cl2 → CuCl2 3. Cl2 + NaOH→ NaCl + NaClO + H2O 4. Cl2 + 2FeCl2 → 2FeCl3 5. Cl2 + H2O HCl + HClO Số phản ứng Clo đóng vai trò làm chất oxi hóa là: A. 5 B. 2 C. 3 D. 4
Đọc tiếp
Cho các phản ứng :
1. Cl2 + NaBr→ NaCl + Br2
2. Cu + Cl2 → CuCl2
3. Cl2 + NaOH→ NaCl + NaClO + H2O
4. Cl2 + 2FeCl2 → 2FeCl3
5. Cl2 + H2O ![]() HCl + HClO
HCl + HClO
Số phản ứng Clo đóng vai trò làm chất oxi hóa là:
A. 5
B. 2
C. 3
D. 4
Cân bằng PTHH :
a. Na + Cl2 + ? ----------- ?
b. CxHyO2 + O2 ----------------- CO2 + H20
c. FeS2 + O2 ------------- ? + ?
d. NaOH + ? --------------- NaCl + H2O
e. Fe(OH)3 --------------- ? + ?
f. Fe + Cl2 ---------------- ?
g. e(OH)2 + O2 + H20 -------------- Fe(OH)3
h. Fe3O4 + Al -------------- Fe + CO2
i. FexOy + HCL --------------- ? + H20
k. FexOy + CO -------- Fe + CO2
l. CnH2n+2 + O2 --------- CO2 +...
Đọc tiếp
Cân bằng PTHH :
a. Na + Cl2 + ? -----------> ?
b. CxHyO2 + O2 -----------------> CO2 + H20
c. FeS2 + O2 -------------> ? + ?
d. NaOH + ? ---------------> NaCl + H2O
e. Fe(OH)3 ---------------> ? + ?
f. Fe + Cl2 ----------------> ?
g. e(OH)2 + O2 + H20 --------------> Fe(OH)3
h. Fe3O4 + Al --------------> Fe + CO2
i. FexOy + HCL ---------------> ? + H20
k. FexOy + CO --------> Fe + CO2
l. CnH2n+2 + O2 ---------> CO2 + H2O
a. \(2Na+Cl_2\rightarrow2NaCl\)
b. \(C_xH_yO_2+\left(\frac{x+y}{4-1}\right)O_2\rightarrow xCO_2+\frac{y}{2}H_2O\)
c. \(4FeS_2+11O_2\rightarrow2Fe_2O_3+8SO_2\)
d. \(NaOH+HCl\rightarrow NaCl+H_2O\)
e. \(2Fe\left(OH\right)_3\rightarrow Fe_2O_3+3H_2O\)
f. \(2Fe+2Cl_2\rightarrow2FeCl_3\)
g. \(4Fe\left(OH\right)_2+2H_2O+O_2\rightarrow4Fe\left(OH\right)_3\)
h. \(Fe_2O_3+4CO\rightarrow3Fe+4CO_2\)
i. \(Fe_xO_y+2yHCl\rightarrow xFeCl_{\frac{2y}{x}}+yH_2O\)
k. \(Fe_xO_y+yCO\rightarrow xFe+yCO_2\)
l. \(C_nH_{2n+2}+\frac{3n+1}{2}O_2\rightarrow nCO_2+\left(n+1\right)H_2O\)
a. NaCl → Cl2 → FeCl3 → NaCl → HCl → CuCl2 → AgCl.b. CaCO3 → CaCl2 → NaCl → NaOH → NaClO → NaCl → Cl2 → FeCl3 → AgClc. KMnO4 → Cl2 → KClO3 → KCl → HCl → CuCl2 → AgCl → Cl2 → clorua vôid. Cl2 → KClO3 → KCl → Cl2 → HCl → FeCl2 → FeCl3 → PbCl2.
Đọc tiếp
a. NaCl → Cl2 → FeCl3 → NaCl → HCl → CuCl2 → AgCl.
b. CaCO3 → CaCl2 → NaCl → NaOH → NaClO → NaCl → Cl2 → FeCl3 → AgCl
c. KMnO4 → Cl2 → KClO3 → KCl → HCl → CuCl2 → AgCl → Cl2 → clorua vôi
d. Cl2 → KClO3 → KCl → Cl2 → HCl → FeCl2 → FeCl3 → PbCl2.
a. NaCl → Cl2 → FeCl3 → NaCl → HCl → CuCl2 → AgCl.
2NaCl+2H2O-đp\mn->2NaOH+H2+Cl2
3Cl2+2Fe-to>2FeCl3
FeCl3+3NaOH->3NaCl+Fe(OH)3
2NaCl+H2SO4-to>Na2SO4+2HCl
2HCl+CuO->CuCl2+H2O
CuCl2+2AgNO3->2AgCl+Cu(NO3)2
Đúng 3
Bình luận (0)
b. CaCO3 → CaCl2 → NaCl → NaOH → NaClO → NaCl → Cl2 → FeCl3 → AgCl
CaCO3+2HCl->CaCl2+H2O+CO2
CaCl2+Na2CO3->2NaCl+CaCO3
2NaCl+2H2o-đp->2NaOH+Cl2+H2
2NaOH+Cl2-to>NaCl+NaClO+H2O
2NaClO-to->2NaCl+O2
2NaCl+2H2O-đp\mn->2NaOH+H2+Cl2
3Cl2+2Fe-to>2FeCl3
FeCl3+3AgNO3->3AgCl+Fe(NO3)3
Đúng 1
Bình luận (0)
Câu 1: viết các phương trình phản ứng xảy ra cho các sơ đồ sau
a,HCl→Cl2→FeCl3→NaCl→HCl→CuCl2→AgCl
b,KMnO4→Cl2→HCl→FeCl3→AgCl→Cl2→Br2→I2→ZnI2→Zn(OH)2
c,MnO2→Cl2→KClO3→KCl→HCl→Cl2→Clorua vôi
a)
\(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
\(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\)
\(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3\downarrow+3NaCl\)
\(2NaCl+H_2SO_4\underrightarrow{t^o}Na_2SO_4+2HCl\)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
\(CuCl_2+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2AgCl\downarrow\)
b)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(H_2+Cl_2\underrightarrow{t^o}2HCl\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
\(FeCl_3+3AgNO_3\rightarrow Fe\left(NO_3\right)_3+3AgCl\downarrow\)
\(2AgCl\underrightarrow{as}2Ag+Cl_2\)
\(2NaBr+Cl_2\rightarrow2NaCl+Br_2\)
\(2NaI+Br_2\rightarrow2NaBr+I_2\)
\(Zn+I_2\underrightarrow{H_2O}ZnI_2\)
\(ZnI_2+2NaOH\rightarrow2NaI+Zn\left(OH\right)_2\)
c)
\(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
\(3Cl_2+6KOH\underrightarrow{t^o}5KCl+KClO_3+3H_2O\)
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(2KCl+H_2SO_4\underrightarrow{t^o}K_2SO_4+2HCl\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(Ca\left(OH\right)_2+Cl_2\rightarrow CaOCl_2+H_2O\)
Đúng 2
Bình luận (0)
Bài 1: Hoàn thành phản ứnga) MnO2 - Cl2 - HCL - Cl2 - Clorua vôib) KMnO4 - Cl2 - KCl - Cl2 - HCl - FeCl2 - FeCl3 - Fe(OH)3c) HCl - Cl2 - NaCl - HCl - CuCl2 - AgClBài 2: Hoà tan 15,3g oxit của kim loại M hóa trị II vào một lượng dung dịch HCl 18,25% thu được 20,8g muối. Xác định tên và khối lượng dung dịch HCl đã dùngBài 3: Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc, dư. Dẫn khí thoát ra đi vào 500ml dung dịch NaOH 4M (ở nhiệt độ thường)a) Viết phương trình hóa học của các phản ứng xảy rab) Xá...
Đọc tiếp
Bài 1: Hoàn thành phản ứng
a) MnO2 -> Cl2 -> HCL -> Cl2 -> Clorua vôi
b) KMnO4 -> Cl2 -> KCl -> Cl2 -> HCl -> FeCl2 -> FeCl3 -> Fe(OH)3
c) HCl -> Cl2 -> NaCl -> HCl -> CuCl2 -> AgCl
Bài 2: Hoà tan 15,3g oxit của kim loại M hóa trị II vào một lượng dung dịch HCl 18,25% thu được 20,8g muối. Xác định tên và khối lượng dung dịch HCl đã dùng
Bài 3: Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc, dư. Dẫn khí thoát ra đi vào 500ml dung dịch NaOH 4M (ở nhiệt độ thường)
a) Viết phương trình hóa học của các phản ứng xảy ra
b) Xác định nồng độ mol của những chất có trong dung dịch sau phản ứng (thể tích dd thay đổi không đáng kể)
bài 1
câu a:
Mn02 + 4HCl --> MnCl2 + Cl2 + 2H20
Cl2 + H2 -->t° ánh sáng 2HCl
4HCl + Mn02 --> MnCl2 + Cl2 + 2H20
Cl2 + 2Na -->t° 2NaCl
2NaCl -->điện phân nóng chảy 2Na + Cl2
câu b/
2KMnO4 + 16HCl (đ) -> 2KCl + 2MnCl2 + 5Cl2 + 8H2O (Đ.C Cl2)
Cl2 + KOH -> KCl + KClO3 + H2O
2KClO3 -> 2KCl + 3O2 (đ/c khí O2 lớp 8)
2KCl -> 2K + Cl2
Cl2 + H2O ->HCl + HClO
2HCl + Fe -> FeCl2 + H2
2FeCl2 + Cl2 -> 2FeCl3
FeCl3 + NaOH -> Fe(OH)3 + NaCl
câu c/
HCl ---> Cl2 ---> FeCl3 ---> NaCl ---> HCl ---> CuCl2 ---> AgCl
2HCl→Cl2+H2
3Cl2+2Fe→2FeCl3
3NaOH+FeCl3→3NaCl+Fe(OH)3
H2SO4+NaCl→HCl+NaHSO4
CuO+2HCl→2H2O+CuCl2
2AgNO3+CuCl2→2AgCl+Cu(NO3)2
Đúng 0
Bình luận (0)
Bài 2:
CTHH: MO
\(n_{MO}=\dfrac{15,3}{M_M+16}\left(mol\right)\)
PTHH: MO + 2HCl --> MCl2 + H2O
=> \(n_{MCl_2}=\dfrac{15,3}{M_M+16}\left(mol\right)\)
=> \(\dfrac{15,3}{M_M+16}\left(M_M+71\right)=20,8\)
=> MM = 137 (g/mol)
=> M là Ba (Bari)
\(n_{BaO}=\dfrac{15,3}{153}=0,1\left(mol\right)\)
PTHH: BaO + 2HCl --> BaCl2 + H2O
0,1-->0,2
=> mHCl = 0,2.36,5 = 7,3 (g)
=> \(m_{ddHCl}=\dfrac{7,3.100}{18,25}=40\left(g\right)\)
Đúng 0
Bình luận (0)
Bài 3:
a)
MnO2 + 4HCl --to--> MnCl2 + Cl2 + 2H2O
2NaOH + Cl2 --> NaCl + NaClO + H2O
b)
nNaOH = 0,5.4 = 2 (mol)
\(n_{MnO_2}=\dfrac{69,6}{87}=0,8\left(mol\right)\)
PTHH: MnO2 + 4HCl --to--> MnCl2 + Cl2 + 2H2O
0,8--------------------------->0,8
2NaOH + Cl2 --> NaCl + NaClO + H2O
1,6<--0,8----->0,8----->0,8
=> \(\left\{{}\begin{matrix}n_{NaOH\left(dư\right)}=2-1,6=0,4\left(mol\right)\\n_{NaCl}=0,8\left(mol\right)\\n_{NaClO}=0,8\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(NaOHdư\right)}=\dfrac{0,4}{0,5}=0,8M\\C_{M\left(NaCl\right)}=\dfrac{0,8}{0,5}=1,6M\\C_{M\left(NaClO\right)}=\dfrac{0,8}{0,5}=1,6M\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Thiết lập phương trình phản ứng oxi hóa - khử theo phương pháp thăng bằng electron?
Chỉ rõ chất khử, chất oxi hóa trong mỗi phản ứng.
1: NH3 + Cl2 - N2 +HCl
2: NH3 +O2 - NO + H2O
3: Al + Fe3O4 - Al2O3 + Fe
4: MnO2 + HCl - MnCl2 + Cl2 + H2O
5: HCl + KMnO4 - MnCl2 + KCl + Cl2 + H20
6: Cu + HNO3 - Cu(NO3)2 + NO + H2O
7: Zn + HNO3 - Zn(NO3)2 + NH4NO3 + H20
8: Al + HNO3 - Al(NO3)3 + N20 + H20
9: Al + H2SO4(đặc) -Al2(SO4)3 + SO2 + H20
10: KMnO4 + FeSO4 + H2SO4 - MnO4 + Fe2(SO4)3 + K2SO4 +H2...
Đọc tiếp
Thiết lập phương trình phản ứng oxi hóa - khử theo phương pháp thăng bằng electron?
Chỉ rõ chất khử, chất oxi hóa trong mỗi phản ứng.
1: NH3 + Cl2 -> N2 +HCl
2: NH3 +O2 -> NO + H2O
3: Al + Fe3O4 -> Al2O3 + Fe
4: MnO2 + HCl -> MnCl2 + Cl2 + H2O
5: HCl + KMnO4 -> MnCl2 + KCl + Cl2 + H20
6: Cu + HNO3 -> Cu(NO3)2 + NO + H2O
7: Zn + HNO3 -> Zn(NO3)2 + NH4NO3 + H20
8: Al + HNO3 -> Al(NO3)3 + N20 + H20
9: Al + H2SO4(đặc) ->Al2(SO4)3 + SO2 + H20
10: KMnO4 + FeSO4 + H2SO4 -> MnO4 + Fe2(SO4)3 + K2SO4 +H20
11: Cl2 + KOH -> KClO3 + KCl + H20
12: Fe + HNO3 -> Fe2(SO4)3 + SO2 + H20
13: FeS + H2SO4(đặc, nóng) ->Fe2(SO4) + SO2 + H20
1)\(N^{-3}H_3+Cl_2\rightarrow N^0_2+HCl\)
\(\left\{{}\begin{matrix}1\times|2N^{-3}\rightarrow N_2^0+6e\left(oxihóa\right)\\3\times|Cl_2^0+2e\rightarrow2Cl^{-1}\left(khử\right)\end{matrix}\right.\)
\(\Rightarrow2NH_3+3Cl_2\rightarrow N_2+6HCl\). Cl là chất oxi hóa và N là chất khử
2)\(N^{-3}H_3+O_2^0\rightarrow N^{+2}O+H_2O^{-2}\)
\(\left\{{}\begin{matrix}4\times|N^{-3}\rightarrow N^{+2}+5e\left(oxihóa\right)\\5\times|O_2^0+4e\rightarrow2O^{2-}\left(khử\right)\end{matrix}\right.\)
\(\Rightarrow4NH_3+5O_2\rightarrow4NO+6H_2O\). N là chất oxi hóa và O là chất khử
3)\(Al^0+Fe^{+\frac{8}{3}}_3O_4\rightarrow Al^{+3}_2O_3+Fe^0\)
\(\left\{{}\begin{matrix}4\times|2Al^0\rightarrow Al_2^{+3}+6e\left(oxihóa\right)\\3\times|Fe^{+\frac{8}{3}}_3+8e\rightarrow3Fe^0\left(khử\right)\end{matrix}\right.\)
\(\Rightarrow8Al+3Fe_3O_4\rightarrow4Al_2O_3+9Fe\)
Fe là chất khử và Al là chất oxi hóa