
Những câu hỏi liên quan
Cho sơ đồ phản ứng sau: Fe + 2HCl -> FeCl2 + H2
a. tính khối lượng sắt và axit HCl đã tham gia phản ứng, biết rằng thể tích khí hidro thoát ra là 3,361.(đktc)
b. tính khối lượng FeCl2 tạo thành?
giúp mình nhé !
a)
\(n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)\)
Phương trình hóa học : \(Fe + 2HCl \to FeCl_2 + H_2\)
Theo PTHH :
\(n_{HCl} = 2n_{H_2} = 0,3(mol)\\ n_{Fe} = n_{H_2} = 0,15(mol)\)
Vậy :
\(m_{HCl} = 0,3.36,5 = 10,95(gam) \\m_{Fe} = 0,15.56 = 8,4(gam)\)
b)
Bảo toàn khối lượng :
\(m_{Fe} + m_{HCl} = m_{FeCl_2} + m_{H_2} \\m_{FeCl_2} = 10,95 + 8,4 - 0,15.2 = 19,05(gam)\)
Đúng 2
Bình luận (0)
Fe + 2HCl-> FeCl2 + H2
theo phương trình:1 2 1 1 theo đề bài: 0,15 0,3 0,15 0,15 Số mol của H2: nH2=3,361:22,4≈0,15(mol) a)Khối lượng của các chất lần lượt là
mFe=0,15.56=8,4(g)mFe=0,15.56=8,4(g)
mHCl=0,3.36,5=10,95(g).mHCl=0,3.36,5=10,95(g).
b) Khối lượng của FeCl2: mFeCl2=0,15.127=19,059(g)
Đúng 1
Bình luận (0)
Sắt tác dụng axit clohiđric : Ta có phương trình hóa học sau : Fe + 2HCl → FeCl2 + H2
Nếu 1,4g Fe tham gia phản ứng hết với lượng dung dịch axít trên. Hãy tính :
a) Khối lượng axit Clohiđric cần dùng .(1,825g)
b) Thể tích khí H2 thu được đktc .(0,56 lít)
\(n_{Fe}=\dfrac{1.4}{56}=0.025\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.025.....0.05...............0.025\)
\(m_{HCl}=0.05\cdot36.5=1.825\left(g\right)\)
\(V_{H_2}=0.025\cdot22.4=0.56\left(l\right)\)
Đúng 3
Bình luận (0)
Sắt tác dụng với axit clohiđric : Fe + 2HCl → FeCl2 + H2↑.
Nếu có 2,8g sắt tham gia phản ứng em hãy tìm:
a) Thể tích khí hiđro thu được ở đktc.
b) Khối lượng axit clohiđric cần dùng.
a) PTPU

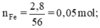
Theo pt: nH2 = nFe = 0,05 (mol)
VH2 = 22,4.n = 22,4.0,05 = 1,12 (l)
b) nHCl = 2.nFe = 2. 0,05 = 0,1 (mol)
mHCl = M.n = 0,1.36,5 = 3,65 (g)
Đúng 0
Bình luận (0)
Cho 11,2g sắt tác dụng vừa đủ với 400ml dung dịch axic clohdric (HCl) theo phương trình hoá học như sau: Fe+2HCl-> FeCl2+ H2
a. Tính số mol sắt đã phản ứng
b. Tính khối lượng FeCl2 thu được
c. Tính thể tích khí H2 (đktc)
d. Tính nồng độ mol của dung dịch HCl trước phản ứng
Giúp mình với ạ !!!! ☕
Mình cảm ơn ❤
a, nFe = 11,2/56 = 0,2 (mol)
b, PTHH: Fe + 2HCl -> FeCl2 + H2
Mol: 0,2 ---> 0,4 ---> 0,2 ---> 0,2
mFeCl2 = 0,2 . 127 = 25,4 (g)
c, VH2 = 0,2 . 22,4 = 4,48 (l)
d, CMddHCl = 0,4/0,4 = 1M
Đúng 2
Bình luận (1)
Fe + 2HCl -> FeCl2 + H2
Nếu có 2,8 g sắt tham gia phản ứng, em hãy tìm:
a) Thể tích khí hidro thu được ở đktc.
b) Khối lượng axit clohidric cần dùng.
chưa học tới đó ms học phần 2 ÙvÚ
a) PTPU
Tháy hình ko ạ , ko thấy = ib
a) Để tìm VH2 ,cần tìm n ( số mol chất)
m=2,8 ; M= 56
=> n= \(\frac{2,8}{56}\)
= 0.05 (mol)
n=0.05 =>V= n.22,4
= 0,05.22,4
=1,12(l)
Phần b) chưa học hihi sorry b
Cho 16,8g Fe tác dụng hết với dd HCl, sau đó phản ứng có H2 thoát ra:
a.Lập PTHH của phản ứng
b.Tính thể tích của khí H2 sinh ra (ở đktc)
c.Tính khối lượng FeCl2 sinh ra theo hai cách: Tính theo PT và dùng định luật bảo toàn khối lượng( cho bt H=1,Fe=56,Cl=35.5,S=32,Na=23)
mời các đồng chí giải giúp tôi ! XD
a.b.\(n_{Fe}=\dfrac{16,8}{56}=0,3mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,3 0,6 0,3 0,3 ( mol )
\(V_{H_2}=0,3.22,4=6,72l\)
c. Cách 1:
\(m_{FeCl_2}=0,3.127=38,1g\)
Cách 2:
\(m_{HCl}=0,6.36,5=21,9g\)
\(m_{H_2}=0,3.2=0,6g\)
Áp dụng ĐLBTKL, ta có:
\(m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\)
\(\Rightarrow m_{FeCl_2}=\left(16,8+21,9\right)-0,6=38,1g\)
Đúng 5
Bình luận (2)
sắt tác dụng với axit clohidric HCL theo sơ đồ phản ứng sau fe + HCL ---> FeCl2 +H2
nếu có 11,2 gam sắt tham gia phản ứng Hãy tính
a. khối lượng axit chohidric HCL cần dùng
b. thể tích khí hidro tạo thành ở đktc
( cho biết Fe = 56 ; Zn = 65 ; S=32; O = 16 ; K= 39; H=1 ; C=12; CL=35)
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
_____0,2_____0,4__________0,2 (mol)
a, \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
b, \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
Đúng 1
Bình luận (0)
Cho 5,6g Fe tác dụng vs dung dịch Axit Clohidric dư thu được muối sắt (2) Clorua FeCl2 và khí h2
a) hãy tính khối lượng muối fecl2 thu được
b) tính thể tích khi h2 thu được theo đktc
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{Fe}=0,1\left(mol\right)\)
a, \(m_{FeCl_2}=0,1.\left(56+35,5.2\right)=12,7\left(g\right)\)
b, \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 2
Bình luận (0)
cho 5,6 gam sắt (Fe) tác dụng hết với dung dịch HCl, tạo thành muối sắt (II) clorua (FeCl2) và khí hidro (H2)
a. Viết phương trình phản ứng?
b. Tính thể tích khí Hidro (H2) sinh ra ở (đktc)?
c. Tính khối lượng muối FeCl2 tạo thành ?
\(a.Fe+2HCl\rightarrow FeCl_2+H_2\\b.n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ n_{H_2}=n_{Fe}=0,1\left(mol\right)\\ \Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\\ c.n_{FeCl_2}=n_{Fe}=0,1\left(mol\right)\\ m_{FeCl_2}=0,1.127=12,7\left(g\right) \)
Đúng 2
Bình luận (0)


























